Artículos Especializados
Artículo especializado
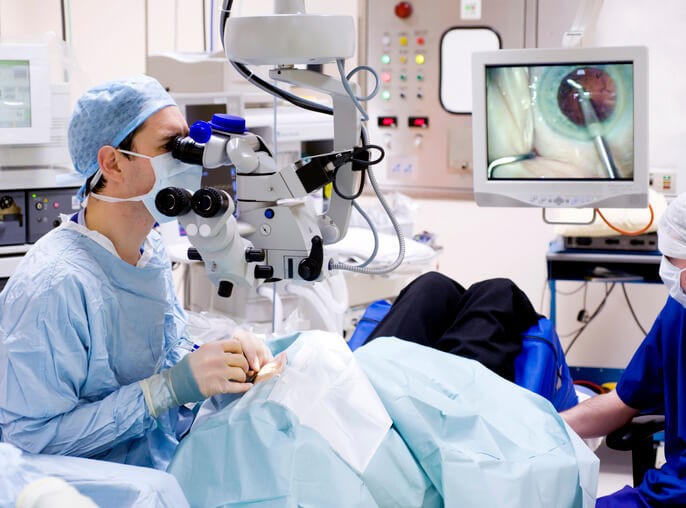
Cómo Saber si Tengo Cataratas
Habrás escuchado que, algún familiar, sobre todo los abuelos, padecen “cataratas”… pero, ¿sabes qué son y por qué se producen? Seguro que desconocías que es una enfermedad en la que la parte afectada es el cristalino.
Qué sabes del cristalino
El cristalino es una lente biconvexa, sólida y transparente, situada en el interior de la parte más anterior de la cámara posterior del globo ocular, por detrás entre la superficie posterior del iris (la parte coloreada del ojo) y por delante la parte anterior del cuerpo vítreo. Está formada, de fuera hacia adentro, por una cápsula transparente, que lo envuelve, una porción periférica, que es la corteza y una porción central, que se llama núcleo . Su función consiste en enfocar los rayos de manera que formen una imagen perfecta sobre la retina. Para alcanzar este resultado, es necesario que se produzca el fenómeno de “acomodación”, que consiste en un fenómeno de carácter reflejo que se produce gracias a la modificación de la forma del cristalino, que, a su vez, modifica su poder dióptrico (la capacidad de refracción de un sistema óptico viene expresada en dioptrías).
La emetropía es el estado refractivo del ojo normal en el que los rayos luminosos paralelos que lo atraviesan provenientes de un objeto situado en el infinito se reúnen y enfocan sobra la retina y forman una imagen precisa. Cuando este equilibrio se rompe y los rayos no se enfocan en la retina, aparece la “ametropía” o “defecto de refracción”.
Qué son
Se define como “ catarata ” toda opacidad del cristalino que afecta a la corteza o córtex o al núcleo . Pueden afectarse estas estructuras de forma total, sólo la zona central, la zona anterior (catarata con afectación anterior) o la posterior (catarata con afectación posterior), respectivamente. Las más frecuentes son las cataratas asociadas al envejecimiento , que progresan lentamente. En los países desarrollados la catarata congénita es responsable del 3% al 12% de todos los casos de baja visión y corresponde aproximadamente a seis de cada 100.000 niños.
Tipos de cataratas
Cataratas congénitas (o del desarrollo) uni o bilaterales (en los niños): el desarrollo de las fibras de la lente ha sido afectado por causas hereditarias o inflamatorias, con la pérdida consiguiente de transparencia. El 50% de ellas son de causa desconocida. Entre el 50% restante, de causa conocida, se incluyen las causadas por trastornos genéticos hereditarios, las infecciones (tipo TORCH), las metabolopatías (galactosemia, aciduria mevalónica), los traumatismos o las secundarias a tóxicos, entre otros ejemplos. La manifestación clínica más característica será la pupila blanca (leucocoria) con ausencia de reflejo rojo de fondo de ojo. Implican un importante déficit visual y pueden provocar nistagmo (movimientos involuntarios de los ojos). Todo ello podrá repercutir en un bajo rendimiento escolar.
Cataratas Degenerativas (en los adultos): la sustancia del cristalino, normalmente desarrollada, pierde su transparencia como resultado de alteraciones degenerativas, por varias causas. En este grupo se incluyen las siguientes:
Catarata senil: propia de la vejez.
Catarata metabólica (diabética…)
Catarata medicamentosa (p.ej. tratamientos con glucocorticoides tópicos o esteroides).
Catarata traumática (tras traumatismos oculares).
Catarata eléctrica.
Catarata por energía radiante (por el calor, la luz o las radiaciones ionizantes – p. ej. Rayos X -). La catarata provocada por el calor y la luz también ha sido denominada “ catarata de los vidrieros ”, trabajadores expuestos al calor y al brillo durante periodos de tiempo prolongados, de 10 o 20 años. También afecta a otra multitud de oficios en los que se emplean hornos a altas temperaturas o donde se trabajan metales fundidos, tales como fundiciones, talleres de cerámica e, incluso, herreros y panaderos. Los pacientes que reciben tratamiento con radioterapia también pueden verse afectados de cataratas.
Síntomas y diagnóstico
Las cataratas que se forman lentamente provocan una alteración gradual de la visión.
El diagnóstico debe incluir una prueba de agudeza visual , una exploración con lámpara de hendidura y un examen del reflejo rojo del fondo, sin y con dilatación pupilar, en el que se apreciará un reflejo rojo alterado al examinarlo con el oftalmoscopio.
Tratamiento
El único tratamiento posible de las cataratas es la extirpación quirúrgica del cristalino opacificado . La cirugía de la catarata es uno de los procedimientos quirúrgicos más comunes, y cada año se realizan en el mundo casi 22 millones de intervenciones. España es un país referente en la cirugía de la catarata con más de 400 intervenciones al año.
Suele realizarse, generalmente, bajo antestesia local y de forma ambulatoria . Se han efectuado grandes innovaciones técnicas que permiten aspirar la catarata, dejando la cápsula intacta (extracción extracapsular de la catarata), en lugar de retirar todo el cristalino junto con la cápsula (extracción intracapsular de la catarata). Seguidamente se coloca una lente intraocular que puede estar fabricada en distintos materiales en la cámara posterior de la cápsula del cristalino evacuada, sustituyendo a la lente natural: la visión se recupera rápidamente. Más del 95% de los enfermos operados de cataratas mejora la visión. En muchos casos, la cápsula lenticular del ojo, dejada durante la extirpación de las cataratas, acaba por opacificarse y produce una pérdida secundaria de la visión. La práctica de un pequeño orificio en la cápsula lenticular con un rayo láser restablece la claridad.
Pronóstico
Las cataratas congénitas o infantiles representan una amenaza para la visión y son un problema mucho más importante que en el adulto por su potencial en inhibir o detener la maduración y desarrollo visual normal en el niño, y por la mayor complejidad en el tratamiento. El pronóstico visual está relacionado con la edad del paciente en el momento del diagnóstico y con la precocidad del tratamiento quirúrgico y la rehabilitación óptica.

Artículo especializado
Cómo Operar el Estrabismo
El estrabismo es una patología de diagnóstico frecuente en la consulta de pediatría, y que afecta a un 4-5% de la población infantil. Los mismos padres, los profesores o cuidadores pueden observar y apreciar si un niño/a desvía un ojo. Manteniéndose siempre alerta en la observación de los más pequeños puede diagnosticarse el estrabismo precozmente y eso, seguro, repercutirá en un mejor pronóstico de la enfermedad.
La posición de los ojos adquiere su posición anatómica de los cuatro a seis meses de vida. Durante el primer mes la musculatura extraocular es capaz de proporcionar una fijación de la mirada estable y a partir de los dos meses el ojo puede realizar movimientos precisos para fijar la mirada sobre objetos situados en el campo visual. Desde los tres meses podrá realizar el seguimiento fino de un objeto en movimiento (hasta entonces el seguimiento es irregular). Si en el tercer mes de vida no se aprecia la fijación de la mirada del bebé, así como el seguimiento con la mirada de los objetos en movimiento en su campo visual, es conveniente llevar al niño a valoración por un especialista en oftalmología.
Durante los seis primeros meses de vida se puede considerar normal la desviación transitoria de uno o ambos ojos, ya que la visión binocular (la visión integrada de ambos ojos) no está perfectamente instaurada y sólo se consideran enfermedad las desviaciones permanentes .
¿Cómo ve una persona con estrabismo?
El estrabismo se incluye dentro del grupo de patologías de la motilidad ocular . Se produce cuando existe una pérdida del paralelismo de los ojos , es decir, cuando un ojo dirige la mirada hacia un punto del espacio y el otro se desvía a una dirección diferente. Cuando una persona padece estrabismo puede sufrir una disminución de la percepción de profundidad y de la visión en tres dimensiones.
En un ojo no fijado o estrábico, la imagen del objeto no se proyecta sobre la fóvea de la retina (una zona concreta de mayor capacidad visual), sino en una zona de la retina más o menos alejada de ella según sea la magnitud del ángulo de desviación. Esto hace que lleguen dos imágenes distintas al cerebro, una procedente de cada ojo, que tiende a descartar, suprimir o anular la imagen del ojo menos nítida. Con ello se originará la denominada ambliopía estrábica, causada por ese reflejo de supresión y que se manifiesta básicamente por una disminución de la agudeza visua l del ojo estrábico. Es decir, se puede acabar desarrollando el denominado “ojo vago u ojo perezoso” y si no se estimula precozmente puede acabar perdiendo la visión.
¿Qué causas tiene?
Las causas del estrabismo son múltiples y poco conocidas. Intervienen factores hereditarios, factores oftalmológicos como las cataratas congénitas o defectos de refracción , como la miopía o la hipermetropía. Todo esto sin olvidar que el control del alineamiento ocular, en última instancia, se produce en el cerebro, por lo que alteraciones a ese nivel también pueden desencadenarlo.
Síntomas
Los ojos se pueden desviar hacia dentro (endotropía o esotropía), hacia fuera (exotropía), hacia arriba (hipertropía) o hacia abajo (hipotropía).
Como norma general, debe tenerse en cuenta que, hasta los seis meses de vida, la incoordinación motora fisiológica es notable, por lo que será difícil valorar como patológico un estrabismo aparecido antes de esa edad.
¿SABÍAS QUE…?
Es importante diferenciar el estrabismo del pseudoestrabismo o falsa apariencia de estrabismo, que se produce debido, por ejemplo, a la forma peculiar del ojo denominada “epicantus”, muy frecuente en los primeros meses de vida (una deformación congénita o traumática en las razas occidentales o una forma del ojo normal en Asia o América).
El estrabismo intermitente, por su parte, consiste en que el niño desvía los ojos solamente en determinadas situaciones (al fijar un objeto en visión próxima o en la visión lejana, o en algunas posiciones de la mirada) mientras que el resto del tiempo controla bien la posición de los ojos. Puede aparecer por simple cansancio.
Diagnóstico
Ei estrabismo es uno de los motivos principales de consulta al especialista en oftalmología, de hecho, constituye la principal razón de la primera consulta. La detección del estrabismo se puede realizar mediante tests sencillos de aplicar como son la prueba de Hirschberg o la prueba del tapar-destapar (cover-uncover test).
Prueba de Hirschberg (esta prueba puede realizarse ya hacia los siete meses): consiste en la observación del reflejo luminoso corneal que aparece cuando el niño mira una luz proyectada por una linterna de exploración. La luz se emitirá desde unos 30-40 cm de distancia de los ojos, en el contexto de una iluminación ambiental poco intensa, para poder observar mejor los aspectos importantes. Se debe valorar si el reflejo luminoso queda centrado o descentrado en relación a la pupila. El examen se realizará desde el frente y en las diferentes posiciones de la mirada (arriba, abajo, izquierda, derecha).
En un caso normal, los reflejos de la luz se verán centrados simétricamente sobre ambas pupilas. Si el reflejo no queda centrado y simétrico se podrá sospechar un estrabismo.
Prueba del tapar-destapar (cover-uncover test) (esta prueba podrá realizarse a los tres o cuatro años): es la observación de la aparición de movimientos de fijación al tapar y destapar un ojo. Este método sólo puede utilizarse cuando existe una óptima y suficiente colaboración del paciente . Se debe solicitar que fije la mirada en una luz o algún pequeño objeto situado a unos 30-40 cm de distancia y posteriormente se debe tapar un ojo con un oclusor o con la mano. En el momento de tapar se observará si en el ojo no tapado tiene lugar algún movimiento de fijación que indicará la presencia de un estrabismo. De la misma forma, al destapar el ojo, se observará también si tiene lugar algún movimiento de fijación, que también sugerirá un estrabismo. Si la visión binocular (de ambos ojos) es normal no se observará ningún movimiento en el ojo tapado al destaparlo ni tampoco en el ojo no tapado. La maniobra se repetirá en el otro ojo igualmente, y siempre se procurará que el paciente mantenga el ojo no tapado fijado en la luz u objeto propuesto, sin efectuar ningún movimiento con la mirada.
Tratamiento y pronóstico
Algunos tipos de estrabismo pueden curarse con el simple uso de gafas . En algunos casos, podrá ser propuesta también una intervención quirúrgica. En los niños, la operación de estrabismo se realiza habitualmente con anestesia general mientras que en los adultos se puede realizar también con anestesia local y consiste en reforzar o debilitar los músculos oculares responsables de la mala alineación. No son operaciones complicadas; su única dificultad radica en la precisión del procedimiento, para conseguir los grados de reforzamiento/debilitación más exactos para corregir la desviación.
El ojo desviado es un ojo que no ha aprendido a ver, y por tanto hay que estimularlo y obligarlo a trabajar. Esto se consigue tapando el ojo que ve bien periódicamente con parches oculares adhesivos. La alteración anatómica del estrabismo (defecto estético) se podría corregir, en principio, a cualquier edad, pero las alteraciones sensoriales que provoca, que son mucha más importantes que las propiamente estéticas, sólo se pueden tratar durante la época de desarrollo o “de plasticidad visual”. Es decir, en el caso de los estrabismos, únicamente con un tratamiento precoz se puede conseguir la visión adecuada de ambos ojos.

Artículo especializado
Cuándo y Por Qué se Realiza la Operación de Fimosis
Seguro que en algún momento de la vida de tu hijo, te has preguntado si tiene o tendrá fimosis y si puedes hacer algo para evitarlo. Afortunadamente, la fimosis es un problema que tiene solución .
¿Qué es la fimosis?
La fimosis se define como un estrechamiento congénito (desde el nacimiento) o adquirido (a lo largo de la vida), de la abertura prepucial del pene.
Pueden diferenciarse dos tipos :
Con prepucio anatómicamente normal, es decir, asintomático, pero no retráctil (1% de los casos a los 16 años de edad).
Con prepucio no retráctil por la presencia de anillo fibroso o cicatrizal, debido a repetidos intentos de retracción.
Desarrollo anatómico normal
En el momento del nacimiento, existe en los bebés humanos una ‘ fimosis fisiológica’ , es decir, el prepucio del recién nacido no se retrae por la existencia de adherencias balanoprepuciales naturales en prácticamente la totalidad de los casos (es decir, en el momento del nacimiento, el prepucio está adherido a la superficie del glande del pene). Con el paso del tiempo, estas adherencias balanoprepuciales van desapareciendo de forma espontánea y gradual, por la presencia de esmegma (perlas blancas) y las erecciones intermitentes, permitiendo que el prepucio sea progresivamente más móvil y finalmente retráctil. A los tres o cuatro años de edad, 80% de los niños puede retraer el prepucio y a los 16 años, únicamente el 1% no lo podrá hacer, dándose lugar al diagnóstico de fimosis.
TENER EN CUENTA…
Se puede afirmar que hasta los 16 años de edad la fimosis es fisiológica y la actitud correcta ante ella es no hacer casi nada . La higiene diaria de los genitales con una suave retracción prepucial es suficiente. Las retracciones forzadas del prepucio convierten la fimosis fisiológica en patológica (cicatrizal). No es necesario ningún otro cuidado especial para su prevención.
Signos y síntoma
En ocasiones, la fimosis fisiológica y la fimosis cicatrizal pueden dar lugar a cuadros de :
Balanitis y balanopostitis (inflamación del glande e infección por hongos) de repetición.
Dificultad para la micción.
Dolor en las erecciones y dificultades en la ejecución del coito.
Existencia de episodios de parafimosis (cuadro clínico que se produce cuando se retrae un prepucio estrecho y no puede volver a su posición anatómica normal, quedando como un anillo que aprieta y ‘ahoga’ el glande, dando lugar a congestión venosa y tumefacción del mismo. Es una urgencia médica y las consecuencias de la parafimosis puede ser, incluso, la necrosis por isquemia –muerte por asfixia– de las células del glande).
Infecciones urinarias de repetición…
Tratamiento
Algunos autores optan por un primer tratamiento farmacológico de tipo pomada corticoidea tópica, con una tasa de éxito terapéutico descrito en los estudios clínicos de hasta el 80% de los casos. Indicada en todo tipo de fimosis, síntomas asociados y a cualquier edad.
La circuncisión es una de las intervenciones quirúrgicas que más se practica a los niños. Los motivos de su realización son muy diversos:
La presencia de fimosis fisiológica sintomática o fimosis patológica, que no ha respondido a tratamiento con corticoide tópico.
Principios religiosos y culturales (judíos, musulmanes…).
En algunos países, como EEUU o Canadá, se practican circuncisiones neonatales como medida preventiva (este debate no existe en Europa).
¿La operación tiene riesgos?
Obviamente, como en cualquier operación, existen riesgos inherentes a la cirugía, por muy sencillo que sea el procedimiento. Sin embargo, en este caso, la relación entre los bajos índices de consecuencias indeseables de la intervención, comparado con los enormes beneficios, hace que los riesgos apenas se tengan en cuenta .
Desde hace unos años se ha intensificado el f enómeno social de la inmigración en nuestro entorno , y esto obliga, particularmente a los profesionales de la salud, a saber interpretar las nuevas demandas formuladas por los nuevos colectivos. Si unos padres toman la decisión de realizar la circuncisión a su hijo por motivos personales, religiosos o culturales, deben ser informados sobre los conocimientos médicos del momento, referentes a los riesgos y beneficios de la intervención. Hay que permitir que se realice con garantías para la salud del niño, evitando circuitos y prácticas que serían un riesgo añadido.
En los adultos también se practican circuncisiones, siendo una operación generalmente realizada de forma ambulatoria y con muy buenos resultados . La recuperación es rápida, necesitándose tan sólo dos o tres días de reposo y unas pocas semanas de abstinencia sexual y/o esfuerzos físicos que puedan traumatizar la zona operada.
Artículo especializado
Fases y Evolución del Parkinson
¿Quién no tiene un conocido o familiar cercano afectado por esta enfermedad? ¿Sabes de dónde viene su nombre? Esta enfermedad fue descrita inicialmente con otro nombre por el Dr. James Parkinson en 1817. Posteriormente, otro científico lo modificó por Enfermedad de Parkinson en honor al médico que la describió en primer lugar .
¿En qué consiste esta enfermedad?
Es un proceso crónico y progresivo cuyo origen radica en la pérdida o degeneración de las neuronas que sintetizan el neurotransmisor dopamina en la sustancia negra (parte del cerebro cuyas neuronas producen la dopamina). La disminución en los niveles de dopamina da lugar a los síntomas de esta enfermedad.
Su causa es desconocida, pero se asocia a múltiples factores. Su prevalencia entre la población mayor de 60 años llega al 1%, siendo en mayores de 80 años superior al 4%. Es más frecuente en varones. En general, la edad y el antecedente de enfermedad de Parkinson en la familia son factores de riesgo para su desarrollo. Se habla de factores de riesgo genéticos en pacientes que inician la enfermedad en edad inferior a los 40 años (Parkinson precoz).
¿Cómo empieza a manifestarse esta enfermedad?
Sus síntomas iniciales suelen ser trastornos del movimiento pero, posteriormente, aparecen otras alteraciones en la progresión de la enfermedad como cambios en la función cognitiva , depresión , dolor , etc.
El inicio es lento e insidioso , lo que dificulta el diagnóstico en fases iniciales. Suele afectar inicialmente a un lado y, posteriormente, se hace bilateral.
Los síntomas típicos de esta enfermedad son:
Temblor : en manos, brazos, piernas, pies, mandíbula, lengua y cara. Está presente en aproximadamente el 80% de los pacientes. Se caracteriza por producirse en reposo. A veces se presenta al mantener una postura o al inicio de un movimiento, pero siempre es más intenso en reposo. Por curiosidad, ¿sabías que el temblor desaparece cuando la persona está durmiendo y empeora en situaciones de estrés?
Hipertonía muscular : rigidez en brazos, piernas y tronco. Puede afectar incluso a la expresión facial con disminución del parpadeo. Presente en el 90% de pacientes, suele comenzar en la misma extremidad que el temblor. La rigidez muscular ocasiona resistencia al movimiento pasivo (es la llamada rigidez en rueda dentada).
Bradicinesia : lentitud de los movimientos tanto voluntarios como involuntarios, sobre todo dificultad para iniciarlos y terminarlos. Ocasiona dificultad para movimientos de la vida cotidiana como pasear, levantarse de la silla, abrocharse los botones, vestirse, asearse, etc.
Problemas de equilibrio y coordinación por pérdida de los reflejos posturales . Aparecen en estadios más avanzados de la enfermedad. Proporciona una postura al caminar inclinado hacia delante y hacen movimiento de los brazos al caminar para aumentar su estabilidad. Ocasiona caídas frecuentes en estos pacientes.
Otros síntomas serían:
Alteraciones motoras : disminución del parpadeo, disartria (dificultad para hablar) disfagia (dificultad para deglutir), visión borrosa, cifosis dorsal, escoliosis…
Trastornos cognitivos y neuropsiquiátricos: demencia (30%), depresión (40%), ansiedad, ataques de pánico, alucinaciones y psicosis.
Trastornos del sueño, estreñimiento, alteraciones del olfato y sudor, dolor…
¿Es preciso realizar alguna prueba para confirmar el diagnóstico?
Ante la sospecha clínica de una enfermedad de Parkinson, el paciente debe ser derivado al neurólogo para una valoración inicial y la confirmación diagnóstica . El neurólogo instaurará el tratamiento farmacológico en función de los síntomas específicos del paciente.
Su diagnóstico es exclusivamente clínico. Existen unos criterios clínicos incluidos en una tabla que nos conducen al diagnóstico. Se centran en la severidad de las alteraciones motoras y en el grado de deterioro en las actividades diarias. Este diagnóstico debe ser periódicamente reevaluado para conocer la evolución.
En cuanto a pruebas diagnósticas te diré que, en ocasiones, solicitamos pruebas de imagen para descartar otras enfermedades que pueden tener síntomas similares , por ejemplo, la hidrocefalia. La prueba diagnóstica para confirmar o descartar la hidrocefalia es un TAC . En cambio, no existe ningún marcador bioquímico que oriente al diagnóstico de Parkinson.
¿Cómo valoramos entonces la progresión y la gravedad de la enfermedad?
Disponemos de unas escalas de valoración (las más frecuentemente usada es la de Hoenh y Yarh) para la clasificación clínica de la enfermedad. Según esta escala encontraríamos los siguientes estadios de la enfermedad:
Estadio 0: No hay signos de enfermedad.
Estadio 1: Enfermedad unilateral.
Estadio 2: Enfermedad bilateral, sin alteración del equilibrio.
Estadio 3: Enfermedad bilateral leve a moderada con inestabilidad postural, físicamente independiente.
Estadio 4: Incapacidad grave, aún capaz de caminar o permanecer de pie sin ayuda.
Estadio 5: Permanece en silla de rueda o encamado si no tiene ayuda.
¿Cuál es el pronóstico una vez debuta la enfermedad?
Existen unos marcadores que indicarán un peor pronóstico en cuanto al deterioro motor: edad avanzada en el momento del diagnóstico, la presencia de rigidez, situaciones médicas asociadas, inestabilidad postural y dificultad en los movimientos.
Sin embargo, cuando el temblor es el único síntoma inicial en el momento del diagnóstico, se considera un factor pronóstico favorable implicando una progresión más lenta de la enfermedad.
¿Existe un tratamiento específico para la enfermedad de Parkinson?
Tratamiento estándar o de confort : beneficiaría a estos pacientes, por ejemplo, la fisioterapia y la terapia ocupacional. Es importante mantener una nutrición adecuada, recomendar una dieta rica en fibra y una hidratación generosa. Mencionar también la existencia de los grupos de apoyo que ofrecen una ayuda importante tanto a los pacientes como a los familiares.
Tratamiento médico específico : no hay un consenso claro sobre cuál es el mejor fármaco para iniciar el tratamiento ni cuándo el momento preciso.
Uno de los fármacos de referencia es la levodopa. Considerado como el más eficaz en el control de los síntomas motores. Puede utilizarse como tratamiento único al inicio o asociarse a otros fármacos para conseguir mejor control de estos síntomas. Prácticamente la totalidad de los pacientes va a necesitar más de un fármaco tras cinco a siete años de tratamiento.
Debemos comentar un gran inconveniente asociado a este tratamiento : las complicaciones motoras (discinesias o movimientos involuntarios y fluctuaciones con episodios de movimientos lentos). La mitad de los pacientes pueden presentarlas después de cinco a 10 años de iniciar el tratamiento. Se cree que está relacionado con la dosis de fármaco, por ello, se recomienda el uso de la menor dosis posible.
En general, se decide iniciar el tratamiento médico cuando los síntomas afectan en la vida cotidiana ya sea por su gravedad como por sus complicaciones (afectación de la mano dominante, trastornos de la marcha, caídas frecuentes…). Una vez iniciado el tratamiento no puede interrumpirse de forma brusca, en caso de ser necesario lo haremos en dosis decrecientes.
Tratamiento quirúrgico : es el último recurso terapéutico en aquellos pacientes en los que no se consiguen controlar las complicaciones motoras a pesar de un correcto tratamiento farmacológico. Algunos de los tratamientos quirúrgicos actualmente disponibles son la estimulación cerebral profunda, la palidotomía, la talamotomía y la subtalamotomia. Existen otras opciones en investigación. Los resultados quirúrgicos son inciertos y no idénticos en todos los pacientes. Van a depender de muchos factores como técnica quirúrgica, perfil del paciente, progresión de la enfermedad, etc.
¿EL TABACO PROTEGE?
Te va a sorprender pero… se postula que el consumo de tabaco ejerce un efecto protector frente al riesgo de sufrir Parkinson. Otros de los posibles factores protectores que se enuncian son: ingesta de cafeína, té, alcohol, vitamina E, actividad física intensa, ingesta de antinflamatorios no esteroideos y estatinas. Pero, sólo lo comentamos a modo de curiosidad, así que, por favor, no te lo tomes al pie de la letra. Ya conocemos los efectos dañinos tanto del tabaco como del alcohol. Sin embargo, sí te recomiendo una actividad física intensa, ¿qué te parece?

Artículo especializado
Cómo Evitar la Parálisis del Sueño
Nada puede ser más aterrador que tu cerebro y tu cuerpo no se despierten al mismo tiempo . Aunque parezca mentira, esto no es una escena de una película de terror ni una experiencia paranormal, sino la realidad que viven las personas que han sufrido la llamada parálisis del sueño.
¿Qué es?
La parálisis del sueño es un trastorno muy común que se produce durante la transición del sueño a la vigilia (los minutos antes de despertarse), en los momentos previos a conciliar el sueño o bien justo al despertarse. Consiste en un despertar brusco con una conciencia plena de sus pensamientos pero con el cuerpo completamente paralizado. Es una sensación muy desagradable donde la persona se siente atrapada en su propio cuerpo.
Uno puede abrir los ojos pero no puede articular palabra ni mover un solo músculo . Esto genera un estado de angustia terrible hasta el punto de llevar a pensar que se está sufriendo algún trastorno grave. Es muy frecuente que, además, la persona presente alucinaciones visuales y auditivas, debido a que se encuentra en un estado entre la vigilia y el sueño.
La parálisis del sueño también se conoce como parálisis del sueño aislada, parálisis del sueño familiar, parálisis hipnopómpicas o hipnagógicas, parálisis predormital o postorbital.
¿A qué es debido?
Durante el sueño, pasamos por diferentes etapas o fases . La etapa de movimiento ocular rápido (REM) es la etapa donde soñamos. En ella se crea un mecanismo protector de nuestra integridad física que nos protege para no vivir ni escenificar nuestros sueños, y se llama atonía muscular (se anula la actividad de los músculos excepto el diafragma y los músculos de los ojos). Esta atonía se acaba cuando se pasa a otra fase de sueño o nos despertamos.
Pero si la persona se despierta durante el sueño REM, y este mecanismo de protección «atonía» continúa, le genera una incapacidad para moverse (parálisis) junto con sueños que la acompañan que son vividos como alucinaciones.
Por lo tanto, está estrechamente relacionada con la parálisis normal que ocurre durante el sueño REM . La fase REM se cuela, como un intruso, en el estado de vigilia. La persona está despierta, pero parte de su cerebro sigue todavía dormido. Como en la fase REM el movimiento ocular no es anulado, los pacientes que sufren parálisis del sueño, pueden abrir los ojos, pero son incapaces de mover el resto del cuerpo.
La parálisis del sueño se debe a una desconexión entre el cerebro y cuerpo.
Factores de riesgo
El estrés, los cambios de horario, el jet lag o el cansancio pueden favorecer la aparición ocasional de este fenómeno. Las circunstancias anteriormente descritas provocan que la persona alcance la fase profunda del sueño excesivamente rápido (antes de las primeras dos horas desde el inicio del sueño). En estos casos, descansar y recuperarse físicamente resuelve la situación.
La parálisis del sueño puede darse de manera periódica en pacientes que presentan trastorno bipolar, ansiedad, depresión y estrés post-traumático.
Las personas que padecen narcolepsia (excesiva somnolencia diurna) pueden tener mayor predisposición para padecer parálisis del sueño.
Síntomas
Este síndrome no pone en peligro la vida de la persona , pero las sensaciones que experimenta le hacen percibir que está en una situación muy grave.
La persona siente un miedo intenso y sensación de muerte inminente . Además, es muy frecuente que las alucinaciones tengan un carácter siniestro que empeora la situación emocional.
La sensación de parálisis dura unos dos minutos y recuperar el movimiento puede costar un poco . Cuando se presenta, los expertos recomiendan moverse y levantarse porque, el no hacerlo, puede favorecer que se repita el episodio de parálisis del sueño.
Tipos de parálisis del sueño
Típica o común
Es el más frecuente y sólo presenta parálisis, pero sin alucinaciones, y su duración es corta (de dos minutos como máximo).
Hipnagógica o alucinatoria
La parálisis se acompaña de alucinaciones y suele ser un episodio más largo, de hasta ocho minutos de duración. Es menos frecuente, pero se trata de u na experiencia aterradora ya que se percibe que una persona o presencia maligna está allí, como si alguien o algo está realmente sentado sobre ellos y sienten que se ahogan o se van a morir.
Tratamiento
El tratamiento principal es reducir el estrés, tener unos horarios de sueño regulares y dormir las horas suficientes para tener un sueño reparador. En los casos graves se pueden administrar fármacos para controlar la situación, como los antidepresivos.
Si los episodios son muy recurrentes se debe descartar alguna patología mental y debe ser valorado por un psiquiatra.
Artículo especializado
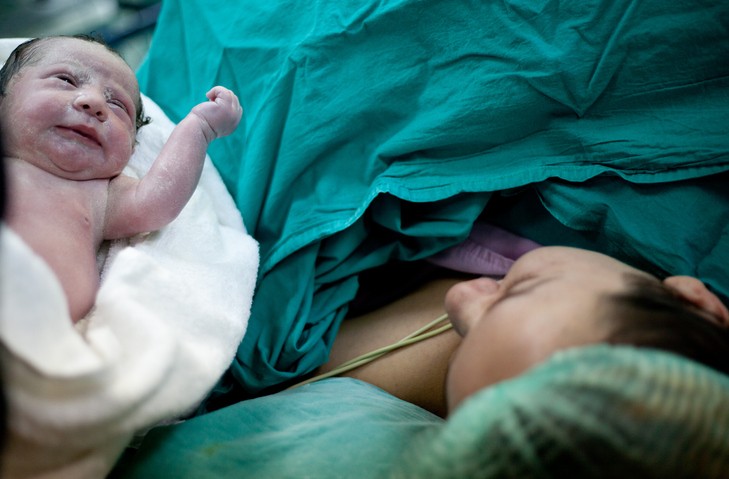
Preparación y Etapas del Parto
No hay dos partos iguales : el parto es un acontecimiento único, catártico, impredecible. Hay muchas variables en juego: el feto, con su forma y tamaño únicos, su posición… la pelvis materna, también con su forma y su tamaño, la placenta y el cordón umbilical suministrando oxígeno durante ese momento tan crítico, mientras el músculo uterino se contrae rítmicamente para abrir una salida y empujar el cuerpecito del recién nacido fuera. Las combinaciones son infinitas, por eso no hay dos iguales.
¿Cuándo sucede?
El parto se desencadena en la inmensa mayoría de mujeres unos tres o cuatro días antes o después de la fecha probable de parto (40 semanas desde la fecha de última regla en mujeres con ciclos regulares). El reloj biológico pone en marcha la secreción de una hormona desde el cerebro, llamada oxitocina, que será la responsable de que el útero se contraiga intensamente y de forma periódica empujando el contenido hacia el canal del parto. Esto hace que el cuello del útero, que es el órgano que hace de “puerta”, se vaya dilatando y que la presentación fetal, habitualmente la cabeza, vaya descendiendo por la pelvis a lo largo de la vagina hasta el exterior.
El orden deseable de los acontecimientos es que la bolsa amniótica se rompa durante el trabajo de parto cuando la dilatación ya está adelantada, por la misma presión provocada por las contracciones. Pero esto no siempre ocurre así, y en ocasiones se rompe accidentalmente la bolsa de las aguas antes de que se inicie el parto, y esto nos obliga a “provocarlo”, pues a partir del momento en que la bolsa está rota el feto deja de estar en su medio estéril y por tanto susceptible de sufrir una infección, así que, cuanto menos horas pasen entre la rotura de la bolsa y el parto, mejor.
El primer parto
El inicio del primer parto suele ser lento, y son frecuentes las “falsas alarmas”, en las que a las primerizas nos confunden las primeras contracciones, que suelen ser irregulares y de baja intensidad. Cuando se inicie de verdad el parto serán mucho más intensas y adoptarán un ritmo preciso, que nos permitirá predecir con exactitud cuándo se inicia la siguiente. Es frecuente que unos días antes del parto la gestante experimente conatos de contracciones, sobre todo por las tardes-noches, que no acaban de acelerarse y terminan cediendo. Si algo tiene el parto que lo hace inconfundible es que siempre va a más: se incrementa el dolor de las contracciones y se reduce el periodo entre ellas.
LAS CONTRACCIONES
Empiezan más espaciadas y se van acelerando , aceptando como norma que estamos de parto cuando hace una hora que se repiten a un ritmo de una cada cinco minutos aproximadamente. Desde el inicio del parto hasta el nacimiento de un primer hijo pasan de media unas ocho horas.
El segundo parto
El segundo parto o posteriores es muy distinto. Son frecuentes los partos que se inician de golpe, sin previo aviso , con contracciones que a veces ya son de alta intensidad y frecuencia desde el principio, y todo va mucho más rápido, reduciéndose el tiempo medio a la mitad.
El dolor
La tolerancia individual al dolor es variable , pero el dolor ocasionado por las contracciones podemos considerarlo como de alta intensidad , tanto es así que en nuestro medio es habitual administrar anestesia epidural durante la fase de dilatación. La anestesia epidural es infiltrar un fármaco a través de una punción en la parte baja de la espalda que dejará insensible al dolor la parte del cuerpo desde la zona de punción hasta los pies. Esto nos permite que la embarazada esté tranquila y sin dolor, sin afectar al bebé ni al ritmo de las contracciones.
La salida
Durante la fase de dilatación el cuello del útero se va abriendo hasta que permite el paso de la cabeza del bebé , en ese momento se llama dilatación completa y corresponde a unos 10 cm. Al mismo tiempo la cabeza va descendiendo a lo largo del canal del parto. La siguiente fase del parto se llama expulsivo, desde que la dilatación es completa hasta que el bebé sale. Esta fase puede durar aproximadamente una hora, pues el descenso de esos pocos centímetros a lo largo del canal del parto es lento, pues el espacio es escaso y la cabeza se va adaptando a la forma de la pelvis y el descenso lo hace a la vez que la cabeza va rotando. La manera que le resulta más eficiente para salir es ir girando 90º desde una posición en que mira a una de las caderas de la madre hasta colocarse mirando a su espalda, que es como saldrán la infinita mayoría de los bebés. Una vez la cabeza está fuera, ésta vuelve a girar en dirección contraria hacia la misma cadera que miraba inicialmente, eso le permite alinear los hombros con el diámetro máximo de la pelvis para que estos puedan salir. A partir de los hombros el resto del cuerpo sale con facilidad.
Una vez fuera, se secciona el cordón y se extrae la placenta que es un tejido carnoso en forma de disco de unos 20 cm de diámetro, que estaba hasta entonces adherido a una de las paredes del útero. La misma reducción de volumen que se produce al salir el bebé favorece que la placenta se despegue espontáneamente y se expulse con facilidad. Si esto no se produce de forma natural es importante extraerla manualmente de forma completa para evitar hemorragias postparto.
¿Parto espontáneo o inducido?
La vagina es muy elástica, y aumenta de capacidad para permitir el paso del feto sin problemas habitualmente, pero la parte más externa, la que limita con la piel de la vulva y el periné, que no son tan elásticos pueden desgarrarse fácilmente durante el expulsivo, para ello es importante que un profesional dirija ese periodo y proteja el periné para que no se desgarre o realice una episiotomía (corte preventivo) si es necesaria. En el postparto tendremos que tener un mínimo de cuidados e higiene con ese corte, pero a pesar de no siempre son pequeños y no estan en una zona demasiado limpia ni ventilada suelen curar sin dar problemas en la mayoría de casos.
S i el parto no se pone en marcha de forma espontánea en un margen de días suficiente después de la fecha probable del parto o hay algún motivo materno o fetal que aconseje finalizar la gestación antes de que se desencadene el parto espontáneamente puede ser necesario “provocar” el parto. En estos casos, los profesionales administramos la medicación que sustituye a las hormonas naturales del parto: prostaglandinas y oxitocina, para imitar lo que la naturaleza no ha hecho espontáneamente.
Los partos provocados cuando el cuello uterino está «maduro» o en segundos partos suelen evolucionar rápido, pero si las condiciones de partida no son buenas pueden durar muchas horas e incluso acabar en una cesárea por una inducción fallida. En ocasiones, los partos, tanto inducidos como espontáneos pueden terminar en cesárea después de haber invertido tiempo y esfuerzo. Es una sensación muy desagradable, pero hemos de comprender que es imposible predecir a priori la evolución de todos los partos, y que hemos de ser conscientes de que, como hemos dicho al principio, el fin es impredecible, y «no se sabe hasta que no se prueba».
En cualquier caso, el parto es un acontecimiento emocionante como ninguno, y cuando el resultado es que tanto la madre como el bebé están bien no nos replanteemos el camino que hemos recorrido hasta obtener ese resultado.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Artículo especializado
Consecuencias del Papiloma
El virus del papiloma Humano (VPH) es una familia de virus de los que existen más de 200 tipos diferentes, algunos de los cuales causan infecciones genitales. Es tan frecuente que se considera que casi todos los hombres y mujeres sexualmente activos pueden ponerse en contacto con el virus en algún momento de su vida . En determinados países, incluso, constituye la infección de transmisión sexual más frecuente.
De los 40 tipos que afectan la zona genital y anal sólo 15 se consideran de alto riesgo pues pueden llegar a desarrollar un cáncer. El resto son inofensivos o son responsables de las verrugas genitales. Los tipos que causan verrugas genitales (habitualmente los tipos 6 y 11) no son los mismos que los que pueden causar cáncer (los tipos más agresivos son los 16 y 18).
Verrugas genitales
Las verrugas genitales son lesiones cutáneas elevadas, rugosas, que suelen aparecer en grupos. No son precursoras de cáncer, son de comportamiento benigno y suelen responder bien a tratamientos médicos y a veces quirúrgicos. Suelen crecer en forma de brote, y en cuanto se erradican no suelen salir más en personas sanas con un buen estado inmunitario. Se ven habitualmente en la zona genital tanto de hombres como en mujeres y, en ocasiones, mucho más raramente, en la mucosa oral.
En cuanto a los otros tipos de VPH que no son responsables de las verrugas su presencia es invisible a menos que nos realicemos una citología cervical periódicamente.
¿Qué es la citología cervical?
Es una sencilla prueba que se realiza de forma indolora en el contexto de una revisión ginecológica. Se le llama también Papanicolau, en referencia al doctor que la describió por primera vez. Consiste en recoger una muestra de las células que se desprenden al “cepillar” el cuello uterino. Para poder obtener esta muestra se coloca en la vagina un “espéculo”, una especie de separador de las paredes vaginales para poder acceder al cuello uterino. Y la muestra se extiende en un cristal y se remite al laboratorio donde el citólogo la analizará.
¿Cómo se interpreta la citología?
Las células cervicales obtenidas se estudian al microscopio. Si son normales, tienen los rasgos “típicos” de las células cervicales normales, pero si estas células han sido infectadas por el virus del papiloma humano pueden presentar rasgos “atípicos” , es decir, la presencia del virus en su interior puede hacer que cambie su forma y de esta manera el citólogo interpreta que estas atipias (en grado leve, moderado o severo) son sugestivas de una infección por VPH. Cuando tenemos un diagnóstico de este tipo se puede pedir una prueba de laboratorio específica para confirmar la infección vírica y si esta infección es por uno de los tipos de alto riesgo. También se puede solicitar una prueba llamada colposcopia que consiste en mirar con un microscopio el cuello uterino con la ayuda de unas tinciones que nos resaltan el tejido afectado. Si es necesario, se toma una pequeña muestra de biopsia de esa zona para confirmar si existe una lesión cervical de bajo o alto grado.
¿Qué hay que hacer en caso de infección por el VPH?
Pues dependerá del tipo de virus y de la lesión que esté ocasionando:
Puede haber infección vírica sin alteración en la citología. En este caso, no hay tratamiento, pues no disponemos de tratamiento para el virus, solamente si es necesario se trata la lesión que el virus ocasiona en el cuello uterino.
Si la lesión observada es de bajo grado normalmente se hace un seguimiento pues una buena parte de estas lesiones desaparecen espontáneamente. Sobre todo, cuanto más joven es la paciente, más capacidad tiene de limpiar la lesión y el virus.
Si la lesión observada es de alto grado el tratamiento es quirúrgico, y consiste en extraer superficialmente el tejido cervical afectado. Normalmente, al extirpar la lesión también eliminamos el virus, pues lo más probable es que sólo haya virus en la zona afectada.
Una lesión cervical causada por un virus de alto riesgo que no se controla puede llegar a desarrollar un cáncer de cuello uterino con los años, por eso es tan importante realizarse revisiones ginecológicas periódicas, pues esta infección no da síntoma alguno y la manera de detectarla únicamente es realizándose una citología. Y haciéndose los controles adecuados diagnosticamos estas lesiones mucho antes de que se conviertan en cáncer.
¿Cómo se transmite?
La transmisión es por vía sexual únicamente, pero la infección puede estar latente durante años hasta que pueda detectarse en una citología . El virus puede contagiarse por vía oral y causar cáncer orofaríngeo o amigdalar (tanto a hombres como mujeres), aunque es rarísimo, pues el órgano diana al que el virus puede hacer daño con más frecuencia es el cuello uterino. A los varones no suele afectarles y a menudo simplemente actúan de transmisores (existe una baja incidencia de cáncer de la mucosa anal en varones homosexuales).
¿Cómo se previene la infección por VPH?
La prevención primaria es la vacuna . Desde hace seis o siete años disponemos en España de una vacuna para los serotipos más agresivos del virus, que nos protege del 85% de los cánceres cervicales. Se administra dentro del calendario vacunal a todas las niñas de 12 años, y está valorándose vacunar también a los niños como se hace en otros países.
La vacunación es muy importante porque este virus no deja inmunidad permanente cuando se contagia, pues afecta localmente a las células del cuello pasando desapercibido por nuestro sistema inmune. Por tanto, nos podemos reinfectar de nuevo tras haber limpiado una infección. La única manera de inmunizarnos correctamente es a través de la vacuna. Se escoge la edad de 12 años pues si no se han iniciado las relaciones sexuales nos aseguramos de que sea absolutamente útil, ya que la vacuna no tiene efecto terapéutico sobre una persona ya infectada, aunque tampoco le ocasionaría ningún perjuicio. Así pues, se recomienda la vacuna a cualquier edad para cualquier persona que esté en riesgo de infección.
La p revención secundaria es el uso de preservativo durante toda la relación sexual pues el contagio se produce por contacto piel con piel, no a través del intercambio de fluidos como otras infecciones víricas. Por este motivo, incluso utilizando preservativo es posible el contagio, aunque se minimiza el riesgo.
Por tanto ¿es una infección por el virus del papiloma sinónimo de cáncer? Rotundamente NO , pero como podría llegar a serlo, ante un diagnóstico de infección conviene ponerse en manos de un especialista. Y, para prevenir, hay que hacerse los controles periódicos, vacunarse y usar preservativo en los contactos sexuales con parejas ocasionales.

Artículo especializado
Ataxia: Qué Debes Saber
Ante todo, vamos a definir este síntoma para tenerlo bien claro de aquí en adelante. Esta palabra proviene del griego y quiere decir, literalmente, sin orden (a=sin, taxia=orden). Se trata de un síntoma derivado de la alteración en la capacidad de coordinar los movimientos voluntarios . Puede afectar a cualquier parte del cuerpo, desde una alteración de la marcha, hasta una alteración en los movimientos oculares o en la musculatura del habla. En cualquiera de estos casos, estaríamos hablando de ataxia. Entonces, ante una torpeza o descoordinación en un brazo o en ambas piernas o dificultades con el habla o al tragar hablaremos de brazo de atáxico, marcha atáxica, habla atáxica, y así sucesivamente.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Síntomas de varias enfermedades
No es síntoma específico de una enfermedad, sino que puede estar presente en diferentes enfermedades. Las causas pueden ser muy diferentes, por tanto, ante una ataxia. Así que por leve que parezca, debemos acudir inicialmente a la consulta del neurólogo para una primera valoración y despistaje de las principales enfermedades que se acompañan de la misma. En ocasiones no encontramos la causa de este síntoma y entonces le damos el nombre de ataxia idiopática (de causa desconocida). Puede afectar al cerebelo y a sus vías asociadas .
Voy a mencionarte algunas enfermedades, conocidas popularmente, que cursan con ataxia: la rabia , la encefalopatía espongiforme bovina (enfermedad de las vacas locas), la enfermedad de Wermicke (causada por un déficit de vitamina B1, muy frecuente en el alcoholismo crónico), ataxia por gluten (provocada por el consumo de gluten en pacientes que no lo metabolizan correctamente), ataxia telangiectásica (caracterizada por dar los primeros síntomas en edad muy temprana, sobre los 12-18 meses), etc.
Ataxia hereditaria
Este es uno de los dos grandes grupos en que se divide la ataxia. Es la ataxia transmitida por genes. En este caso podremos encontrar personas que manifiestan la enfermedad y personas portadoras (genes alterados, pero sin enfermedad).
Ataxia de Friedreich: es la más relevante dentro de este grupo, y consiste en la afectación progresiva del cerebelo y otras partes del sistema nervioso. Se debe a una alteración cromosómica. Para que se manifieste la enfermedad los dos brazos del cromosoma deben estar alterados (si sólo uno está alterado la persona será portadora pero no padecerá la enfermedad, pero podría transmitir el gen afectado a sus hijos). Sus síntomas suelen manifestarse entre los 5 y los 15 años. El síntoma inicial suele ser la dificultad en la marcha o marcha atáxica. Se caracteriza por una pérdida de sensibilidad , descoordinación en los movimientos , dificultad al tragar, dificultad al hablar y problemas cardíacos graves (sobre todo arritmias que suele causarles la muerte).
Ataxia no hereditaria
Este es el segundo gran grupo. En este caso, puede ser debida a un traumatismo, a una infección, a un tumor, al abuso de drogas, a una alteración hormonal … o incluso ser de causa desconocida.
Ataxia cerebelosa no hereditaria : aquí la alteración en la coordinación afecta al cerebelo (ubicado bajo la zona occipital), que es la central de coordinación de todos los movimientos. En su parte derecha se coordina el movimiento de la parte derecha del cuerpo y en su parte izquierda la del izquierdo. La parte central coordina los movimientos de andar o caminar. Otras partes del cerebelo ayudan a coordinar los movimientos de los ojos, el hablar y el tragar.
Ataxia sensitiva: también la mencionamos por tratarse de un desorden en la recepción del estímulo propioceptivo procedente de los miembros inferiores. La persona no es capaz de identificar cuál es su posición en el espacio, de forma que no percibe correctamente su forma de caminar ni la superficie por donde lo hace. Precisa dar pasos grandes para no perder el equilibrio y caminar lentamente y con cautela ayudándose visualmente para vencer los obstáculos. Tienen dificultades para caminar por superficies irregulares o con poca iluminación. Presentan una gran inestabilidad y sufren caídas frecuentes.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
¿ATAXIA MENSTRUAL?
Como curiosidad voy a mencionarte la llamada ataxia menstrual por tratarse de una secuencia irregular de ciclos y de diferente duración . Es frecuente en mujeres de entre 35 y 40 años de edad con una base hormonal alterada. Se le da el nombre de ataxia por el desorden en el tiempo. La mujer afectada sufre de ciclos muy irregulares y de duración arbitraria.
Diagnóstico
Es difícil la detección precoz de la ataxia hasta que no empieza a dar síntomas. Sólo en los casos con una base hereditaria se realiza un cariotipo (estudio genético).
Sin embargo, cuando los síntomas comienzan a florecer se realiza una batería de pruebas diagnósticas entre las que se incluye, igualmente, estudio genético. En caso de detectarse un caso hereditario se estudian los familiares directos (consanguíneos) del paciente.
De entre las posibles pruebas a realizar tenemos que mencionar que algunas de ellas se realizan sólo ante la aparición de determinados síntomas.
Tomografía computarizada (TC) y resonancia magnética (RM) : estas pruebas de imagen permiten estudiar el sistema nervioso central y descartar posibles causas (tumores, infecciones, malformaciones…).
Estudio genético : permite confirmar el diagnóstico en el caso de las ataxias hereditarias.
Punción lumbar : se realiza si se sospecha una causa infecciosa. El análisis del líquido cefalorraquídeo permite descartar algunas enfermedades.
Audiometría: en caso de hipoacusia o sordera
Electrocardiograma y ecografía cardíaca en caso de arritmias u otros síntomas cardíacos.
Electromiografía: para estudio de la conducción nerviosa periférica.
Tenemos que confesar que, en algunos casos, no conseguimos encontrar la posible causa de este síntoma por lo que la ataxia será catalogada como idiopática o de causa desconocida.
¿Existe un tratamiento específico?
No existe un tratamiento específico, a menos que no se detecte una causa específica que origine la ataxia. Me refiero, por ejemplo, a una ataxia infecciosa, que debería ser abordada con el agente antimicrobiano específico.
Como hemos indicado al inicio, esta afectación puede ocasionar diferentes síntomas por lo que los iremos abordando médicamente en función de la especialidad que corresponda.
Normalmente estos pacientes son controlados por el neurólogo, quien sigue la evolución de la enfermedad, pero paralelamente siguen controles por el otorrinolaringólogo (si tienen hipoacusia -disminución de la capacidad auditiva-) o por el cardiólogo (si tienen arritmias), etc.
Cualquier enfoque terapéutico va dirigido a enlentecer la evolución de la enfermedad y a tratar los síntomas que aparezcan. Obviamente, tenemos que ser conscientes de que el paciente va a precisar de unas atenciones especiales como pueden ser fisioterapeuta, terapeuta ocupacional y ajustes en el entorno domiciliario para llevar a cabo sus actividades de la vida cotidiana. No debemos descartar la intervención de terceras personas si pierde su capacidad de autonomía personal.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Artículo especializado
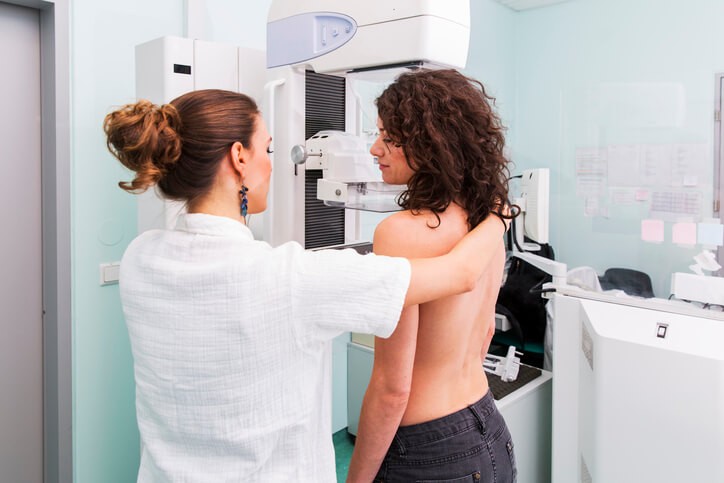
Qué Debes Saber Sobre la Mamografía
La importancia de la mamografía radica en que permite detectar el cáncer en algunos casos dos años antes de que éste sea palpable y detectable, tanto por el médico como por la propia paciente. La mamografía es una prueba de imagen radiológica que permite explorar las mamas y detectar precozmente el cáncer de mama .
Sobre el cáncer de mama…
El cáncer de mama es el tumor más frecuente en las mujeres occidentales. De hecho, se considera que una de cada ocho de nosotras desarrollará un cáncer de mama a lo largo de su vida. Por ello es tan importante su diagnóstico precoz , basado en la mamografía de control, para diagnosticarlo en sus primeras etapas, pues en esta fase casi todos se pueden curar.
La mamografía permite detectar el cáncer en algunos casos dos años antes de que éste sea palpable y detectable , por el médico o por la propia paciente. Utiliza rayos X de baja dosis para tener una imagen de la trama que dibuja el tejido mamario. Inicialmente el cáncer se diagnostica por distorsiones de esta trama o agrupaciones de pequeños depósitos de calcio que harán sospechar el inicio de un tumor maligno de mama.
¿Cómo se obtiene la imagen?
Técnicamente para obtener esta imagen habrá que colocar la mama en el mamógrafo y ponerla entre dos planos de fibra de metacrilato, que tienen la finalidad de comprimir la mama para extender al máximo el tejido e inmovilizarlo para que la imagen sea lo más nítida posible. Las proyecciones habituales de rutina son de arriba a abajo y de perfil de ambas mamas , es decir, cuatro proyecciones (o “fotos”) en total. Esta compresión puede resultar discretamente molesta o algo dolorosa en pacientes especialmente sensibles, pero en cualquier caso es una molestia puntual, el procedimiento dura escasos minutos y habitualmente no persiste la incomodidad una vez finalizada la prueba.
¿Cómo acudir a realizarse la mamografía?
Para realizar una mamografía no es necesaria ninguna preparación . Como única recomendación mencionaremos no utilizar según qué tipo de desodorantes o lociones que puedan tener talco o minerales pues pueden hacer opacificar la imagen obtenida. Por otro lado, y para minimizar la molestia que puede ocasionar, es preferible realizar la mamografía los días posteriores a la regla , pues durante la menstruación y los días previos los senos suelen estar más sensibles. Los rayos X no persisten en los tejidos después de realizar la prueba, con lo que se puede llevar a cabo, si es necesario, en madres lactantes.
¿Cómo se realiza?
Una vez el técnico de radiología ha colocado las mamas en la posición adecuada se proyectará una baja dosis de rayos X sobre las mamas , que atravesarán todo su grosor componiendo una imagen sobre un “medio”. Este “medio” clásicamente era una placa de radiografía que se revelaba como una fotografía, pero actualmente los mamógrafos utilizan sistemas digitales en los que la imagen se compone de sistemas electrónicos igual que las cámaras digitales y se pueden revisar en la pantalla del ordenador y transportarse en un CD.
En función de la densidad de cada tejido se absorben más o menos rayos X, por tanto, la cantidad de rayos que atravesarán todo el grosor quedará más o menos atenuada como sucede cuando la luz impacta sobre el negativo de una fotografía: si emitimos los rayos X sobre el aire, sin que tengan que atravesar ningún tejido, todos los rayos emitidos llegarán a la placa o sistema digital, con lo que quedará totalmente “negro”. Si el tejido atravesado es muy denso, como un hueso, un metal o una prótesis el tejido absorberá casi todos los rayos y apenas llegarán rayos a impactar en la placa, con lo que la silueta trazada sobre la radiografía será “blanca”. Si los tejidos son intermedios, como grasa y músculos, serán más o menos “grises” según su densidad. De este modo es como se componen las imágenes de las radiografías y mamografías.
Los mamógrafos han sufrido una importante evolución en los últimos años, disminuyendo mucho la cantidad de irradiación necesaria , concentrando los rayos sobre el tejido a estudiar y así evitando la dispersión y exposición de otros tejidos, y mejorando la resolución de la imagen en soportes digitales. Se ha introducido la tomografía digital en la exploración mamaria que, al hacer un “barrido” sobre toda la mama, permite componer imágenes en tres dimensiones.
Aun así, no se puede negar que hay un impacto de los rayos X sobre los tejidos, pero hoy en día, con los aparatos actuales, se puede asegurar que el riesgo que suponen es absolutamente asumible y compensa con creces el beneficio obtenido al poder diagnosticar los tumores de mama con tanta precocidad.
¿Cuándo hacerse una mamografía?
Los protocolos de frecuencia de mamografías de cribaje varían de unos países a otros, y se basan en criterios de salud, pero sobre todo económicos. El protocolo del colegio de radiólogos de Estados Unidos y del Instituto Nacional del Cáncer recomienda una mamografía anual a partir de los 40 años en mujeres sin riesgo añadido de cáncer de mama.
Pueden haber circunstancias que le resten resolución a la mamografía y, por tanto, nos coloquen en situación de riesgo de que una lesión pase desapercibida, como puede ser el caso de pacientes portadoras de prótesis mamarias y de mamas muy “densas”, muy “fibrosas”. En estos casos es de ayuda complementar el estudio mamográfico con una ecografía mamaria. Habitualmente, cuanto más joven es la mujer, más densas son sus mamas, por lo que es común solicitar el complemento de la ecografía a las mujeres en edad menstrual.
MAMOGRAFÍA Y ECOGRAFÍA MAMARIA
Quizás te preguntes: ¿por qué no realizamos ecografía mamaria en lugar de mamografía para ahorrarnos el tema de la irradiación? Pues no es equivalente: la prueba realmente eficaz para el diagnóstico precoz es la mamografía , la ecografía es complementaria para sacar más información a una imagen dudosa en la mamografía o como prueba única en mujeres muy jóvenes en las que no se pretende hacer un despistaje de cáncer sino hacer un estudio con sospecha de benignidad.
Conservar las mamografías previas
No hay dos mamas iguales, cada una es característica, como las huellas digitales, y el patrón de cada una, aunque puede irse modificando a lo largo de los años, se mantiene constante en su estructura. Por este motivo, es importante conservar las imágenes de mamografías previas y aportarlas en futuros exámenes pues son de ayuda para observar cambios evolutivos . Informa al centro si te has sometido a alguna cirugía en la mama pues obviamente las cicatrices de los tejidos se plasmarán en la imagen obtenida.
¿Y si se observa una imagen sospechosa?
Si en una mamografía se observa alguna imagen sospechosa puede ser que el radiólogo indique la práctica de nuevas proyecciones en otra posición , y en ocasiones se proponga una punción o biopsia para analizar los tejidos. Esto no tiene por qué ser sinónimo de sospecha de cáncer, pues actualmente la tendencia es la de biopsiar lesiones de aspecto benigno para efectivamente confirmar su benignidad. Y si desgraciadamente la sospecha es de malignidad y así lo confirma la biopsia ten siempre una actitud positiva porque, como he dicho al inicio, actualmente la mayoría de los cánceres de mama se curan.
Por tanto, mi recomendación es hacerse los controles periódicos, pues es mucho lo que nos puede beneficiar este acto.
Artículo especializado
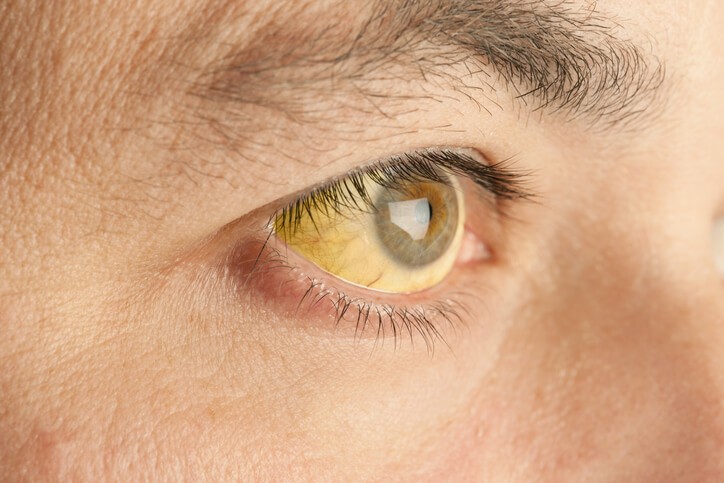
Control del Nivel de Bilirrubina
El cantante Juan Luís Guerra puso de moda este parámetro analítico hace unos años con su famosa canción. Sin embargo, los médicos empleamos este parámetro a diario y no hemos conseguido popularizarlo. Si te parece, vamos a darle un poco de protagonismo. Y a ver si al finalizar esta lectura eres capaz de asociar estos términos te menciono: bilirrubina, hígado, ictericia y enfermedad de Gilbert.
¿Qué es la bilirrubina?
La bilirrubina es un pigmento de color amarillo-anaranjado. Se trata de un producto de desecho que proviene de la destrucción del grupo hemo presente en la hemoglobina de los hematíes o glóbulos rojos.
El hígado interviene favoreciendo su eliminación. Si medimos el nivel de bilirrubina en sangre podremos evaluar la correcta función hepática , así como los niveles de destrucción del grupo hemo de los hematíes. Seguro que ya estás asociando que una posible causa de un aumento de bilirrubina puede ser debida a un aumento en la destrucción de hematíes, por lo que podríamos estar ante una anemia hemolítica (por destrucción de hematíes).
Déjame recordarte que la vida media de los hematíes es de 120 días (circulan por la sangre durante cuatro meses). Por eso al donar sangre debemos tener presente si ha habido suficiente tiempo de regeneración desde la última donación.
El hematíe dañado o viejo libera a la sangre el grupo hemo de su hemoglobina que se descompone dando lugar a la bilirrubina no conjugada (poco soluble en agua) que es transportada por proteínas desde la sangre al hígado. En el hígado existe una enzima llamada glucuronosiltransferasa que la modifica convirtiéndola en una forma soluble en agua o bilirrubina conjugada que pasa a formar parte de la bilis y se vacía en el intestino delgado. Finalmente se elimina por las heces. ¿Sabías que el color marronoso de las heces es debido a los productos de degradación de la bilirrubina?
Aumento de bilirrubina
Las pruebas de laboratorio permiten medir ambas formas de bilirrubina, conjugada o directa y no conjugada o indirecta, así como la bilirrubina total (suma de las dos anteriores).
Si aumentan los niveles de bilirrubina en sangre puede aparecer ictericia , es este caso la piel, la conjuntiva ocular y las mucosas tomarán un color amarillento.
Si sospechamos que existe un aumento de bilirrubina no conjugada sucede lo que seguramente has pensado, que aumenta la destrucción de hematíes (hemólisis) o bien una enfermedad hepática que no permita la transformación de la bilirrubina no conjugada en conjugada.
Un aumento de bilirrubina conjugada indica una dificultad en la eliminación, por ejemplo, una obstrucción de los conductos biliares.
¿Qué les pasa a los bebés al nacer?
Especialmente durante los tres primeros días, puede darse la llamada ictericia fisiológica del recién nacido. Se debe a una inmadurez del hígado del bebé para metabolizar la bilirrubina. No suele precisar tratamiento y desaparece a las dos semanas.
¿Cuándo solicitamos una determinación de bilirrubina?
El médico suele solicitar la determinación de la bilirrubina juntamente con otras pruebas de laboratorio (fosfatasa alcalina, AST, ALT) cuando existen signos o síntomas de función hepática anormal como Ictericia, c onsumo excesivo de alcohol, posible toxicidad de fármacos o posible hepatitis , coloración oscura de la orina, náuseas y vómitos, dolor o inflamación abdominal, fatiga extrema, etc.
¿Cómo se interpreta el resultado?
Aumentos de bilirrubina total a expensas de la bilirrubina no conjugada o indirecta suelen deberse a anemia hemolítica o anemia perniciosa, cirrosis o un síndrome de Gilbert u otros trastornos metabólicos. Ante una bilirrubina conjugada o directa aumentada puede existir un problema asociado a una disminución de la eliminación hepática, como puede suceder en hepatitis víricas, reacciones a fármacos, enfermedad por alcoholismo, litiasis u otras obstrucciones en los conductos biliares o tumores. Debo mencionarte que una concentración baja de bilirrubina no tiene relevancia.
¿En qué consiste el síndrome de Gilbert?
Es frecuente y se trata de una enfermedad hereditaria debida a una alteración en el cromosoma 2. Se caracteriza por un aumento de bilirrubina no conjugada y un déficit aproximado del 30% de la enzima glucuronosiltransferasa (que transforma la bilirrubina no conjugada en conjugada). Se traduce en una disminución de la capacidad de metabolizar la bilirrubina indirecta en directa en el hígado (para después ser excretada por la bilis). El diagnóstico se realiza tras la detección de una ictericia leve e intermitente en la adolescencia, entre los 15 y los 30 años. Al realizar una analítica nos encontraremos unos niveles elevados de bilirrubina indirecta o no conjugada y disminuidos de la conjugada. A pesar de que puede ser preciso realizar un estudio genético para confirmar el diagnóstico se trata de una patología totalmente benigna y clínicamente irrelevante. No precisa ningún tratamiento específico.
Efectivamente existen otros síndromes que cursan con hiperbilirrubinemias conjugadas como los síndromes de Rotor y de Dubin-Johnson, que son mucho menos frecuentes.
¡Ojo! Existen otras causas que pueden ocasionar un aumento de bilirrubina total, por ejemplo: hemólisis, un ayuno prolongado (si ingerimos menos de 400 kcal/día a las 48 horas encontraremos unos niveles multiplicados por tres que se normalizan tras 24 horas de volver a una dieta normal), fiebre, ejercicio físico o estrés, deshidratación, infecciones , cirugía, menstruación, etc.
Una curiosidad, ¿se puede encontrar bilirrubina en la orina?
En condiciones normales, no. No obstante, recordemos que la bilirrubina conjugada o directa es soluble en agua . Si los niveles de bilirrubina están muy aumentados en el organismo es posible que se elimine parte del exceso por la orina. Por tanto, ¿es posible encontrar bilirrubina en orina? Sí, pero sugiere una patología como puede ser una obstrucción en los conductos hepáticos o biliares, una hepatitis u otra lesión de origen hepático. La forma de detectar bilirrubina en orina es mediante la recogida de una muestra en condiciones de máxima esterilidad donde introduciremos una tira reactiva que vira el color cuando la detecta. La detección casual de bilirrubina en orina obliga a la solicitud de una analítica sanguínea para estudiar los parámetros correspondientes en sangre (ahora ya sabes que pediremos bilirrubina directa, bilirrubina indirecta y bilirrubina total).

Artículo especializado
Claves para Aumentar tu Autoestima
La autoestima es el resultado final de la suma de opiniones que tiene una persona de sí misma (apariencia física, aptitudes, éxitos profesionales, personales, vida afectiva…), que le ayuda a aceptarse tal y como es, a protegerse de las críticas negativas y a creer en sus propias aptitudes para hacer frente a la vida. ¿Pero cómo se construyen estas opiniones?, ¿de dónde viene que la percepción de nosotros mimos sea negativa o positiva?
Así se construye
La autoestima se construye con el contacto con las personas y depende del trato y los mensajes recibidos por los que nos han educado. Los padres en primer lugar, la familia, los amigos y los profesores después, todos, a su manera, tienen una influencia sobre la percepción que tenemos de nosotros mismos, porque los mensajes escuchados a una temprana edad, se graban profundamente y se acaban transformando en nuestro diálogo interior, haciendo que nos sintamos seguros de nosotros mismos o escondiendo al resto nuestra identidad por miedo al rechazo.
No es inmutable
Pero si los primeros años de vida ejercen un papel tan importante en el desarrollo de una autoestima saludable, ¿es posible hacer algo como adultos para cambiarlo?, ¿se puede aumentar la autoestima a pesar de no tener unas buenas bases? La respuesta es sí e indudablemente. En la madurez, el entorno adquiere un papel muy importante que se va sumando a las influencias experimentadas en la infancia, así, los éxitos, los errores, los fracasos…, pueden ir modificando la sensación de autoconfianza, autoeficacia, dignidad y en definitiva, seguridad en uno mismo. Y aunque nuestras figuras educadoras nos hayan dado elementos importantes positiva o negativamente para el desarrollo de una autoestima sana, sólo a nosotros como adultos nos corresponde tomar la decisión de realizar maniobras para poder cambiarlo.
Así se puede potenciar
Por ello, viendo que la autoestima es algo que podemos desarrollar a lo largo de toda la vida y que, a la par, tiene un claro valor de supervivencia, te proponemos, mediante estas pautas y consejos, empezar a potenciarla:
No dejes para mañana lo que puedas hacer hoy. La fuerza de voluntad, el autocontrol y la disciplina favorecen tener una buena autoimagen; por ello, hacer de inmediato aquello que se debe hacer, y no dejarlo para más tarde, aumenta considerablemente la autoestima. Se trata de pasar a la acción y no quedarse “enganchado” en el pensamiento ya que puede ser autodestructivo. La motivación llegará a medida que avances en la acción y el beneficio recaerá directamente sobre la autoestima. “No esperes a tener ganas de ir al gimnasio para apuntarte; apúntate y vendrán las ganas de continuar”.
Utiliza la “lupa” para rescatar lo positivo. Hay personas con tendencia a ignorar o desvalorizar los aspectos positivos y únicamente subrayan lo que ha ido mal. Si eres uno de ellos, complementa tu pensamiento con la otra cara de la moneda y fíjate en los aspectos que han funcionado bien. Esto te ayudará a romper con esa actitud negativa que obstaculiza que te enfrentes a nuevas experiencias y tu autoestima se verá reforzada. “La buena noticia es que la manera de pensar se puede modificar, sólo requiere que empieces a entrenar”
Muéstrate tal y como eres. No tengas miedo a expresar emociones profundas y comparte con los demás, lo bueno y lo malo de ti. Descubre al resto esa “cara oculta” que sólo tu conoces y escondes a los demás. Relacionarte emocionalmente con libertad, favorece que los demás empaticen contigo y recibas el sosiego de que el otro capta tu estado interno, a la par que se fortifica la autoestima. Piensa: “¿Qué aspectos tuyos te gustaría revelar a los demás?”
Afronta los cambios en vez de rechazarlos. Acepta que la vida es cambio y no está bajo tu control que las cosas fluyan a tu gusto. Resistirse, quejarse y resignarse no hacen más que estancarte en un momento temporal sin conseguir evolucionar. Si un cambio viene a ti, tienes que encontrar la forma de cambiar con él, si no, el sufrimiento estará garantizado y la autoestima se verá tocada. “Si tu empresa está avanzando en su expansión internacional, puedes quedarte parado/a o mejorar tu nivel de inglés de una vez por todas”.
Enfréntate a los conflictos en vez de evitarlos . No sirve de nada ignorar el conflicto, ya que lejos de desaparecer, crece la incertidumbre hasta que éste se resuelve. Así que soluciona las cosas cuanto antes y enfréntate a las emociones desagradables que genera, de este modo, no tendrás que arrastrarlas durante tiempo hasta reunir la valentía de hacerlo. “Soluciona ese problema con la compañera de trabajo que llevas arrastrando desde hace años, enfréntate para que la emociones que acompañan a la retención del conflicto puedan desaparecer”.
Asume riesgos calculados en vez de elegir exclusivamente la seguridad . Si quieres evolucionar y sentirte competente es necesario salir de la zona de confort. Si no lo haces, seguramente siempre te quedes en el momento actual por temor a fracasar. Correr riesgos es algo necesario para poder alcanzar nuestras metas y conocer donde están nuestros límites. “Atrévete con ese proyecto que llevan tiempo proponiéndote, puede salir bien y conseguir una meta o fallar y aprender de ello”.
No te compares con los demás . En las comparaciones, tendemos a exaltar las cualidades de los otros y a minimizar las propias; este proceso llevado a cabo de forma continuada provoca que la autoestima baje. Es más útil reconocer las fortalezas y las debilidades que tenemos y aprender a pedir ayuda cuando lo necesitemos. “No soy mejor, no soy peor, simplemente soy yo”.
Regálate tiempo . Haz actividades que te gusten para conocerte mejor, podrás averiguar cuáles son tus habilidades, desarrollarlas y sentirte bien contigo mismo. También es importante dedicar un poco de tiempo a salir y simplemente divertirse llanamente. “Apúntate a ese taller de manualidades que siempre has querido y desarrolla tu habilidad para crear”
Cuida a las personas de tu entorno. Cuando una persona es empática con los demás y trata acorde a ello, recibe valoraciones acompañadas de adjetivos como amable, servicial, atento, educado, cercano, etc. Todos ellos recaen directamente sobre la autoestima porque nuestro autoconcepto depende en gran medida de cómo nos ven los demás. “Cuidar hacia fuera es cuidar hacia dentro”.

Artículo especializado
Cómo Identificar y Prevenir la Astenia Infantil
La astenia es un síntoma que se asoma con frecuencia a las consultas del pediatra de atención primaria. Es muy frecuente en adolescentes, pero también en niños. La astenia es fatiga o cansancio no justificado por un esfuerzo físico o mental. Es un síntoma, no una enfermedad en sí misma.
¿Qué es la astenia?
Se define astenia como la sensación de falta de energía o motivación para realizar nuestras actividades diarias. Serían sinónimos: cansancio, fatiga o agotamiento. No hay que confundir astenia con somnolencia y apatía, aunque éstas pueden acompañar al niño asténico.
El cansancio aparece de forma fisiológica tras un esfuerzo físico o mental y se recupera durmiendo y bajando el nivel de actividad.
La astenia es un cansancio inusual y extremo que disminuye el rendimiento físico e intelectual y requiere un excesivo reposo. Puede acompañarse de otros síntomas en los niños o adolescentes, como irritabilidad, falta de motivación, bajo rendimiento escolar o somnolencia.
Causas de astenia
La sensación de cansancio puede ser debida a una gran variedad de causas, por lo que no debemos subestimar al niño o adolescente que se queja de que está fatigado permanentemente sin una causa que lo justifique. En muchas ocasiones, son causas banales pero, en otras, podemos encontrarnos con diagnósticos importantes.
De hecho, las causas más frecuentes de astenia son: la actividad excesiva, el estrés o la sobrecarga de trabajo y el desorden del sueño (típico en los adolescentes que duermen poco por realizar otro tipo de actividades en la noche).
Cuando un niño se queja de cansancio debemos analizar su estilo de vida, realizar una exhaustiva exploración física y emocional , rendimiento escolar, sobrecarga de extraescolares y solicitar alguna prueba complementaria, como una analítica de sangre o una prueba de imagen de los pulmones y/o el abdomen.
Las enfermedades que pueden manifestarse con astenia pueden ser:
Infecciones (como la mononucleosis infecciosa o la tuberculosis).
Anemia.
Depresión.
Enfermedad cardíaca.
Hipotiroidismo.
Trastornos del sueño.
Diabetes.
Enfermedades reumatológicas (como lupus o artritis reumatoide).
Trastornos inmunológicos.
Hepatitis.
Enfermedades renales.
Cáncer.
Embarazo (no es una enfermedad, pero hay que descartar su diagnóstico en adolescentes).
Si hablamos de astenia y niños no podemos olvidar dos entidades: la astenia primaveral y el síndrome de fatiga crónica.
Astenia primaveral
Sentir más cansancio en primavera también es cosa de niños. Esta sensación se relaciona con el cambio horario, el aumento de la temperatura (llega el calor) y los cambios en la luz diurna.
Los síntomas más frecuentes de la astenia primaveral en niños son:
Falta de energía y sensación de cansancio.
Cambios de humor, como tristeza, sin motivo aparente.
Irritabilidad.
Pérdida de apetito.
Problemas de sueño.
Este trastorno no suele durar más de dos semanas y, aunque no hay un tratamiento específico, podemos mejorar la adaptación de los niños a la nueva estación con estas sencillas pautas:
Exponerse al sol: el sol y su luz en fundamental para regular los ritmos circadianos (o día y noche de nuestro cuerpo). Que el niño disfrute del sol y que se despierte con su luz le puede ayudar a mejorar o aliviar la astenia primaveral y los problemas de sueño asociados.
Ejercicio físico: la actividad física es clave para nuestro bienestar físico y emocional. Aunque la astenia primaveral provoque cansancio, la práctica de ejercicio diario, moderado, de unos 30 minutos, es muy beneficioso.
Dormir suficiente: los niños deben dormir unas 10 horas al día. Respetar esas horas de sueño es fundamental para superar la astenia primaveral.
Hidratarse bien: tomar líquidos suficientes, sobre todo agua, parece que ayuda a mantenerse mejor en primavera, cuando las temperaturas ya empiezan a subir.
Alimentación equilibrada: el cansancio puede aliviarse comiendo. Por eso ofrece cinco comidas al día con tentempiés saludables como frutos secos, fruta y alimentos integrales. Evita los azúcares y las grasas saturadas.
Tomar omega 3: ofrece alimentos ricos en omega 3 como el salmón.
Síndrome de fatiga crónica
Es muy poco frecuente en niños y muy difícil de diagnosticar. Es un síndrome que engloba componentes físicos y psicológicos . Los síntomas son muy variados y pueden ir desde el dolor articular, la cefalea, el cansancio y la desmotivación.
La causa todavía no se sabe con certeza, pero se apunta a posibles desencadenantes:
Infecciones: parece que virus como el Epstein-Barr (mononucleosis infecciosa) pueden incrementar el riesgo de padecer síndrome de fatiga crónica.
Problemas del sistema inmune.
Estrés.
Hipotensión o tensión arterial baja.
Antecedentes familiares.
Se sospecha fatiga crónica si la sensación de cansancio es inexplicable por otras causas y dura seis meses o más. Y, además, se asocian problemas de concentración, cefalea, dolores articulares o musculares, ganglios inflamados y tener un sueño no reparador.
Todavía no sabemos la cura para este síndrome, pero se recomienda un cambio hacia hábitos más saludables como ejercicio regular, descanso adecuado y dieta equilibrada. Las técnicas de manejo del estrés o acudir a un psicólogo o terapeuta son herramientas que pueden ser muy útiles. En algunos casos se pueden prescribir fármacos antidepresivos.

Artículo especializado
Qué Debes Saber sobre los Juanetes
¿Sabías que el primer dedo del pie se llama Hallux? De ahí el nombre de Hallux Valgus . Lo primero que tenemos que saber es que ese nombre hace referencia a los conocidos juanetes, también llamados bunios. Se trata de una deformidad que afecta al primer metatarsiano del pie y al primer dedo junto a la articulación que los une . A pesar de ser muy frecuente en adultos también puede aparecer en niños en cuyo caso recibe el nombre de Hallux Valgus congénito (aparece antes de los 15 años).
¿En qué consiste?
Esta deformidad afecta al primer dedo del pie que está desviado y orientado hacia la cara externa mientras que el primer metatarsiano estará desviado y orientado hacia el borde interno del pie. Esto provoca una incongruencia articular y una afectación de toda la articulación entre el metatarsiano y la primera falange del primer dedo, por lo que se verá afectada tanto estética como funcionalmente (pues el acto de caminar se verá alterado).
Una enfermedad multicausal
Al tratar de buscar posibles causas asociadas concluimos que se trata de una deformidad de origen multicausal. Vamos a citar algunos factores asociados a su alta prevalencia :
Genética y herencia : numerosos estudios confirman la existencia de predisposición familiar entre padres e hijos. Se cree que no se hereda la deformidad, sino la funcionalidad del pie.
Calzado : es el factor más estrechamente relacionado con la aparición de esta deformidad. Los zapatos que más la favorecen son los apretados y en forma de punta, así como los de tacón. Como curiosidad, en personas que suelen caminar descalzas, es menos frecuente la aparición de juanetes.
Influencia hormonal y biotipo : podríamos considerar diferentes aspectos que favorecen una mayor incidencia en mujeres: la forma del pie (más estrecha), la laxitud ligamentosa (más común en mujeres), la disminución de niveles de relaxina en la menopausia ( hormona que confiere laxitud a los ligamentos), etc.
Alteración en el apoyo podal: los pacientes que presentan un apoyo podal alterado y son portadores de plantillas u ortesis son candidatos a tener otras deformidades asociadas.
¿Qué síntomas presentará la persona afecta de Hallux Valgus?
Los motivos de consulta más frecuentes serán el dolor y la deformidad . El dolor estará localizado específicamente en la primera articulación metatarsofalángica, que puede irradiarse a la planta del pie por una alteración del apoyo durante la marcha.
La mejor manera de explorar esta deformidad es con el paciente de pie (en bipedestación) dado que en situación de carga se acentúa, mientras que se reduce al no apoyar. También analizaremos las posibles deformidades asociadas en los dedos contiguos, el arco plantar y la orientación y el apoyo del talón.
Conforme se hace más marcada la deformidad aparecerán otros síntomas locales que dificultarán la marcha, así como el uso de su calzado habitual, formándose de esta manera un círculo vicioso: se tenderá al uso de zapatillas de suela blanda que empeorará el apoyo podal y aumentará la deformidad y el dolor.
¿Cómo llegamos al diagnóstico de Hallux Valgus?
El diagnóstico comienza con una exhaustiva exploración clínica, y se corrobora con unas radiografías del pie en diferentes proyecciones que evidenciarán las conocidas deformidades.
Estableceremos el grado de afectación . Para ello disponemos de diferentes clasificaciones, como puede ser la Escala de Mánchester:
Grado 1: no deformidad
Grado 2: deformidad leve
Grado 3: deformidad moderada
Grado 4: deformidad severa
¿Cuál será el tratamiento más indicado?
Existen dos alternativas terapéuticas : el tratamiento conservador y el tratamiento quirúrgico .
El tratamiento conservador se propone en los estadios iniciales. El traumatólogo y el podólogo son los profesionales implicados más estrechamente en las enfermedades de los pies. En general, se opta inicialmente por un tratamiento conservador, salvo que el paciente presente un grado 4 o deformidad severa en cuyo caso se propone tratamiento quirúrgico directamente.
Es primordial que una persona con Hallux Valgus use plantillas para corregir el apoyo podal.
Existen otros tratamientos como los separadores nocturnos (corrigen la posición del primer dedo durante el sueño), las ortesis de silicona (que funcionan como un separador interdigital) y las llamadas juaneteras (protegen de la fricción con el calzado).
Recomendaremos evitar tacones altos y calzado acabado en punta.
Cuando el tratamiento conservador es insuficiente para controlar los síntomas se optará por el siguiente eslabón terapéutico: la cirugía . Se recomendará en función del dolor, el grado de afectación, la edad, la actividad del paciente y las manifestaciones clínicas para el paciente. No estaría indicado intervenir un Hallux Valgus por motivos únicamente estéticos.
Las técnicas quirúrgicas para la cirugía del Hallux Valgus en la actualidad son menos agresivas.
El tratamiento estrella es la osteotomías o sección ósea del primer metatarsiano, pero existen muchas otras opciones destinadas a corregir la desviación del primer dedo y alinear el primer metatarsiano. Los resultados son buenos pero el postoperatorio pde ser doloroso.
¿Y QUÉ ES EL HALLUX VARUS?
Para finalizar te quería mencionar otra deformidad que afecta al dedo gordo del pie, pero mucho menos frecuente : el Hallux Varus. Como su nombre indica es la deformidad antagonista al juanete y se caracteriza por la desviación de dedo gordo del pie hacia la parte interna del mismo.
La mayoría de estas deformidades tiene indicación quirúrgica tras años de evolución , pero muchas de ellas mejoran con tratamiento ortopédico. No dudes en acudir al podólogo si observas un desgaste irregular en la suela de tus zapatos o tienes tendencia a desviar el pie durante la marcha.

Artículo especializado
Balón Gástrico: Tratamiento, Beneficios y Contraindicaciones
Ante la epidemia del sobrepeso y la obesidad ( un 53% de la población adulta esté por encima de su peso ), las sociedades científicas han centrado sus esfuerzos en investigar diferentes métodos para el tratamiento de la pérdida de peso más allá de la intervención dietética, farmacológica o de cambios conductuales. Entre ellos, destacamos los procedimientos endoscópicos cuyo método más común es la inserción del balón intragástrico.
Entre los métodos para para el tratamiento de la obesidad debemos distinguir dos procedimientos, según la técnica utilizada:
Procedimientos quirúrgicos (cirugía bariárica)
Técnicas restrictivas (contribuyen a disminuir la ingesta de alimentos): gastroplastia, banda gástrica, manga gástrica, gastrectomía vertical.
Técnicas malabsortivas (contribuyen a disminuir la absorción de los alimentos): by-pass yeyunoileal.
Técnicas mixtas (contribuyen a disminuir tanto la ingesta como la absorción de alimentos): By-pass gástrico en Y de Roux, derivaciones biliopancreáticas.
Procedimientos endoscópicos
Balón o globo intragástrico (actúa produciendo ocupación o restricción de espacio en el estómago).
Balón ingerible, con los que no es necesario realizar una endoscopia (se introducen mediante una cápsula unida a un hilo que se hincha al llegar al estómago).
POSE (Primary Obesity Surgery Endolumenal): técnica endoscópica sin incisiones que reduce la capacidad volumétrica gástrica mediante la colocación de puntos de sutura. A diferencia del balón intragástrico, esta técnica está más indicada en casos de obesidad grave y se obtienen mejores resultados a largo plazo.
En este artículo nos centraremos en analizar los pros y contras de la implantación del balón intragástrico, así como la correcta elección de los beneficiarios de esta técnica.
¿Quién puede ser candidato al balón intragástrico?
Antes de elegir esta opción terapéutica para la pérdida de peso, hay que tener en cuenta los siguientes criterios de elección de los pacientes que son aptos:
Personas con obesidad (IMC entre 30 y 40) sin comorbilidades (más de una enfermedad al mismo tiempo) ni enfermedades metabólicas y que ya hayan intentado perder peso mediante otros tratamientos (dietético o farmacológico) sin éxito.
Personas con IMC a partir de 35 con comorbilidades que requieran esta técnica como paso puente a una cirugía bariátrica (reduciendo así el riesgo quirúrgico) o para mejorar sus enfermedades metabólicas asociadas.
Personas con obesidad cuya intervención quirúrgica está contraindicada por sus posibles complicaciones o cuando el paciente se niega a someterse a cirugía
Por el contrario, la implementación del balón intragástrico es un procedimiento contraindicado en los siguientes casos:
Personas que tienen un IMC superior a 40 (obesidad mórbida) o superior a 35 y que además presentan comorbilidades: en estos casos se requiere una cirugía bariátrica.
Personas con trastornos psicológicos y cognitivos graves .
Personas drogodependientes.
Personas que padecen enfermedades crónicas y graves (hepática, renal, cardiaca o pulmonar) o que hayan sido sometidas a otras cirugías por padecer reflujo gastroesofágico, hernia de hiato o úlcera duodenal y gástrica.
Procedimiento de colocación del balón intragástrico
En primer lugar, hay que tener en cuenta que esta intervención se realiza bajo anestesia general, tiene una duración de 20-30 minutos , no requiere de hospitalización y sólo puede ser realizada por un médico especialista en Endoscopia Digestiva.
En cuanto al proceso de intervención, primero se introduce un balón doblado de silicona resistente, pero flexible mediante endoscopia (de la boca hasta el estómago). Una vez en el estómago, se llena con 450-650 cc de suero fisiológico (ocupando entre el 40 y el 50% del volumen gástrico) y permanece flotando en el estómago por un periodo no superior a seis meses durante el cual se producirá una sensación de saciedad precoz tras la ingesta de alimentos.
Por último, una vez transcurridos los seis meses (o hasta un año en algunos tipos concretos de balones), se procede a la extracción del balón con una aguja de punción y un fórceps , retirándolo del estómago por endoscopia.
Beneficios y expectativas del balón intragástrico
Una de las ventajas de las técnicas endoscópicas (balón intragástrico) frente a la cirugía bariátrica es la disminución de riesgos y complicaciones , ya que se respeta por completo la anatomía gastrointestinal sin producir modificaciones irreversibles. Además, se trata de una técnica con una óptima eficacia sólo a corto plazo: se puede perder hasta un kilo por semana según la situación de cada paciente, aunque esta pérdida se puede revertir (es muy frecuente recuperar el peso perdido a largo plazo) si el paciente no realiza una correcta educación nutricional durante los meses que lleva el balón.
Complicaciones del balón gástrico
Las complicaciones de esta técnica son mínimas y, en caso de haberlas, se dan lugar durante el proceso de implantación y retirada del balón:
En la implantación, pueden darse complicaciones en la endoscopia, entre ellas: irritación de la mucosa estomacal o gastritis , úlceras o perforaciones.
En la retirada, también se pueden dar acumulaciones de fibra alrededor del balón, hecho que dificulta su extracción.
Además, hay que tener en cuenta que pueden aparecer ciertos efectos secundarios de carácter transitorio, sobre todo en las primeras 48-72 horas tras la colocación del balón: náuseas, vómitos, sensación de plenitud y dolor epigástrico.
La importancia de la reeducación alimentaria post-intervención
Tal y como hemos comentado, la implantación del balón intragástrico debe ser un “impulsor” para producir una pérdida de peso a corto plazo ya que son múltiples los estudios que concluyen que esta técnica no implica una mayor pérdida de peso a largo plazo en comparación con un tratamiento convencional para la obesidad (dieta y ejercicio).
Por eso, debido a su carácter temporal, el uso del balón intragástrico debe ir acompañado siempre de un cambio de hábitos de forma definitiva, para poder mantener la pérdida de peso conseguida una vez retirado el balón
En resumen, el éxito de esta intervención radica en la motivación del paciente para realizar cambios permanentes en sus hábitos de alimentación y ejercicio durante y después de la implementación del balón gástrico.

Artículo especializado
Qué Debes Saber Sobre la Fiebre
Mucha gente utiliza el término fiebre de manera inespecífica para expresar que se sienten demasiado calientes, demasiado fríos, sudorosos, con escalofríos, pero en realidad no han medido su temperatura. De manera correcta, decimos que una persona tiene fiebre cuando su temperatura axilar es superior a 38ºC , cuando su temperatura rectal es mayor a 38,5ºC o su temperatura oral es superior a 38,2ºC. Entre 37 y 37,5ºC hablaremos de febrícula.
Valores y formas de tomar la fiebre
La fiebre es una temperatura corporal elevada . No es una enfermedad sino el signo de una enfermedad. Existen discrepancias tanto en el valor de temperatura que se considera fiebre como en la forma de tomarla.
La medida de la fiebre con otros termómetros distintos al axilar-digital no muestran fiabilidad.
En la actualidad, los termómetros de mercurio están fuera de uso y se recomienda su retirada o reciclaje debido a la alta toxicidad del mercurio en caso de rotura.
El termómetro digital es rápido, irrompible y cómodo. Se recomienda retirar la pila después de su uso para evitar su descarga.
El termómetro ótico, que funciona por infrarrojos, es impreciso y caro, al igual que el termómetro cutáneo, ya que da valores inadecuados pues en las primeras fases de la respuesta febril se produce un descenso de la perfusión cutánea lo que altera su temperatura.
Temperatura
Eficacia
Valores Normales (ºC)
Rango de
Temperatura (ºC)
Axilar
Sí
37,0
34,7 – 37,3
De Elección
Rectal
No
38,0
36,6 – 38,0
Oral
No
37,5
35,8 – 38,0
Timpánica
No
37,5
35,8 – 38,0
Aunque se considera normal una temperatura de 37ºC, nuestra temperatura corporal varia durante el día, siento más baja por la mañana y más alta a última hora de la tarde cuando puede alcanzar los 37,7ºC. Cuando tenemos fiebre, la temperatura tampoco se mantiene constante. Puede haber picos de fiebre que se normalizan durante el día, lo que se denomina fiebre intermitente. En otros casos la temperatura varía, pero no vuelve a la normalidad; es lo que se conoce como fiebre remitente.
El curso de la fiebre puede indicar el tipo de enfermedad : infecciosa, oncológica, multiorgánica, politraumática…
¿Qué puede causar fiebre?
Dos son las causas principales que provocan fiebre:
Causas no infecciosas : son la producidas por aquellas reacciones del organismo diferentes a enfermedades bacterianas o víricas.
Reacciones a vacunas.
Reacciones a un fármaco.
Enfermedades reumatológicas
Causas metabólicas como la deshidratación o fiebre de sed.
Neoplasias.
Enfermedades autoinmunes: enfermedad del suero, vasculitis.
Causas infecciosas :
Víricas.
Respiratorias.
Gastrointestinales.
Enfermedades exantemáticas (varicela).
Bacterianas.
Infecciones de garganta, nariz u oído.
Infecciones respiratorias como la bronquitis, neumonías.
Infecciones del tracto génito-urinario: infecciones de orina, prostatitis aguda, enfermedades de transmisión sexual.
Infecciones del sistema nervioso central: meningitis, encefalitis, abscesos cerebrales.
Infecciones generalizadas del organismo: sepsis y bacteriemia oculta.
Tipos de fiebre
Fiebre de inicio reciente: de pocas horas de evolución, no suele encontrarse una causa evidente. En general, no es necesario acudir al médico exceptuando aquellos pacientes con gran afectación del estado general.
Fiebre de corta duración o de menos d cinco días : fiebre con foco (después de una historia clínica y exploración) o fiebre sin foco, donde desconocemos su causa. El paciente debe acudir al médico a partir del tercer día de su inicio o enseguida en pacientes con enfermedades crónicas o gran afectación del estado general.
Fiebre prolongada o FOD : es aquella que dura de siete a 10 días, sin encontrar la causa con las medidas diagnósticas habituales.
Signos de alarma
En ocasiones hay síntomas y signos clínicos por los que deberemos acudir de inmediato a urgencias :
Confusión o delirio mental.
Dolor de cabeza, rigidez de cuello o ambos. Debemos de ser capaces de flexionar la cabeza hacia delante en posición de decúbito prono.
Manchas planas redondeadas pequeñas de color rojo púrpura en la piel (petequias): cuando presionamos con un vaso o yema del dedo éstas no desaparecen.
Hipotensión arterial.
Frecuencia cardiaca rápida o respiración acelerada.
Dificultad respiratoria.
Temperatura superior a 40ºC o inferior a 35ºC.
Viaje reciente del paciente a áreas donde hay enfermedades infeccionas graves como malaria o dengue.
Tratamientos con fármacos quimioterápicos recientes o inmunosupresores.
¿Y LOS BEBÉS?
En caso de bebés menores de tres meses consultaremos de inmediato a partir de 37,5-38ºC . Recordemos que los bebés, al igual que los ancianos mayores de 80 años, suelen tener alteraciones a nivel del centro regulador de la temperatura corporal o hipotálamo del sistema nervioso central.
El médico de familia, pediatra en caso de niños o el médico de urgencias en caso de existir signos de alarma, serán los especialistas que detecten en un primer momento la fiebre, realicen un primer diagnóstico y pauten un tratamiento adecuado para su curación.
Tratamiento para bajar la fiebre
Los fármacos utilizados para bajar la temperatura del cuerpo son los antitérmicos o antipiréticos. La pauta del tratamiento como siempre la prescribirá nuestro médico. Los principales son:
Paracetamol (acetaminofeno por vía oral, rectal o endovenosa).
Fármacos antiinflamatorios no esteroideos (AINES). Se administran por vía oral o endovenosa (Ibuprofeno, Naproxeno).
Aspirina (Ácido Acetil Salicílico) sólo para casos seleccionado.
Metamizol (Nolotil).
En cuanto a las principales medidas físicas a adoptar , estas son:
Retirar la ropa en exceso.
Mantener el ambiente a temperatura 20-22ºC, con una buena ventilación.
Colocar toallas con agua tibia por todo el cuerpo cambiándolas frecuentemente.
Bañarse con agua templada.
No usar jamás paños de alcohol ya que pueden provocar intoxicación etílica.
Beber abundante líquido (zumos azucarados y agua). Recordar siempre que nuestro cuerpo pierde también líquidos por transpiración.
Mantener al enfermo en reposo en el domicilio siempre que tenga fiebre y de manera óptima un día más al término de ésta, como mínimo.

Artículo especializado
Recuperación y Tratamiento de un Esguince
En el mundo del deporte los esguinces se encuentran entre las lesiones más habituales y su localización más frecuente es el tobillo y la rodilla. Los deportes que suelen aparecer en las primeras posiciones de las listas en las que las lesiones ligamentosas de tipo agudo son frecuentes, suelen ser aquellos en los que existe contacto como futbol, baloncesto o rugby. Te explicamos cómo se trata un esguince y en qué consiste la recuperación.
Por qué se produce
Nuestras articulaciones están formadas por diferentes elementos y cada uno de ellos tiene su función concreta , pero ofrecer estabilidad y permitir el movimiento suelen ser funciones comunes a todos ellos. Entre los elementos de una articulación encontramos los ligamentos , que son bandas de tejido conectivo que unen los huesos entre sí, a diferencia de los tendones que unen músculo a hueso.
Estas bandas tienen características que, hasta cierto punto, pueden resultar contradictorias entre sí. Deben ofrecer estabilidad, pero a su vez un cierto grado de flexibilidad para permitir adaptarse a los movimientos sin una extrema rigidez articular. En ocasiones esta flexibilidad no es suficiente y es cuando puede lesionarse, sufriendo un esguince. En general ocurre cuando la articulación pierde el eje, como por ejemplo en una entorsis (torcedura).
En función de la gravedad de la lesión se clasificará en grado I, grado II o grado III.
El esguince de grado I corresponde al más leve. De inicio hay dolor leve, pero éste desaparece en un periodo corto de tiempo. Apenas hay inflamación y no se produce rotura del ligamento.
El esguince de grado II presenta una rotura de la banda, pero ésta es parcial. Se acompaña de edema (hinchazón) y de hematoma. El dolor es más agudo y se acompaña de inestabilidad articular.
El esguince de grado III equivale a una rotura completa del ligamento. El edema y el dolor son importantes y hay una imposibilidad de apoyo estable.
Tratamiento inicial
En general el tratamiento inicial seguirá el método RICE , que se denomina así por sus siglas en inglés: R (Rest -reposo-), I (Ice -hielo-), C (Compression -Compresión-), E (Elevation -Elevación-), para minimizar la sintomatología desde el primer momento tras la lesión. Por su parte, la administración de fármacos antiinflamatorios y analgésicos ayudará a mejorar la calidad de vida del paciente, reduciendo las molestias y el dolor.
El reposo no tiene por qué ser absoluto, ya que dependerá del grado de la lesión, así como de la actividad que desarrolle la persona en su día a día.
La crioterapia (hielo) tiene función antiinflamatoria, produce una vasoconstricción que reduce el edema, así como una disminución de la temperatura de la zona afectada. Se recomienda colocar hielo varias veces a lo largo del día en el área lesionada en sesiones de unos 15 segundos, sobre todo en las primeras 24-48 horas tras el esguince.
El vendaje compresivo actúa a dos niveles: provoca inmovilización de la articulación y actúa sobre el edema. Se realiza con material que proporciona estabilidad pero que no es completamente rígido, como podría ser un yeso. Se trata de un vendaje funcional.
Al elevar la articulación , algo que es posible sobre todo cuando el esguince afecta a las extremidades inferiores, se favorece el retorno venoso y, por tanto, se actúa sobre la inflamación.
Seguimiento de la lesión
Además del tratamiento inicial habrá que hacer seguimiento para valorar la evolución de la lesión, e ir incorporando la rehabilitación para conseguir la recuperación de la funcionalidad de la articulación afectada en un periodo de tiempo adecuado.
La rehabilitación es esencial para conseguir recuperar la movilidad adecuada, más aún en los casos en que el paciente es un deportista y requiere de un gesto deportivo determinado para practicar su deporte al nivel previo a la lesión.
Apenas el dolor lo permita, y dependiendo de la afectación ligamentosa, se recomienda empezar a hacer apoyos para que los tejidos no lesionados mantengan cierta funcionalidad y los lesionados empiecen a recuperarse. No hay que olvidar que en función de la región afectada se puede seguir entrenado. Si la lesión se circunscribe a las extremidades superiores se puede, y se debe, seguir entrenando el resto del cuerpo y lo mismo pasa si son las extremidades inferiores las que han resultado afectadas.
De manera progresiva, se van incorporando al programa de rehabilitación ejercicios para recuperar la movilidad , así como de fortalecimiento de los ligamentos. Las bandas fibrosas que han perdido su continuidad deben recuperarse y es necesario un trabajo específico. Efectuar movimientos articulares concretos, tanto asistidos por el profesional como realizados por el propio paciente, es una práctica habitual, pues de forma gradual se amplía la capacidad de esa articulación para realizar gestos propios y la amplitud de movimiento.
Por ejemplo, en el caso del tobillo los ejercicios de propiocepción (de equilibrio y estabilidad) son muy habituales, su objetivo es fortalecer músculos y ligamentos además de trabajar el equilibrio usando superficies inestables. El paciente “reaprende” a controlar su estabilidad recuperando la articulación que ha quedado inestable tras la lesión y para ello es necesario recuperar no sólo las estructuras más físicas sino también la parte más funcional.
Incorporar terapias manuales como el masaje “cyriax”, una técnica de fricción profunda, o el uso de métodos de recuperación tisular acelerará la evolución. En este último caso estas técnicas actúan por longitud de ondas favoreciendo, entre otros, el aporte de oxígeno y de nutrientes a los tejidos que promueven la regeneración.
Conocer el estado previo
Es importante además de una correcta recuperación y tratamiento conocer si exista algún déficit que ha podido aumentar el riesgo de lesión . Poseer una musculatura y articulaciones débiles y poco estables va a favorecer la aparición de estas lesiones por lo que es esencial incorporar al programa de rehabilitación no sólo ejercicios enfocados a mejorar los tejidos afectados sino también ejercicios de prevención cuyo objetivo será fortalecer aquellas estructuras adyacentes que intervienen en el movimiento para reducir el riesgo a posteriori.

Artículo especializado
Apnea del Sueño en Bebés y Niños
Parece un concepto asociado al adulto, pero lo cierto es que algunos niños y bebés padecen apneas durante el sueño. Y es que el síndrome de las apneas-hipopneas del sueño (SAHS) en los niños es una enfermedad poco conocida por los padres e, incluso, también por los pediatras que los atienden. Estos con frecuencia no reconocen la patología, por lo que está muy infradiagnosticada e infratratada en los menores de nuestro país.
¿Qué es?
El SAHS es un trastorno respiratorio durante el sueño caracterizado por una obstrucción parcial prolongada de la vía aérea superior y/o obstrucción intermitente completa, que interrumpe la ventilación normal durante el sueño y los patrones normales del mismo. Se estima que afecta a un 2-3% de los niños , con una prevalencia similar en niños y niñas y en todas las edades (incluso en bebés), aunque quizás es más frecuente en la edad preescolar, coincidiendo con el momento en que el tejido linfoide (de defensa) que rodea la vía aérea alta (denominado anillo de Waldeyer) es mayor en relación al tamaño de la vía aérea.
Causas
La faringe es colapsable para permitir la fonación y la deglución . Las funciones de la faringe como son deglutir, proteger la vía aérea y mantenerla abierta, se logran por la acción de varios grupos musculares que actúan de forma coordinada. El sueño es el factor funcional más evidente que predispone al SAHS. Durante su fase REM se produce una reducción tan marcada de la actividad de los músculos que mantienen abierta la vía aérea, que el SAHS pediátrico podría considerarse una enfermedad de la fase REM del sueño.
Los factores predisponentes del SAHS en el niño son:
Hipertrofia de amígdalas y adenoides (vegetaciones). Es la causa más frecuente.
Malformaciones congénitas craneofaciales: Síndrome de Down, Síndrome de Pierre Robin, Síndrome de Treacher Collins, Síndrome de Klippel-Feil, Síndrome de Prader Willi, acondroplasia, retrognatia (barbilla pequeña y retraída), alteraciones anatómicas del paladar, etc.
Obstrucción nasal marcada (rinitis alérgica).
Laringomalacia (laringe débil, poco consistente, fácilmente colapsable).
Enfermedades neurológicas y neuromusculares.
Reflujo gastroesofágico (RGE).
Obesidad.
Miembros familiares con SAHS o hábito tabáquico familiar (especialmente la madre).
Signos y síntomas
El síntoma guía es el ronquido . Su ausencia prácticamente descarta la existencia de un SAHS, pero su presencia no indica necesariamente la existencia del mismo.
Hablamos de “ronquido primario” o “ronquido simple” cuando éste no se acompaña de alteraciones del sueño (apneas-hipopneas, desaturaciones, hipercapnia -aumento de CO2 sanguíneo- o fragmentación del sueño).
Tipos de apnea
Desaturación: caída del valor de oxigenación en la máquina de pulsioximetría (digital) mayor o igual a un 4%.
Apnea obstructiva: cese del flujo aéreo en nariz y boca durante más de dos ciclos respiratorios mientras se mantienen los movimientos tóraco-abdominales.
Apnea central (origen en el Sistema Nervioso Central): cese del flujo aéreo y los movimientos tóraco-abdominales durante más de dos ciclos respiratorios. Son frecuentes en los niños y sólo se consideran problemáticas si duran más de 20 segundos o se acompañan de desaturaciones.
Hipopnea: reducción del flujo aéreo mayor del 50% que se acompaña de una caída de la saturación de oxígeno mayor o igual a un 4% y/o con un microdespertar.
Además del ronquido, en el SAHS se aprecian apneas o pausas respiratorias precedidas por un aumento del esfuerzo respiratorio (incluso movimientos paradójicos de la caja torácica), provocándose con ello movimientos del paciente, o un despertar, un sueño intranquilo no reparador o adquisición de posturas anormales para dormir (cabeza colgando fuera de la cama) para poder mantener abierta la vía aérea. El mayor esfuerzo respiratorio conlleva un aumento del gasto energético que se ha asociado a una sudoración profusa , muy frecuente en estos niños. También son posibles, por presencia de RGE, náuseas o vómitos durante el sueño y, ocasionalmente, también despertares con ansiedad y sensación de dificultad respiratoria (disnea), pesadillas, terrores nocturnos, sonambulismo o bruxismo (acto de frotar los dientes). Otro síntoma posible es la enuresis (no control de la contención de orina en edades en las que ya se produce habitualmente).
Los síntomas diurnos más frecuentes son los propios de la obstrucción de la vía aérea superior secundaria a la hipertrofia adeno-amigdalar o la rinitis como la respiración bucal y ruidosa durante el día, que se agrava durante las habituales infecciones respiratorias de vía alta, cefaleas (dolor de cabeza) o, incluso, alteraciones del carácter con agresividad, labilidad emocional (llanto fácil) o hiperactividad, así como práctica de conductas antisociales. No suelen presentar somnolencia diurna.
Consecuencias
Las consecuencias del SAHS en el niño pueden ir desde una disminución del rendimiento escolar hasta complicaciones más serias como la hipertensión arterial, insuficiencia cardiaca, retraso del desarrollo psicomotor o de crecimiento, así como depresión.
Diagnóstico
La polisomnografía convencional es la prueba que registra simultáneamente, y de manera continua, las variables neurofisiológicas (mediante el registro de un electroencefalograma) y cardiorespratorias durante el sueño. Las primeras son necesarias para conocer si el niño está durmiendo en un momento determinado y en qué fase concreta del sueño está, así como para conocer la arquitectura del sueño y determinar la existencia de microdespertares electroencefalográficos. Las segundas se basan en la detección de valores de tipo frecuencia y ritmo cardiaco, la pulsioximetría (oxigenación) o detección de movimientos respiratorios…
El sueño del niño debe ser espontáneo, es decir, no inducido farmacológicamente.
Tratamiento
Las complicaciones importantes en los niños que lo padecen pueden evitarse con un abordaje terapéutico adecuado, que deberá ser multidisciplinar, es decir, con la intervención de diversos especialistas (pediatras, neumólogos, otorrinos…).
El tratamiento, en la gran mayoría de niños, dado que la causa más frecuente es la hipertrofia adenoamigdalar, será la adenoamigdalectomía (intervención quirúrgica para extirpar ambas glándulas): ha demostrado resolver los trastornos respiratorios y los síntomas nocturnos en el 75-100% de los niños sin otra enfermedad de base.
La segunda línea de tratamiento será el empleo del CPAP (presión positiva continua sobre la vía aérea, mediante el uso de un compresor y una mascarilla), si la adenoamigdalectomía fracasa o está contraindicada. La cantidad de presión del CPAP se debe individualizar y su objetivo será conseguir la presión óptima para mantenerla abierta durante todo el ciclo respiratorio (evitando su colapso) de manera que elimine las apneas y minimice el ronquido, y resulte a la vez tolerable para el niño.
Otros niveles de tratamiento incluyen: educación sanitaria acerca de hábitos saludables de sueño, el tratamiento de la congestión nasal, el uso de oxigenoterapia nocturna o el tratamiento antiácido contra el reflujo gastroesofágico, entre otros.
Pronóstico
Los niños con ronquido primario no tienden a progresar a SAHS con el tiempo.
Los niños que padecen esta patología tienen mayor probabilidad de recaer cuando son adultos si adquieren factores de riesgo como la obesidad o la ingestión de alcohol .
No se conoce la historia natural ni el pronóstico a largo plazo del SAHS pediátrico no tratado.
Artículo especializado
Artroscopia: Qué Debes Saber
¿Conoces a alguien que haya pasado por una artroscopia? ¿Es tu caso? ¿Sabías que actualmente se operan más rodillas por artroscopia que por cirugía abierta? Esta técnica quirúrgica, que nació en Japón , actualmente es utilizada a nivel mundial. Te facilitamos una pincelada de este procedimiento.
La artroscopia es una modalidad quirúrgica en la que se visualiza el interior de una articulación con una cámara con el fin de detectar lesiones (o comprobar lesiones detectadas en pruebas diagnósticas previas) y su reparación definitiva. Por tanto, su finalidad puede ser diagnóstica o terapéutica-reparadora.
No sólo se realiza en grandes articulaciones como rodilla, cadera y hombro . En la actualidad y, gracias a los avances tecnológicos, pueden visualizarse pequeñas articulaciones como son el tobillo y la muñeca. Se consiguen imágenes de alta definición en 3D que permiten valorar la estructura anatómica con todo lujo de detalles. Incluso es posible la captura de imágenes y su impresión posterior para mostrarle al paciente las lesiones detectadas y el procedimiento realizado.
¿Cómo se realiza?
El instrumental específico que se emplea recibe el nombre de artroscopio . Puede ser equipado con distintas herramientas accesorias, para realizar los tratamientos oportunos. El artroscopio es un tubo fino de fibra óptica (formado por un sistema de lentes, cámara de video y luz). La cámara del artroscopio está conectada a un monitor que permite visualizar en pantalla la información captada durante la intervención en tiempo real.
¿Por dónde entra el artroscopio? Se introduce en la zona a explorar por una pequeña incisión que el cirujano realiza en la piel llamada portal (sería la puerta de entrada del instrumental). Puede ser precisa la apertura de otros portales por donde se introducen los instrumentos especiales para realizar el tratamiento (aspirador, pinzas, tijeras, bisturí, fresas, material de sutura…). Normalmente son suficientes tres portales de entrada en el acto quirúrgico.
Si la finalidad de la artroscopia es sólo diagnóstica el artroscopio únicamente estará equipado con la cámara básica, que entra por un portal. Si la finalidad es la reparadora necesitaremos instrumental, aspiración e iluminación (que entrará por los otros dos portales).
¿Para qué?
El uso de la artroscopia está delimitado a cirugías de determinadas especialidades, sobre todo traumatología y cirugía general , siendo con diferencia la artroscopia de rodilla la reina de las artroscopias (más de cuatro millones de artroscopias de rodilla se realizan en todo el mundo cada año), siguiéndole el hombro y la cadera.
Algunas de las patologías que se pueden tractar con artroscopia son: sutura del menisco, exéresis de un fragmento de menisco lesionado, limpieza quirúrgica de una lesión del cartílago (lesión condral), reparación y revisión ligamentosa, eliminación o raspado de una calcificación…
Al finalizar la cirugía el médico cierra los portales (incisiones cutáneas) mediante una pequeña sutura con hilo o puntos adhesivos y suele colocarse un vendaje semicompresivo en la articulación tratada (en caso del hombro se coloca un cabestrillo).
La intervención es rápida y mínimamente invasiva , aunque el paciente permanece un tiempo en quirófano tras la misma y hasta recuperarse de la anestesia.
¿Cuál es la preparación previa a la artroscopia?
Si tu traumatólogo opta por hacerte una artroscopia de rodilla va a ser necesaria la realización de unas pruebas preoperatorias (analítica general, electrocardiograma y, probablemente, una radiografía de tórax) que serán valoradas por el anestesista para decidir el tipo de anestesia más indicado en tu caso. Se valorará la cirugía a realizar, el perfil médico del paciente, así como la medicación crónica . En caso de personas cardiópatas, hipertensos o diabéticos puede ser precisa una modificación de la pauta médica habitual de forma temporal.
En el caso concreto de una artroscopia de rodilla suele emplearse una anestesia epidural pero la decisión es tomada por el anestesista tras valorar al paciente médicamente junto a sus pruebas preoperatorias aportadas. Otros tipos de anestesia podrían ser la locorregional o la general.
Después de la operación…
Una vez en la habitación, las medidas generales que se realizan tras la artroscopia son: aplicación de hielo local frecuentemente, control de analgesia (en función del dolor optaremos por analgesia vía oral o endovenosa), medidas de prevención de trombosis y elevación de la extremidad afecta. Seremos dados de alta del hospital generalmente a las 24 horas si no ha habido ninguna incidencia médica post-quirúrgica.
Ya en el domicilio comienza la fase de recuperación de la articulación tratada (que será mucho más corta que en la cirugía tradicional abierta). Debemos seguir la pauta domiciliaria indicada por nuestro médico e iniciar la rehabilitación precozmente para evitar atrofias musculares por desuso.
¿Y qué signos deben hacernos sospechar complicaciones cuando estamos en casa?
Sobre todo, la presencia de fiebre, signos inflamatorios agudos (calor, aumento de temperatura local, inflamación o enrojecimiento), dolor incontrolado y signos sospechosos de complicación vascular (musculatura dura y dolorosa o dedos fríos o insensibles). En estos casos, es preciso contactar con la consulta del cirujano o con nuestra línea médica para explicar los síntomas y valorar su gravedad.
Tras la cirugía debemos seguir controles de forma periódica. Es posible que precisemos tratamiento rehabilitador realizado en un centro específico (será pautada por nuestro médico). Progresivamente nos podremos reincorporar a nuestra actividad habitual, aunque antes de reiniciar la actividad deportiva precisamos la autorización de nuestro médico.
A modo de conclusión, decirte que la artroscopia es una técnica quirúrgica que no está exenta de las complicaciones habituales de una cirugía convencional (anestesia, infección de herida, fiebre…). Sin embargo, es muy resolutiva , mínimamente invasiva y de recuperación rápida. Requiere una mínima estancia hospitalaria y no deja secuela cutánea estética (sin cicatriz).
 Savia
Savia