Enfermedades

Enfermedad
Pielonefritis
¿Qué es la pielonefritis?
La pielonefritis, también conocida como infección urinaria alta, es una infección de las vías urinarias que, generalmente, afecta al parénquima (tejido que recubre el riñón) y pelvis renal, comienza en la uretra o en la vejiga y sube hasta uno o ambos riñones. Es más frecuente en mujeres jóvenes sexualmente activas o postmenopáusicas y durante el embarazo . En hombres ocurre menos a consecuencia de hiperplasia prostática (aumento de la próstata), que dificulta la excreción de la orina a partir de los 50 años. En el caso de niños se debe a malformaciones urológicas. Es una enfermedad común y en algunos casos potencialmente grave que, si no se trata a tiempo y correctamente, puede llevar a la sepsis, fallo múltiple del órgano, causar daño permanente a los riñones, o a que las bacterias se logren diseminar en el torrente sanguíneo y provocar una infección que puede poner en riesgo la vida.
Tipos de pielonefritis
La pielonefritis se clasifica en:
Pielonefritis aguda no complicada : generalmente ocurre en mujeres jóvenes sin antecedentes de enfermedades o cambios en la anatomía del sistema urinario. El cuadro clínico es de fiebre alta, escalofríos, náuseas, vómitos y dolor lumbar.
Pielonefritis aguda complicada : la pielonefritis complicada evoluciona con absceso dentro o alrededor de los riñones, necrosis de la papila renal o producción de gases en el riñón, un cuadro llamado pielonefritis enfisematosa. La pielonefritis complicada por lo general ocurre en personas con obstrucción del tracto urinario, y bacterias resistentes a los antibióticos o en diabéticos. El cuadro clínico es igual a la pielonefritis no complicada, sin embargo, presenta poca respuesta a los antibióticos.
Pielonefritis crónica: la pielonefritis crónica es una infección urinaria recurrente, generalmente asociada a malformaciones urinarias, obstrucciones por cálculo renal o reflujo vesicoureteral. Generalmente lleva a la cicatrización del riñón y la insuficiencia renal crónica, especialmente en niños con reflujo urinario.
Causas de la pielonefritis
Las bacterias que ingresan en las vías urinarias a través del tubo que transporta la orina del cuerpo pueden multiplicarse y desplazarse a los riñones. Esta es la causa más frecuente de infecciones renales. También las bacterias de cualquier otra parte del cuerpo pueden extenderse a los riñones a través del torrente sanguíneo.
Síntomas de la pielonefritis
Los síntomas de la pielonefritis incluyen:
Fiebre y escalofríos.
Dolor en la espalda, el costado o la ingle.
Dolor abdominal.
Necesidad imperiosa y constante de orinar.
Sensación de ardor o dolor al orinar.
Náuseas y vómitos.
Pus o sangre en la orina.
Orina turbia o con olor desagradable. Entre otros síntomas.
Tratamiento para la pielonefritis
Los antibióticos son la primera línea de tratamiento para las infecciones renales . Los medicamentos que se indiquen y el tiempo de uso dependerá del estado de salud, así como del tipo de bacteria. Por lo general, los signos y síntomas de una infección renal comienzan a desaparecer a los pocos días de tratamiento.
No obstante, es posible que se necesite continuar tomando antibióticos durante una semana o más. Si se tiene una infección renal grave, puede ser recomendable la hospitalización.
El tratamiento puede comprender antibióticos y líquidos que se reciben a través de una vena del brazo (por vía intravenosa) .
La duración de la hospitalización dependerá de la gravedad de la enfermedad.
Pruebas complementarias del tratamiento de la pielonefritis
Para el diagnóstico y tratamiento de la pielonefritis se realizan pruebas como: análisis de orina y urocultivo para analizar la presencia de bacterias, sangre o pus. Ecografía. y tomografía computarizada. Un tipo de radiografía llamada «cistouretrografía miccional» que consiste en una inyección de un tinte de contraste para tomar una radiografía de la vejiga cuando esta está llena y mientras se orina.
Factores desencadenantes de la pielonefritis
No se conoce un factor específico que pueda desencadenar la pielonefritis.
Factores de riesgo de la pielonefritis
Los factores que aumentan el riesgo de la pielonefritis:
El sexo femenino, debido a que la uretra de las mujeres es más corta, por lo cual es más fácil que las bacterias se trasladen desde fuera del cuerpo hasta la vejiga.
Cistitis (inflamación de la vejiga).
Tener un bloqueo de las vías urinarias.
Tener el sistema inmunitario debilitado.
Tener lesiones en los nervios que rodean la vejiga.
Usar un catéter urinario o vesical durante un tiempo.
Diabetes mellitus.
Embarazo. .
Complicaciones de la pielonefritis
Las complicaciones de la pielonefritis incluyen:
Sepsis (complicación más frecuente).
Formación de cicatrices en el riñón.
Intoxicación de la sangre.
Complicaciones en el embarazo.
Recurrencias de pielonefritis.
Absceso perinefrítico.
Insuficiencia renal aguda.
Prevención de la pielonefritis
Para prevenir la pielonefritis es necesario:
Tomar abundantes líquidos, en especial agua.
Orinar apenas se sienta la necesidad.
Limpiarse cuidadosamente y adecuadamente después de orinar.
Vaciar la vejiga después de las relaciones sexuales.
Especialidades a las que pertenece la pielonefritis
La pielonefritis pertenece a la especialidad de nefrología y urología. La nefrología es la parte de la medicina que se encarga de la anatomía, la fisiología y las enfermedades del riñón. La urología es la rama de la medicina que maneja el sistema urinario en la mujer y el sistema genito-urinario en el hombre.
Preguntas frecuentes
¿Qué es la cistitis?
La cistitis es la inflamación de la vejiga.
¿Qué diferencias hay entre la pielonefritis y la cistitis?
La cistitis y la pielonefritis son dos tipos de infecciones del tracto urinario, coloquialmente conocidas como infecciones de orina. La cistitis afecta a la vías bajas del tracto urinario, que abarca desde la vejiga hasta la uretra, mientras que, la pielonefritis, por su parte, se da en las vías altas, desde los riñones a los uréteres y afecta la pelvis y parénquima renal.
¿Cómo se coge la cistitis?
La cistitis es causada por la presencia de bacterias como la Escherichia coli y diversas especies del género Proteus y Klebsiella pneumoniae . Otras razones son no realizar una higiene adecuada y correcta después de realizar una deposición, que debe de ser siempre desde la vagina hacia el ano, principalmente en las mujeres, ya que la entrada de la uretra de la mujer se encuentra más cerca del ano. También en las relaciones sexuales más comúnmente con el sexo anal y el uso de DIU (dispositivo intrauterino).
¿Qué es la cistitis crónica?
La cistitis intersticial o cistitis crónica consiste en la inflamación prolongada de la vejiga. Esta puede ser muy molesta y dolorosa.
¿Qué es una infección de orina?
Una infección de las vías urinarias es una infección que se produce en cualquier parte del aparato urinario: los riñones, los uréteres, la vejiga y/o la uretra. La mayoría de las infecciones ocurren en las vías urinarias inferiores la vejiga y la uretra.

Enfermedad
Oxiuriasis
¿Qué es la oxiuriasis?
La oxiuriasis, también conocida como enterobiasis, es una infestación parasitaria intestinal , causada por el Oxiuro enterobius vermiculares, que es un pequeño helminto nematodo (gusano), un parásito del hombre de forma cilíndrica y color blanco que mide alrededor de 1 cm. Es la enfermedad parasitaria más común alrededor del mundo, el ser humano es el único huésped natural y su infección se produce en todos los países y grupos socioeconómicos. Es más frecuente en niños de entre 5-11 años de edad, pero puede aparecer a cualquier edad, aunque rara vez se puede ver en niños de 2 años. Tiene una prevalencia alta. Es una enfermedad leve que responde muy bien al tratamiento adecuado.
Causas de la oxiuriasis
La causa principal de las oxiuriasis es la presencia del parásito Enterobius vermicularis u oxiuro , que es un gusano nematodo, redondo, pequeño, de 1 cm. de longitud, blanco y filamentoso y que habita exclusivamente en el intestino grueso de los seres humanos. Mientras la persona afectada duerme, la hembra sale del tracto intestinal y pone los huevos en la piel que rodea al ano, tiene la capacidad de producir diariamente varios miles de huevos, los cuales tienen un periodo de incubación de 3-6 semanas.
La infestación se inicia con la ingesta de los huevos de Enterobius vermicularis, que se puede dar a través de las manos contaminadas con huevos, por medio de fomites, o por la presencia de huevos en la ropa de cama o toallas, entre otras que permitan su ingreso al tracto digestivo.
Síntomas de la oxiuriasis
La mayoría de las personas infectadas por oxiuriasis no experimentan síntomas al principio , generalmente estos se presentan a partir de la 2-4 semanas después del contagio. Los más frecuente son prurito (picazón) perineal más intenso durante la noche, así como vulvar y nasal. Falta de sueño, irritabilidad, nerviosismo, inquietud, adelgazamiento, dolor abdominal, náuseas y bruxismo. Los gusanos adultos pueden migrar a la región vaginal y producir vulvovaginitis (inflamación de la vulva y la vagina) y flujo vaginal.
Tratamiento para la oxiuriasis
El tratamiento de la oxiuriasis es simple y con una tasa de curación muy alta. Pero para que sea del todo efectivo se debe administrar tanto al paciente afectado como a los familiares que viven en la misma casa para así disminuir el riesgo de una nueva infección. El tratamiento consiste en:
Albendazol , 400 mg. en una sola dosis, vía oral. Se debe repetir la dosis en dos semanas.
Mebendazol , 100 mg, 2 veces al día durante 3 días consecutivos por vía oral . También se puede administrar 100 mg. en una sola dosis. Se repite la dosis en dos semanas. Pamoato de pirantel, 10 mg/kg, una sola dosis, hasta máximo de 1.000 mg.
Pruebas complementarias del tratamiento de la oxiuriasis
Las pruebas diagnósticas para el tratamiento de la oxiuriasis se dan a través del método de Graham , que utiliza una cinta adhesiva en la piel alrededor del ano para que los huevos que se encuentran en esta región se peguen a la cinta. Estos huevos, por lo tanto, son colocados en una lámina de vidrio y visualizados en un microscopio para detectar el Oxiuro .
Factores desencadenantes de la oxiuriasis
El factor desencadenante de la oxiuriasis es la presencia del Oxiuro o Enterobius vermicularis .
Factores de riesgo de la oxiuriasis
Los factores de riesgo de la oxiuriasis son:
La edad, son más frecuente en niños.
Mala higiene personal: hacinamiento, vivir con familias afectadas por la parasitosis.
Manos contaminadas con los huevos de Oxiuros. Si el paciente se rasca el ano con sus manos puede pasar los huevos por muchos medios y transmitirlo a otras personas.
Complicaciones de la oxiuriasis
Las compliccaiones de la oxiuriasis son:
La parasitosis puede ascender desde la vagina hacia el peritoneo, donde es englobado llegando a producir una peritonitis (inflamación del peritoneo por una infección).
El rascado del ano y sus alrededores puede causar excoriaciones e infecciones añadidas de la piel por otros gérmenes más agresivos como algunas bacterias.
Prevención de la oxiuriasis
La prevención de la oxiuriasis consiste en :
Tener una buena higiene personal adecuada.
Lavarse las manos después de ir al baño y antes de comer.
Se recomienda bañarse todos los días.
Cambiar la ropa interior con regularidad.
Aconsejar a los niños a no rascarse la zona anal.
No introducir las manos en la boca o ningún objeto como los juguetes.
La ropa de cama debe ser cambiada con regularidad y lavarse con agua caliente.
Especialidades a las que pertenece la oxiuriasis
Las especialidades medicas a las que pertenece la oxiuriasis son pediatría si afecta a los niños y en adultos medicina general o medicina interna .
Preguntas frecuentes
¿Qué son los oxiuros?
Los Oxiuros, también conocidos como lombrices intestinales, son parásitos del tubo digestivo que se parecen a los gusanos y que pueden vivir en el colon y el recto. Tienen forma de unos filamentos blancos.
¿Cómo se producen lombrices en los niños?
Las lombrices se producen en los niños por autocontagio, básicamente por la boca cuando se ingieren los huevos del parásito, al rascarse el ano con las manos y luego llevarlas a la boca o al ingerir un alimento que esté en contacto con el Oxiuro o algún objeto o juguete a la boca. Los huevos llegan hasta el intestino delgado donde salen las larvas, y cuando llegan al intestino grueso se hacen adultos. A los uno o dos meses las hembras se reproducen y ponen los huevos.
Si tengo lombrices… ¿Puedo tomar azúcar?
Si tienes lombrices puedes comer azúcar, ya que esto no está implicado con el contagio de las lombrices.

Enfermedad
Osteomielitis
¿Qué es la osteomielitis?
La osteomielitis es la infección de un hueso y la médula ósea, que se caracteriza por la destrucción progresiva inflamatoria del tejido óseo y que suele producirse principalmente por bacterias piogenas (que producen pus) así como, en algunos casos, por micobacterias y/u hongos. Involucra y afecta las diferentes estructuras óseas como el periostio, la cavidad medular, el endostio y en ocasiones vasos sanguíneos y nervios .
Periostio : membrana de tejido conjuntivo, adherida exteriormente a los huesos, que sirve para su nutrición y regeneración.
Cavidad medular : es el espacio interno de la diáfisis (parte tubular de un hueso largo), que contiene a la médula ósea amarilla grasa
Endostio : membrana vascular delgada del tejido conjuntivo que rodea la superficie interior del tejido óseo que forma la cavidad medular de los huesos largo.
Las infecciones pueden llegar al hueso a través del torrente sanguíneo o pueden diseminarse a través del tejido que lo rodea. Es más común en gestantes, niños y adultos de edad avanzada, aunque puede afectar a personas de todas las edades. Afecta más a los hombres que a las mujeres. La población con mayor riesgo incluye a las personas cuyo sistema inmunológico se encuentra debilitado. En niños con mayor frecuencia resultan afectados los huesos largos de brazos y piernas. En los adultos, la osteomielitis es más probable que se manifieste en los huesos de la columna vertebral. La destrucción ósea puede ser muy extensa si no se hace un diagnóstico rápido y se inicia el tratamiento.
Tipos de osteomielitis
Los tipos de osteomielitis incluyen:
Osteomielitis aguda : es aquella que evoluciona en menos de dos semanas. Es la infección bacteriana piógena (produce pus) localizada en huesos a partir de un área previamente infectada del organismo y que se denomina foco primario. El foco primario puede estar en intestino, oído medio, o a partir de piel: forúnculo, ántrax, celulitis…etc.
Osteomielitis crónica : es la que evoluciona en más de cuatro semanas o que no responde al tratamiento antibiótico y requiere cirugía para su curación. Son los enfermos que una vez pasado el período agudo, con tratamiento o sin él, presentan supuración piógena crónica del hueso, siendo característica la presencia de secuestro, cavidades y fístulas.
Osteomielitis no hematógena : la que ocurre por inoculación directa, tras un traumatismo o cirugía o por diseminación a partir de un foco contiguo, generalmente celulitis.
Causas de la osteomielitis
Las causas de la osteomielitis son principalmente bacterianas, debido al Staphylococcus aureus . Los tipos de gérmenes que normalmente se encuentran en la piel o en la nariz de las personas sanas, provocan la mayoría de los casos de osteomielitis. Dependiendo de la forma en la que el hueso se infecta y de la edad de la persona, otros tipos de bacterias pueden también causar esta enfermedad. Las bacterias pueden infectar a los huesos de varias maneras, pudiendo llegar al hueso a través del torrente sanguíneo proveniente de otras áreas infectadas del cuerpo.
Otra forma de contraer la osteomielitis es por una infección directa, cuando la bacteria entra en los tejidos del cuerpo a través de una herida y viaja hasta el hueso. Un hueso también puede infectarse cuando el riego sanguíneo al área del hueso se interrumpe. Esto puede ocurrir en las personas mayores que sufren de arteriosclerosis, lo cual es un estrechamiento de los vasos sanguíneos, o si hay una asociación con la diabetes.
Síntomas de la osteomielitis
Los síntomas de la osteomielitis incluyen: fiebre y/o escalofríos, dolor severo en el área del hueso infectado, irritabilidad o letargo en niños pequeños, hinchazón, así como calor y enrojecimiento sobre la zona de la infección. A veces la osteomielitis no produce signos ni síntomas o tiene signos y síntomas que son difíciles de distinguir de otros trastornos .
Tratamiento para la osteomielitis
La osteomielitis aguda requiere de tratamiento antibiótico que debe ser iniciado sin demora, aunque idealmente se debería obtener una muestra de material infeccioso previamente y comenzar el tratamiento en las primeras 72 horas desde el inicio del cuadro, pues en ese período el hueso aún conserva una adecuada irrigación sanguínea y el antibiótico llega mejor al foco infeccioso.
En la osteomielitis crónica, además del uso de antibióticos de forma prolongada , en muchas ocasiones, se requiere cirugía, limpiando la zona afectada del material infeccioso, desbridando los tejidos muertos para facilitar la llegada del antibiótico, y rellenando los defectos óseos. También se puede aplicar un tratamiento antibiótico local en el hueso afectado.
Pruebas complementarias del tratamiento de la osteomielitis
Para el diagnóstico y tratamiento de la osteomielitis es necesario un análisis de sangre que puede revelar niveles altos de glóbulos blancos y otros factores que pueden indicar que el organismo está combatiendo una infección. Si la causa de la osteomielitis es una infección de la sangre , el análisis puede revelar qué gérmenes son los causantes. Otras pruebas importantes son las radiografías, que pueden revelar el daño en el hueso, o exploración por tomografía computarizada (escáner) y la resonancia magnética, así como la biopsia ósea.
Factores desencadenantes de la osteomielitis
No se conoce un factor específico que pueda desarrollar la osteomielitis.
Factores de riesgo de la osteomielitis
Los factores que aumentan el riesgo de la osteomielitis incluyen traumas, fracturas óseas graves o heridas punzantes profundas, ya que abren una vía para que las infecciones ingresen al hueso y al tejido que lo rodea. Otros factores de riesgo son los trastornos de la circulación, las afecciones que requieren vías intravenosas o sondas y los trastornos que afectan el sistema inmunitario . Las personas que se inyectan drogas intravenosas tienen más probabilidades de tener osteomielitis porque habitualmente usan agujas no estériles y no desinfectan la piel antes de las inyecciones. Gestantes y niños son de igual modo más propensos a esta enfermedad, así como las personas con diabetes, osteoartritis, neoplasias (tumores) o prótesis articulares.
Complicaciones de la osteomielitis
Las complicaciones de la osteomielitis incluyen:
Muerte ósea (osteonecrosis).
Alteración del crecimiento.
Artritis séptica.
Cáncer de piel.
Prevención de la osteomielitis
La prevención de la osteomielitis no siempre es posible porque no es una infección predecible, está más asociada a tomar medidas de protección para la salud que disminuyan los factores de riesgo, como:
Evitar caídas o lesiones osteomusculares en niños y ancianos.
Cuidado de fracturas óseas expuestas o que se puedan ver a través de la piel.
Prevenir las infecciones de la piel debidas a diabetes mellitus.
Desinfectar bien las heridas y tenerlas limpias y secas.
Especialidades a las que pertenece la osteomielitis
La osteomielitis pertenece a la especialidad de traumatología y ortopedia , es la parte de la medicina que se dedica al diagnóstico, tratamiento, rehabilitación y prevención de lesiones y enfermedades del sistema musculoesquelético del cuerpo humano. Este complejo sistema incluye los huesos, las articulaciones, los ligamentos, los tendones, los músculos y los nervios que le permiten a una persona moverse, trabajar y ser activa.
Preguntas frecuentes
¿Qué bacteria causa la osteomielitis?
La bacteria más común que causa la osteomielitis es la Staphilococcus aureus , aunque existen otros tipos de micobacterias que también la pueden causar.
¿Qué es la osteomielitis maxilar?
La osteomielitis maxilar es una infección odontógena de etiología bacteriana donde los agentes causales son los de la cavidad oral, como Staphylococcus aureus entre otros. Afecta principalmente al maxilar inferior, y en raras ocasiones puede afectar al superior; esto es debido a que este tiene una mayor vascularización.
¿Qué es un absceso de Brodie?
El absceso de Brodie es un absceso intraóseo relacionado con un foco de osteomielitis piógena sub-aguda definida por cierta características clínicas, radiológicas y patológicas.
¿Qué es la osteoesclerosis?
La osteoesclerosis es una lesión consistente en un engrosamiento del hueso, aumento de su densidad, con posible disminución del espacio medular y la consiguiente atrofia de la médula ósea.
¿Qué es la pseudoartrosis?
La pseudoartrosis es una articulación falsa que se forma después de una fractura cuyos fragmentos óseos no se han consolidado.
Enfermedad
Alopecia Areata
¿Qué es la alopecia areata?
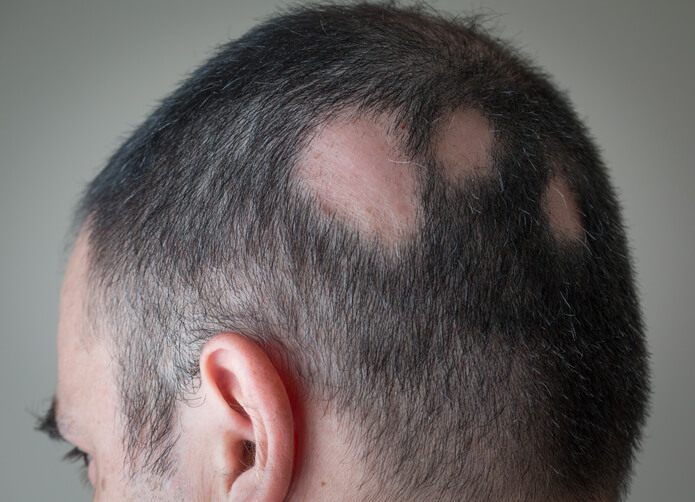
La alopecia areata o pérdida de cabello es una enfermedad de tipo autoinmune que consiste en la pérdida de pelo en una zona localizada del cuerpo. Generalmente aparece en áreas pequeñas y redondeadas, del tamaño de una moneda, ya sea de la barba y/o del cuero cabelludo. Es una enfermedad leve y no requiere urgencia médica, sin embargo, es crónica y puede aparecer en varias ocasiones a lo largo de la vida. Afecta a ambos sexos ya cualquier edad, siendo más común en niños y en adolescentes.
Tipos de alopecias
Alopecia areata en placa única : es la presentación más habitual y afecta solo un área.
Alopecia areata e placa múltiple : hay más zonas afectadas.
Alopecia areata total : afecta todo el cuero cabelludo, produciendo calvicie completa.
Alopecia areata universal : se extiende por todo el cuerpo: axilas, pubis, cejas y pestañas.
Alopecia areata difusa : la zona afectada no está muy definida y es difícil de diagnosticar.
Alopecia areata del cabello oscuro : es una forma rara y afecta sólo a los cabellos de color normal y no a las canas o pelos no pigmentados. Suele darse en situaciones de gran estrés. Se la conoce como areata tipo María Antonieta en las mujeres, o Tomás Moro en hombres.
Alopecia areata ofiásica : la pérdida de pelo se localiza en sienes y nuca.
Causas de la alopecia areata
La alopecia areata tiene un origen autoinmune; las defensas de nuestro propio organismo atacan al folículo piloso (la raíz del pelo), haciendo que esta se inflame y se caiga el pelo, volviendo a salir cuando baja la inflamación. Otras causas pueden ser psicológicas, en periodos de mucho estrés , eventos importantes, o época de estudios. Otras causas pueden ser durante el embarazo, una enfermedad, o procesos infecciosos.
El perfil genético es importante, 1 de cada 5 personas afectadas tiene antecedentes familiares de alopecia.
Síntomas de la alopecia areata
Los síntomas son la caída del pelo en zonas localizadas formando placas redondeadas en cuero cabelludo, barba o cejas. La piel de esa zona mantiene el folículo piloso pero sin pelo.
La piel es blanca y suave al tacto, y rara vez está inflamada. Alrededor de la placa se observan pelos cortos delgados hacia arriba y gruesos hacia abajo.
Otro síntoma es que, al tirarnos de manera suave de un mechón de pelo, este se arranca fácilmente.
Tratamiento de la alopecia areata
No existe un tratamiento totalmente eficaz y no siempre requiere tratamiento inicial. El 50% de los pacientes se recuperan sin tratamiento en poco tiempo y de manera espontánea. Si el origen es psicológico, la recuperación del cabello es rápida y sencilla al disminuir la carga emocional, a veces de requiere la ayuda de profesionales.
El tratamiento se empieza de menos agresivo y menos efectos secundarios a más, y estos suelen ser de larga duración.
Los fármacos empleados intentarán frenar la caída del pelo e intentar, no solo que este crezca, sino que se mantenga. Primero hay que descartar alguna enfermedad o proceso infeccioso, antecedentes familiares o situación psicológica.
Los más empleados son de uso tópico, como las cremas o champús de zinc , corticoides, vasodilatadores como el Minoxidil , o inmunosupresores como Ciclosporina Metotrexato . Si no son efectivos, se pasa a tratamiento con fototerapia, fotoquimioterapia, láser y tratamientos en forma de pastillas o inyecciones locales como los corticoides, inmunomoduladores.
En el caso de algunas patologías como la enfermedad celíaca, solo la dieta sin gluten contribuiría a la recuperación del pelo.
Pruebas complementarias de la alopecia areata
Durante la exploración, el médico realiza:
Pull-test : pequeños tirones de mechones de pelo para así examinar la raíz de los cabellos y ver si ha sido por una inflamación de la raíz.
Tricoscopia digital : es un microscopio digital que hay en las consultas para el análisis del pelo desde su raíz, para ver los efectos del tratamiento aplicado. Si hay inflamación, se observan pelos como el signo de exclamación (!) y puntos negros en la piel de la zona afectada. También permite observar el vello fino cuando el pelo está creciendo.
Análisis de sangre : para valorar la función hormonal del tiroides, alteraciones autoinmunes o alergias.
Factores desencadenantes de la alopecia areata
Los factores desencadenantes son generalmente genéticos, cargas emocionales y psicológicas, alteraciones hormonales, procesos infecciosos u otras enfermedades.
Factores de riesgo de la alopecia areata
Los factores de riesgo podrían ser una situación de estrés, gran carga emocional, mala alimentación, embarazo …etc. Es una enfermedad que afecta a la calidad de vida de los pacientes, pudiendo afectarles de manera psicológica, lo que agravaría aún más la enfermedad.
Complicaciones de la alopecia areata
La complicación de la alopecia areata es que no se consiga erradicar la enfermedad, y por tanto, la pérdida de pelo continúa hasta que las zonas afectadas se juntan unas con otras hasta convertirse en grandes áreas sin pelo o la pérdida total del cabello.
Prevención de la alopecia areata
La alopecia areata no se puede prevenir.
Especialidades a las que pertenece
La alopecia areata es una enfermedad que es tratada por el dermatólogo.
Preguntas frecuentes
¿Qué es la alopecia frontal fibrosante?
La alopecia frontal fibrosante es un tipo de alopecia cicatrizal cuyo origen no está definido. La caída del pelo se localiza en la parte frontal de la cabeza haciendo que cada vez crezca el pelo más lejos de la frente. Afecta más a mujeres pre y postmenopáusicas.
¿Qué es la alopecia seborreica?
La alopecia seborreica aparece cuando las glándulas sebáceas producen más cantidad de grasa de la necesaria. Esto nos causa picor, aspecto sucio del pelo y, en estados más avanzados, comienza a caerse porque el pelo no puede respirar bajo tanta grasa. Afecta más a hombres en edad juvenil.
¿Qué es la dermatitis en el pelo?
La llamada dermatitis seborreica, es una afectación dermatológica común, crónica y no contagiosa, que consiste en la descamación de algunas zonas de la piel donde hay glándulas sebáceas que producen grasa. Afecta más a hombres y a recién nacidos, produciendo la llamada costra láctea.
¿Qué es bueno para la dermatitis seborreica?
Para la dermatitis seborreica son buenos los champús, cremas o lociones con corticosteroides para la inflamación, los antifúngicos lo champús contra la caspa. Como remedios caseros podía ayudar el aceite de oliva o aloe vera masajeando la zona afectada. Hay que evitar productos químicos como moldeados o tintes, o que contengan alcohol.
¿Qué es la Malassezia?
La Malassezia es un género de hongo que se encuentra en la piel de todos los animales, incluidos los humanos, y es el causante de la caspa y de la pitiriasis versicolor (enfermedad infecciosa pero no contagiosa que produce manchas en la piel de color canela o marrón que se descama al rascarse).

Enfermedad
Infección Nosocomial
¿Qué es una infección nosocomial?
La infección nosocomial se define como cualquier infección adquirida durante el tiempo en el que el individuo está hospitalizado , pudiendo manifestarse mientras está internado o después de haber sido dado de alta. Es una afección muy común y puede ser grave si no se trata a tiempo y correctamente.
Estas infecciones están relacionadas con la hospitalización o los procedimientos realizados en el hospital. Son aquellas que se presentan transcurridas las primeras 72 horas después del ingreso en el hospital o antes de los 15 días del alta hospitalaria. Las infecciones nosocomiales son más frecuentes en personas mayores y en niños.
Tipos de infecciones
Dependiendo del tipo de organismo causante de la enfermedad, las infecciones pueden clasificarse en:
Infecciones bacterianas: causadas por bacterias (organismos microscópicos formados por una sola célula que carecen de núcleo). Aunque son muchas las especies que pueden provocar enfermedad en el ser humano, lo hacen menos del 1% de las bacterias existentes. Muchas de las bacterias patógenas liberan toxinas que pueden dañar los tejidos y causar enfermedades. Entre los ejemplos de bacterias que causan infecciones se incluyen los estreptococos, los estafilococos o Escherichia coli, entre muchas otras.
Infecciones por hongos: causadas por hongos se conocen como fúngicas o micóticas. Los hongos son organismos con al menos un núcleo. Los hongos están por todas partes, viven en el aire, el suelo, las plantas y el agua, e incluso algunos lo hacen dentro del cuerpo humano. Sólo aproximadamente la mitad de todos los tipos de hongos son dañinos. Algunos se reproducen mediante pequeñas esporas en el aire, que pueden inhalarse o pueden caer sobre las personas. Como consecuencia, las infecciones fúngicas suelen comenzar en los pulmones o en la piel. Ejemplos de enfermedades provocadas por estos organismos son el pie de atleta, causado por el parásito Tinea pedis, o la candidiasis vaginal, causada por levadura Candida albicans y otras especies.
Infecciones virales: causadas por virus que son microorganismos infecciosos más pequeños que las bacterias y los hongos. No pueden reproducirse por sí mismos, por lo que necesitan invadir una célula viva que le proporcionará la energía y la maquinaria necesaria para multiplicarse. Ejemplos de enfermedades virales son la varicela, causada por el virus varicela zóster; el resfriado común, causado por rinovirus; las hepatitis virales como la hepatitis C o el sida, causado por el virus de la inmunodeficiencia humana.
Infecciones asociadas a la asistencia sanitaria: las infecciones asociadas a la asistencia sanitaria son aquellas que tienen relación con prácticas asistenciales en pacientes que están hospitalizados o atendidos de forma ambulatoria, pero en contacto con el sistema sanitario. Se estima que afectan a alrededor del 5% de los pacientes y comportan una elevada morbimortalidad y un gran coste económico. Los principales tipos de infección asociados a la asistencia sanitaria están relacionados con procedimientos invasivos. Los más frecuentes son la infección respiratoria, la quirúrgica, la urinaria y la bacteriemia de catéter vascular.
Causas de la infección nosocomial
Las causas de una infección nosocomial suelen ser microorganismos (bacterias, virus, hongos o parásitos) de diferentes tipos, fácilmente contagiosos y en ocasiones con resistencia a los antibióticos habituales.
Algunas de las bacterias con cepas resistentes que están implicadas en infecciones nosocomiales son: neumococos, enterococos, estafilococos, por ejemplo, estafilococo aureus meticilina resistente, escherichia coli, tuberculosis, klebsiella pneumoniae, pseudomonas aeruginosa, clostridium,legionella, etc.
Generalmente, los microorganismos que causan la infección hospitalaria no causan infecciones en otras situaciones, ya que aprovechan el ambiente con pocas bacterias inofensivas y el debilitamiento del sistema inmune del paciente para instalarse. A pesar de esto, las bacterias hospitalarias suelen desarrollar infecciones graves y de difícil tratamiento, ya que son más resistentes a los antibióticos, por esto, generalmente es necesario utilizar fármacos más potentes para curar este tipo de infección.
Cualquier procedimiento de diagnóstico o de tratamiento que implique una invasión del interior del organismo puede tener un riesgo de contaminación, por ejemplo, biopsias, endoscopias, catéteres, intubación y operación quirúrgica.
Síntomas de la infección nosocomial
Los síntomas de una infección nosocomial son los propios del agente infeccioso que la provoca y del órgano o sistema que sufre la infección. Los síntomas pueden incluir dolor de garganta, fiebre, inflamación de los nódulos linfáticos en el cuello, dolor pélvico, necesidad urgente de orinar, dolor al orinar , sangre en la orina, la piel afectada tiene una apariencia hinchada y rojiza, y puede estar caliente y sensible, diarrea, calambres, náuseas, vómitos, febrícula, tos con flema o pus, fiebre, escalofríos o dificultad para respirar.
Tratamiento de la infección nosocomial
El tratamiento de una infección nosocomial debe hacerse con el agente antimicrobiano (antibiótico, antivírico, antifúngico o antiparasitario) que sea más eficaz en cada caso. Según el tipo de infección a veces hay que hacer tratamiento preventivo a los posibles contactos. Además de tratar la causa, se aplicará el tratamiento de soporte más conveniente para mantener el buen funcionamiento del órgano o sistema afectado.
Pruebas complementarias de la infección nosocomial
El diagnóstico de una infección nosocomial no siempre es sencillo. Se basa en la demostración del agente infeccioso mediante cultivo de muestras de sangre, secreciones o tejidos , mediante análisis serológico (búsqueda de anticuerpos) o técnicas de laboratorio como reacción en cadena de la polimerasa y otras. Si se trata de una bacteria, en las pruebas complementarias se realiza un antibiograma , que permite saber a qué antibióticos tiene resistencia y a cuál es sensible.
Factores de riesgo de la infección nosocomial
Cualquier persona puede desarrollar una infección nosocomial, sin embargo, tienen mayor riesgo aquellas que tienen el sistema inmunitario más débil como:
Ancianos.
Recién nacidos.
Personas con la inmunidad comprometida, por enfermedades como HIV/SIDA.
Post-trasplantados o que usen medicamentos inmunosupresores.
Diabetes Mellitus mal controlada.
Personas encamadas o con alteración de la conciencia, ya que presentan mayor riesgo de broncoaspiración.
Enfermedades vasculares con el compromiso de la circulación, ya que dificulta la oxigenación y cicatrización de los tejidos.
Realización de cirugías.
Asimismo, mientras más sea el tiempo de hospitalización mayor es el riesgo de adquirir una infección nosocomial, ya que hay mayor exposición a los microorganismos responsables.
Complicaciones de la infección nosocomial
Las complicaciones de la infección nosocomial pueden incluir:
Convulsiones.
Pérdida de conocimiento.
Inflamación de las extremidades.
Dificultad para respirar.
Fiebre o temperatura corporal baja con escalofríos y temblores violentos.
Latido cardíaco acelerado o irregular.
Orinar poco o nada en lo absoluto.
Prevención de la infección nosocomial
La prevención de una infección nosocomial precisa de varias medidas:
Descontaminar las manos , con productos adecuados como jabones o soluciones antisépticas, agua corriente en un lavabo que tenga dispositivos antisalpicaduras y con toallas desechables.
Realizar las técnicas sanitarias con procedimiento estéril o aséptico y un tiempo de lavado adecuado.
Usar guantes de látex o cloruro de vinilo.
Evitar inyecciones o procedimientos médicos que no sean necesarios.
Limpieza escrupulosa del centro hospitalario.
Desinfección y esterilización de los materiales sanitarios que sean reutilizables.
Especialidades a las que pertenece
La infección nosocomial pertenece a la especialidad de infectología, rama de la medicina interna que se encarga del estudio, la prevención, el diagnóstico y el tratamiento de las enfermedades producidas por agentes infecciosos (bacterias, virus, hongos y parásitos)
Preguntas frecuentes
¿Qué es una bacteria nosocomial?
Las bacterias nosocomiales o grampositivas como el Staphylococcus Aureus, son saprofitos cutáneos que colonizan la piel y la nariz del personal de los hospitales y de los pacientes y pueden causar una gran variedad de infecciones pulmonares, óseas, cardiacas y sanguíneas.
¿Cuáles son las infecciones nosocomiales más frecuentes?
Las infecciones nosocomiales pueden ser adquiridas en diversas regiones del cuerpo. Los tipos más frecuentes son:
Infección urinaria : ocurre por el uso de una sonda urinaria durante el período de hospitalización. Algunas de las bacterias que intervienen en esta situación son: Escherichia coli, Proteus sp, Pseudomonas aeruginosa, Klebsiella sp., Enterobacter. Enterococcus faecalis y hongos como la Candida. Sus principales síntomas son dolor o ardor al orinar, dolor abdominal, sangrado por la orina y fiebre.
Infección de la piel: son muy comunes debido a la aplicación de inyecciones a través de las venas para medicamentos o recolección de exámenes, cicatriz de una cirugía, biopsia o la formación de escaras de decúbito. Algunos de los microorganismos que causan ese tipo de infección son: Staphylococcus aureus, Klebsiella sp, Proteus sp, Enterobacter sp, Serratia sp, Streptococcus sp, Enterococcus y Staphylococcus Epidermidis. Sus principales síntomas son enrojecimiento e hinchazón de una área de la piel, con o sin la presencia de ampollas. Generalmente, la región se encuentra dolorida y caliente, y puede haber producción de secreción purulenta y mal olorosa.
Infección de la sangre: la infección en la circulación sanguínea llamada septicemia, surge generalmente, después de la infección de alguna región del cuerpo que termina diseminándose por el torrente sanguíneo. Este tipo de infección es muy grave, y si no es debidamente tratada puede causar un fallo multiorgánico y riesgo de muerte. Sus principales síntomas son fiebre, escalofríos, caída de la presión, latidos del corazón débil y somnolencia.
¿Qué es una neumonía nosocomial?
La neumonía nosocomial es la adquirida en el hospital y suele ser grave. Es más común en las personas que están hospitalizadas o que tienen dificultades para deglutir, por el riesgo de aspiración de alimentos o de la saliva. Las bacterias más comunes en este tipo de neumonía son: Klebsiella, Enterobacter, Pseudomonas, Acinetobacter, Staphylococcus aureus, Legionella, Mycoplasma, además de algunos tipos de virus. Sus principales síntomas son dolor en el tórax, tos con secreción amarillenta o sanguinolenta, fiebre, cansancio, falta de apetito y falta de aire.
¿Qué es una infección hospitalaria?
La infección hospitalaria se define como cualquier infección adquirida durante el tiempo en que el individuo está hospitalizado, pudiendo manifestarse mientras está internado o después de haber sido dado de alta.
¿Cuál es la bacteria más peligrosa para el ser humano?
Las bacterias más peligrosas para el ser humano son: Salmonella, Helicobacter pylori y Streptococcus pneumoniae , entre otras. Tienen prioridad crítica las que resisten un tipo de antibiótico de amplio espectro usado en hospitales por vía intravenosa para atajar infecciones graves. Y entre las de prioridad alta se encuentran bacterias cada vez más resistentes y responsables de enfermedades muy conocidas como la gonorrea, la úlcera estomacal y algunos tipos de neumonía.

Enfermedad
Quiste Epidermoide
¿Qué es un quiste epidermoide?
El quiste epidermoide es una tumoración (que presenta una cápsula con contenido pastoso o líquido en su interior) que está formada por tejido ectodérmico. Se conoce también como quiste infundibular y quiste de queratina. Su situación principal se presenta en cara, tórax o cuello , y está formado por epitelio escamoso. Se da en todas las edades, siendo más frecuente entre los 15 y 32 años, su crecimiento es lento y, hasta un 7% de los casos se da en la cabeza, puede infectarse y es una enfermedad leve.
Tipos de quistes epidermoides
Los tipos de quistes epidermoides se pueden clasificar en función de su número en:
Quistes aislados en que aparece un único quiste, aparecen, en mayor medida, en la zona de la cabeza.
Quistes múltiples como los que se desarrollan en el síndrome de Gardner.
Causas de un quiste epidermoide
Las causas de un quiste epidermoide serán el traumatismo, la inflamación y la proliferación epitelial.
Síntomas de un quiste epidermoide
Los síntomas de un quiste epidermoide son la presencia de un abultamiento en la piel, que presenta una apertura hacia el exterior puntiforme, con un tapón de color negro, similar a una espinilla. Desde su interior puede drenar material amarillento y maloliente, y cuando el quiste epidermoide se infecta, se produce una inflamación local con dolor y enrojecimiento.
Tratamiento de un quiste epidermoide
Los quistes epidermoides son lesiones benignas que no siempre necesitan tratamiento, puede ser necesario retirarlos, cuando producen un problema estético o infecciones de repetición.
El tratamiento será quirúrgico pudiendo realizarse sólo la apertura del quiste , drenando la sustancia que tiene en su interior, en estos casos el quiste puede volver a reproducirse.
El tratamiento definitivo es la exéresis del quiste, es una intervención de cirugía menor en la cual se procede a inyectar anestesia local en la zona, posteriormente se procede a realizar una incisión que abarca toda la extensión del quiste, procediendo a su extracción con la cápsula que lo recubre , tras esto se procede a coser la incisión realizada, retirando los puntos en unos siete días.
En los casos en que los quistes están infectados, puede ser necesario el tratamiento con antibiótico vía oral para resolver la infección previamente a realizar la exéresis del quiste.
Pruebas complementarias de un quiste epidermoide
No suele ser necesario realizar pruebas complementarias para el diagnóstico del quiste, se realiza su análisis anatomopatológico tras la extracción del mismo, para confirmar el diagnóstico clínico .
En caso de dudas, puede realizarse una resonancia magnética para su diagnóstico.
Factores desencadenantes de un quiste epidermoide
Los factores desencadenantes del quiste dermoide serán los traumatismos en la piel.
Factores de riesgo de un quiste epidermoide
Son factores de riesgo para los quistes epidermoides el haber pasado la pubertad, ser varón y síndromes genéticos como el síndrome de Gardner.
Complicaciones de un quiste epidermoide
Tamaño del quiste.
Problemas estéticos.
Número de quistes.
Infecciones recurrentes.
Cicatrices antiestéticas tras su exéresis.
Rotura del quiste.
Prevención de un quiste epidermoide
No existe medio de prevenir los quistes epidermoides, salvo evitar los traumatismos .
Especialidades a las que pertenece
El quiste epidermoide debe de ser tratado o bien por el dermatólogo, o bien por el cirujano general, o por los especialistas en cirugía estética, estas tres especialidades pueden realizar la exéresis del quiste epidermoide.
Preguntas frecuentes
¿Qué es el epidídimo?
El epidídimo es un conducto que se encuentra en la parte posterior del testículo, es un conducto estrecho que conecta los conductos deferentes, está constituido por la unión de los conductos seminales, tiene unos cinco centímetros de longitud, es el lugar donde se produce la maduración de los gametos masculinos.
¿Qué es un quiste triquilemal?
El quiste triquilemal es una tumoración redondeada que crece lentamente, se localiza sobre la superficie de la piel y puede ir desde unos milímetros a varios centímetros. Suele aparecer en la cabeza, en especial en el cuero cabelludo. Este tipo de tumor se forma desde las capas más externas del folículo piloso, la piel que cubre estos quistes es fina y brillante, cuando se ejerce mucha presión en ellos, el contenido, de aspecto graso y con mal olor, sale al exterior.
¿Qué es un quiste en la cara?
Un quiste en la cara es una masa abultada de un tamaño variable, desde unos milímetros a uno o dos centímetros que puede ser de diverso origen. Así puede ser un lipoma, en cuyo caso el interior del quiste es material graso, un quiste epidermoide en el cual el interior es material celular epidérmico, un quiste triquilemal en el cual el interior del quiste es un material de origen piloso, o un quiste sebáceo que está formado por material graso.
En algunos casos, el acné puede dar lugar al llamado acné quístico. La característica primordial de cualquier quiste es una cápsula externa en cuyo interior se encuentra un material que puede ser líquido o pastoso.
¿Qué diferencia un quiste de un tumor?
La diferencia principal entre un quiste y un tumor es que el tumor suele ser una masa sólida y el quiste suele tener un interior pastoso o líquido. El quiste se encuentra recubierto de una cápsula que será necesaria extraer para evitar que se reproduzca la lesión, y el tumor carece de esta cápsula que lo recubre.
Enfermedad
Uveítis Anterior
¿Qué es la uveítis anterior?
La uveítis anterior es una inflamación del segmento anterior de la úvea . La úvea es la capa intermedia del ojo. La uveítis anterior afecta al iris (iritis), el cuerpo ciliar (ciclitis) y se denomina iridociclitis anterior. La inflamación puede estar asociada con enfermedades autoinmunitarias , pero en la mayoría de los casos se presenta en personas sanas. Se manifiesta en forma de dolor, enrojecimiento ocular y fotofobia (sensibilidad ante la luz).
Este trastorno puede afectar únicamente a un ojo y es más frecuente en personas jóvenes de mediana edad.
Se trata de una condición potencialmente grave, que requiere atención inmediata para prevenir la pérdida de la visión.
Tipos de uveítis
Los tipos de uveítis son:
Uveítis anterior: es la forma más común. Implica la inflamación de la parte frontal del ojo (se denomina iritis) y puede afectar al cuerpo ciliar (ciclitis). La inflamación puede estar asociada con enfermedades autoinmunitarias, pero en la mayoría de los casos se presenta en personas sanas. Se manifiesta en forma de dolor, enrojecimiento ocular y fotofobia (sensibilidad ante la luz).
Uveítis posterior: afecta la parte posterior de la úvea y compromete principalmente a la coroides (que son una capa de vasos sanguíneos y tejido conectivo en la parte media del ojo). Este tipo de uveítis se denomina coroiditis y si la retina también está comprometida se llama coriorretinitis. Esta afección se puede presentar si ha habido una infección generalizada o una enfermedad autoinmunitaria.
Uveitis intermedia : También llamada pars planitis , existe cuando se produce disminución de la agudeza visual (visión de moscas volantes), en ocasiones puede presentar fotofobia (sensibilidad a la luz). Se presenta con frecuencia en hombres jóvenes y generalmente no está asociada con ninguna enfermedad. Sin embargo, existe alguna evidencia que puede estar ligada a la enfermedad de Crohn y posiblemente a la esclerosis múltiple.
Causas de la uveítis anterior
La causa de la uveítis anterior es desconocida. Sin embargo, en algunos casos puede deberse a un traumatismo o a una infección .
Las agudas, que aparecen solo en un ojo en cada episodio pero que pueden alternar ambos ojos en diferentes episodios, se asocian con frecuencia a enfermedades reumáticas como la espondiloartropatía y suelen tener un marcador genético que es el HLA-B27.
Las infecciones asociadas con la uveítis anterior incluyen: enfermedad de Lyme, sífilis, tuberculosis, toxoplasmosis, virus del herpes y paperas.
Las crónicas son procesos más graves porque, a menudo el ojo no está enrojecido y suelen existir ya múltiples secuelas en el momento del diagnóstico, puede asociarse a enfermedades reumáticas de la infancia como artritis idiopática juvenil.
Síntomas de la uveítis anterior
Los síntomas de la uveítis anterior son:
Ojos enrojecidos.
Dolor intenso.
Lagrimeo.
Visión borrosa.
Sensibilidad a la luz (fotofobia).
Pupila pequeña o de forma irregular.
Disminución de la agudeza visual.
Tratamiento de la uveítis anterior
El tratamiento de la uveítis anterior se basa en aliviar los síntomas y reducir el cuadro inflamatorio para mejorar y preservar la visión. También es importante tratar las causas subyacentes de la uveítis anterior.
La uveítis anterior se puede tratar con:
Colirios con corticoesteroides para controlar la inflamación.
Antiinflamatorios no esteroides (AINE).
Agentes ciclopléjicos (dilatadores de la pupila) para ayudar a disminuir el dolor, la fotofobia y para evitar que el iris se adhiera al cristalino que está debajo.
Agonistas beta de uso tópico para ayudar a aliviar la presión intraocular.
Antibióticos sistémicos y locales.
Reposo.
Pruebas complementarias de la uveítis anterior
Las pruebas complementarias para el diagnóstico de la uveítis anterior deben iniciarse con una completa historia clínica, un examen ocular más profundo del interior del ojo, las pupilas, y los músculos extraoculares.
Factores desencadenantes de la uveítis anterior
No existen factores desencadenantes.
Factores de riesgo de la uveítis anterior
Los factores de riesgo de la uveítis anterior están relacionados con algunos trastornos inmunitario y problemas de salud como son:
Espondilitis anquilosante
Sarcoidosis
Artritis reumatoide
VIH
Enfermedades inflamatorias intestinales
Virus del herpes
Complicaciones de la uveítis anterior
Las complicaciones de la uveítis anterior son:
Glaucoma secundario
Desprendimiento de la retina
Catarata
Ceguera
Prevención de la uveítis anterior.
Actualmente, no existen pautas para prevenir la uveítis anterior.
Especialidades a las que pertenece
La especialidad médica a la que pertenece la uveítis es la oftalmología, que es la rama de la medicina que se encarga de tratar las enfermedades de los ojos.
Preguntas frecuentes
¿Qué es el Tyndall en los ojos?
El Tyndall en los ojos se refiere a la presencia, en la cámara anterior del ojo, de pequeños corpúsculos flotando en el humor acuoso y que está constituido por células inflamatorias y proteínas. Aparece en los procesos inflamatorios del cuerpo ciliar.
¿Cuánto dura el tratamiento de la uveítis?
El tratamiento de la uveítis va depender de las causas que lo provoquen y del tipo de uveítis que el paciente tenga. Suele durar de tres a cuatro meses . Si el paciente tiene recaídas la duración del tratamiento puede variar.
¿Qué es la uveítis en los ojos?
La uveítis en los ojos es una inflamación de la úvea (capa intermedia de ojo entre la retina y la esclerótica, o lo que es lo mismo, la parte blanca del ojo). Consiste en una inflamación en el interior del ojo que afecta a una o más partes de la úvea: el iris (que da color a los ojos), cuerpo ciliar (detrás del iris donde se produce el humor acuoso) y coroides (parte detrás de la retina).
¿Qué es un glaucoma?
El glaucoma es una neuropatía óptica que deteriora progresivamente el nervio óptico hasta su atrofia total, con asociación de pérdida de campo visual . El principal factor de riesgo es el aumento de la presión intraocular y los daños de fibras retinales.
¿Qué es la iridoclitis?
La iridoclitis es la inflamación del iris (que da color a los ojos) y el cuerpo ciliar (detrás del iris donde se produce el humor acuoso).

Enfermedad
Síndrome de Hellp
¿Qué es el síndrome de Hellp?
El síndrome Hellp es un trastorno relacionado con la preeclampsia (problemas de presión arterial alta durante el embarazo). Se trata de un grupo de síntomas que se presenta en las mujeres embarazas y que se caracterizan por padecer hemólisis (la descomposición de glóbulos rojos), enzimas hepáticas elevada y bajo número de plaquetas.
Es una complicación obstétrica severa, que puede ser difícil de diagnosticar, sobretodo cuando la presión arterial y proteína en la orina no están presentes. Generalmente se desarrolla en las últimas etapas del embarazo (es más común durante el tercer trimestre del embarazo) pero también puede aparecer poco tiempo después del parto.
Este síndrome se presenta en aproximadamente en 1 a 2 de cada 1.000 embarazos. En las mujeres con preeclampsia o eclampsia, la afección se desarrolla en el 10% al 20% de los embarazos. Es un trastorno grave que si no se trata a tiempo y de forma adecuada puede causar la muerte tanto materna como fetal.
Tipos de síndromes más comunes
No hay tipos de síndromes más comunes para esta patología.
Causas del síndrome de Hellp
La causa exacta del síndrome Hellp es desconocida. A pesar de que es más común en las mujeres que tienen preeclampsia o hipertensión inducida por el embarazo (presión arterial alta).
Síntomas del síndrome de Hellp
Los síntomas del síndrome de Hellp en el embarazo pueden ser: hipertensión arterial, fatiga o malestar, retención de líquidos y aumento de peso en exceso, dolor de cabeza, náuseas y vómitos que siguen empeorando, dolor en el cuadrante superior derecho o en la parte media del abdomen y visión borrosa. Más raramente se produce sangrado nasal u otro sangrado que no para fácilmente, crisis epiléptica o convulsiones.
Tratamiento del síndrome de Hellp
El tratamiento para las mujeres con síndrome de Hellp es provocar el parto lo más pronto posible, incluso si es prematuro. Después que el bebé nazca, los síntomas desaparecen.
Durante el embarazo, muchas mujeres que sufren de síndrome de Hellp requieren una transfusión de algún tipo de producto de la sangre (glóbulos rojos, plaquetas, plasma). Los corticosteroides pueden usarse en el embarazo temprano para ayudar a madurar los pulmones del bebé.
Algunos especialistas de la salud también pueden usar ciertos esteroides para mejorar las condiciones de la madre o fármacos para tratar la hipertensión arterial y sulfato de magnesio para evitar las convulsiones.
Pruebas complementarias del síndrome de Hellp
Además del examen físico y la historia clínica completa, los procedimientos para diagnosticar el síndrome Hellp pueden incluir lo siguiente: medición de la presión arterial. análisis de sangre con hemograma, medición de la concentración de lactato deshidrogenasa (enzima catalizadora que se encuentra en muchos tejidos del cuerpo) y la función hepática, análisis de orina para evaluar la cantidad de proteínas y tomografía computarizada que sirve para mostrar sangrado dentro del hígado.
Factores desencadenantes del síndrome de Hellp
No se conoce un factor en específico que pueda desencadenar el síndrome de Hellp
Factores de riesgo del síndrome de Hellp
Los siguientes factores de riesgo pueden aumentar el riesgo de desarrollar el síndrome Hellp: un embarazo anterior con síndrome de Hellp, tener preeclampsia o hipertensión inducida por el embarazo, la edad, embarazo en la adolescencia, grupo étnico caucásico y ser multípara (haber dado a luz dos o más veces).
Complicaciones del síndrome de Hellp
Las complicaciones del síndrome de Hellp son:
Sangrado excesivo (hemorragia).
Edema pulmonar (líquido en los pulmones).
Coagulación intravascular diseminada (CID).
Trastorno de coagulación.
Insuficiencia renal.
Insuficiencia hepática.
Desprendimiento prematuro de placenta.
Prevención del síndrome de Hellp
Desafortunadamente, en la actualidad no hay manera de prevenir este síndrome.
Especialidades a las que pertenece
El síndrome de Hellp pertenece a la especialidad de ginecología y obstetricia . La obstetricia se ocupa de la mujer en todo su periodo fértil (embarazo, parto y puerperio) y la ginecología trata las enfermedades del sistema reproductor femenino (útero, vagina y ovarios). Incluidas glándulas mamarias.
Preguntas frecuentes:
¿Qué secuelas puede dejar el síndrome de Hellp?
Este síndrome puede dejar secuelas debido al embarazo inducido como: edema pulmonar, insuficiencia renal, insuficiencia y hemorragia del hígado y separación de la placenta de la pared uterina (desprendimiento prematuro de placenta).
¿Qué es la preeclampsia?
La preeclampsia es una complicación del embarazo caracterizada por presión arterial alta y signos de daño a otro sistema de órganos, en general, el hígado y los riñones. La preeclampsia suele comenzar después de la 20 semana de embarazo en las mujeres cuya presión arterial ha sido normal.
¿Qué es la eclampsia?
La eclampsia puede aparecer como resultado de la presión arterial elevada y el exceso de proteína en la orina durante el embarazo (preeclampsia). Los síntomas que señalan un mayor riesgo de eclampsia incluyen dolor en la parte superior derecha del abdomen, dolor de cabeza intenso, y cambios en la visión y los estados mentales.
¿Qué es la hemólisis?
Se denomina hemólisis al proceso que se genera cuando los glóbulos rojos se desintegran y la hemoglobina que contenían es liberada en el plasma de la sangre.
¿Qué son las enzimas hepáticas?
Las enzimas hepáticas son las enzimas que produce el hígado . Estas son: fosfatasa alcalina (FA), alanina aminotransferasa (ALT) y aspartato aminotransferasa (AST).
Estas enzimas ayudan al hígado a transformar el alimento en energía. Cuando sus concentraciones son altas, puede ser un signo de que el hígado está lesionado, inflamado o irritado.

Enfermedad
Síndrome Piriforme
¿Qué es el síndrome piriforme?
El síndrome piriforme o síndrome piramidal se refiere a la irritación del nervio ciático cuando pasa por el músculo piramidal, que es un músculo pequeño situado profundamente dentro de la región de la cadera y de la región glútea. Este conecta el sacro (la región más baja de la columna) con el fémur (hueso del muslo). Cuando la cadera está en extensión, su función es de rotador externo, sin embargo, con la articulación de la cadera flexionada, el músculo se convierte en abductor del fémur. Es una afección más frecuente en el campo de la actividad física y el deporte. Afecta más a las mujeres que a los hombres y es poco común.
La mayoría de las personas que tienen el síndrome piriforme mejoran con el tratamiento y los cambios en el estilo de vida. Si no se trata esta afección, puede causar daños permanentes en los nervios.
Tipos de síndromes
No hay más tipos de síndromes comunes asociados al síndrome piriforme .
Causas del síndrome piriforme
El síndrome piriforme está causado predominantemente por un acortamiento o una contractura del músculo piramidal . Esto se traduce en un engrosamiento de sus fibras musculares causando una presión y atrapamiento del nervio ciático y provocando un cuadro clínico de dolor característico del nervio ciático, con irradiación al miembro inferior en el recorrido del mismo .
Las causas que generan este síndrome son:
Sobrecargas por mala práctica deportiva (o errores del entrenamiento), como no respetar el tiempo de descanso, no realizar calentamientos y estiramientos antes de realizar la actividad, secuencialidad de la realización de las actividades físicas, etc.
Escoliosis (columna desviada) o simetría anatómica de los miembros inferiores (pierna más larga que la otra).
Desequilibrio muscular.
Hiperpronación del pie.
Operaciones quirúrgicas en la cadera.
Síntomas del síndrome piriforme
Los síntomas del síndrome piriforme pueden incluir:
Sensibilidad o un dolor breve en el glúteo.
Adormecimiento u hormigueo en el glúteo a lo largo de la parte trasera de la pierna.
Dificultad para sentarse. Dolor al sentarse que empeora si se continúa sentado.
Dolor que empeora con la actividad.
El dolor, usualmente afecta solo a un lado de la parte inferior del cuerpo. Pero también puede ocurrir en ambos lados al mismo tiempo.
Tratamiento del síndrome piriforme
El tratamiento del síndrome piriforme requiere en primer lugar suspender por completo cualquier actividad física que produzca dolor, por lo que tendrá que estar en reposo. En un primer momento se debe aplicar hielo durante 20 a 30 minutos, cada 3 o 4 horas hasta que el dolor vaya desapareciendo. En este caso, siempre que la persona presente dolor, el tratamiento debe de tratar disminuir la tensión del músculo piriforme.
Las sesiones de fisioterapia son una gran opción de tratamiento para disminuir el dolor y la incomodidad , siendo, generalmente, muy eficaces con masajes de descarga. De todos modos, es ideal que el paciente descanse y no fuerce la zona afectada.
El tiempo de recuperación, dependerá de muchos factores como la edad, estado de salud o si ha tenido una lesión piriforme con anterioridad y puede ir de 2 a 6 semanas, según la gravedad de ésta.
Pruebas complementarias del síndrome piriforme
Además de la exploración física de la pierna y columna, las pruebas complementarias para el diagnóstico del síndrome piriforme son, la resonancia magnética y la tomografía axial computarizada (escáner).
Factores desencadenantes del síndrome piriforme
No se conoce un factor en específico que pueda desencadenar el síndrome piriforme .
Factores de riesgo del síndrome piriforme
Entre los factores que aumentan el riesgo de tener el síndrome piriforme están:
Practicar deportes sin hacer un calentamiento y estiramiento adecuado previo.
El sexo suele ser más frecuente en las mujeres que en los hombres.
No utilizar la protección adecuada al realizar algún deporte.
La sobrecarga que genera un exceso de actividad física o abuso de ellas.
Un accidente cerebrovascular .
Alguna lesión traumática.
Escoliosis.
Desequilibrio muscular.
Estar mucho tiempo sentado o en una misma postura.
Complicaciones del síndrome piriforme
Las complicaciones pueden incluir:
Dolor que puede extenderse por semanas.
Se puede encontrar casos en el que el síndrome piriforme aparece y desaparece .
Dificultad para controlar los pies y tropiezos al caminar.
Prevención del síndrome piriforme
Para prevenir el síndrome es necesario:
Practicar ejercicio de manera regular.
Evitar correr o ejercitarse en cuesta o superficies desniveladas.
Hacer calentamiento y estiramiento antes de hacer ejercicio.
No acostarse por períodos prolongados en posiciones que generan más presión en las caderas.
Especialidades a las que pertenece
El síndrome piriforme pertenece a la especialidad de la ortopedia y la traumatología, estas se encargan del diagnóstico, tratamiento, rehabilitación y prevención de lesiones y enfermedades del sistema musculoesquelético del cuerpo humano. Este complejo sistema incluye los huesos, las articulaciones, los ligamentos, los tendones, los músculos.
Preguntas frecuentes
¿Qué es la forma piriforme?
Hace referencia a la forma parecida a la de una pera que tiene el músculo piramidal. Este está situado en la cara posterior del muslo, a nivel inferior del músculo glúteo menor. Tiene su origen en la superficie anterolateral del sacro y su inserción en el borde superior del trocánter mayor del fémur.
¿Cómo es el dolor de ciática?
Se refiere a dolor, debilidad, entumecimiento u hormigueo en la pierna. Es causado por lesión o presión sobre el nervio ciático. La ciática es un síntoma de otro problema de salud. No es una enfermedad por sí sola. La ciática ocurre cuando hay presión o daño al nervio ciático. Este nervio comienza en la región lumbar y baja por la parte posterior de cada pierna. Este nervio controla los músculos de la parte posterior de la rodilla y región inferior de la pierna.
¿Dónde se encuentra el músculo piramidal?
Es un músculo pequeño situado profundamente dentro de la región de la cadera y de la región glútea. Este conecta el sacro (la región más baja de la columna) con el fémur (hueso del muslo). Cuando la cadera está en extensión, su función es rotador externo, sin embargo, con la articulación de la cadera flexionada el músculo se convierte en abductor del fémur.
¿Qué medicamento es bueno para el dolor del nervio ciático?
Los analgésicos como paracetamol o ibuprofeno que son antiinflamatorios no esteroideos (AINES). En algunos casos se utilizan inyecciones o medicación con corticoides.

Enfermedad
Insuficiencia Suprarrenal
¿Qué es la insuficiencia suprarrenal?
Es un trastorno en donde la corteza de las glándulas suprarrenales, no produce suficientes hormonas esteroideas . Este síndrome es provocado por el déficit en la secreción de hormonas de la corteza suprarrenal, sobre todo la disminución de glucocorticoides con o sin deficiencia de mineralocorticoides y andrógenos suprarrenales.
Las glándulas suprarrenales, ubicadas encima de los riñones, producen hormonas esenciales para el funcionamiento del cuerpo. Constan de dos partes. La parte externa, denominada corteza, produce cortisol. Esta es una hormona importante para controlar la presión arterial . La parte interna, denominada médula, produce la hormona adrenalina (también llamada epinefrina). Tanto el cortisol como la adrenalina son liberados en respuesta al estrés. Es una enfermedad grave y, si no se administra el tratamiento oportuno, puede ser mortal.
Tipos de insuficiencias más comunes
Las insuficiencias más comunes incluyen:
Insuficiencia renal: los riñones sanos limpian la sangre eliminando el exceso de líquido, minerales y desechos. También producen hormonas que mantienen sus huesos fuertes y su sangre sana. Pero si los riñones están lesionados, no funcionan correctamente. Pueden acumularse desechos peligrosos en el organismo. Puede elevarse la presión arterial. El cuerpo puede retener el exceso de líquidos y no producir suficientes glóbulos rojos. A esto se le llama insuficiencia renal.
Insuficiencia cardíaca : se produce cuando el músculo del corazón no bombea sangre de forma correcta. Determinadas afecciones, como las arterias estrechadas en el corazón (enfermedad de las arterias coronarias) o la presión arterial alta, dejan progresivamente el corazón demasiado débil o rígido como para llenarse y bombear de forma eficaz.
Insuficiencia respiratoria : sucede cuando no fluye suficiente oxígeno de sus pulmones a su corazón. Sus órganos, como su corazón y cerebro, necesita sangre rica en oxígeno para funcionar correctamente. La insuficiencia respiratoria también puede suceder cuando sus pulmones no pueden eliminar el dióxido de carbono (un gas de desecho) de su sangre. Tener demasiado dióxido de carbono en la sangre puede dañar los órganos.
Causas de la insuficiencia suprarrenal
La causa más común de la insuficiencia suprarrenal primaria o enfermedad de Addison, es una enfermedad autoinmune , lo que significa que el sistema de defensa del cuerpo ataca y destruye los tejidos del propio cuerpo. Cuando se dañan las glándulas suprarrenales, no pueden producir hormonas.
Entre las otras causas de la insuficiencia suprarrenal primaria están el sangrado en las glándulas, infecciones , enfermedades genéticas (heredadas) y extirpación de las glándulas suprarrenales. Los problemas con las glándulas pituitarias causan la insuficiencia suprarrenal secundaria. Normalmente, la glándula pituitaria produce la hormona adrenocorticotrópica , que envía la señal a las glándulas suprarrenales de producir cortisol. Pero con la insuficiencia suprarrenal secundaria, la glándula pituitaria no envía la hormona adrenocorticotrópica a las glándulas suprarrenales. No se produce cortisol. Algunas causas pueden ser temporales, como tomar ciertos medicamentos recetados, como prednisona, hidrocortisona o dexametasona. Otras causas pueden ser permanentes. Incluyen problemas hormonales presentes al nacer, infecciones en la pituitaria, tumores o daño a la pituitaria resultado de cirugía o radiación.
Síntomas de la insuficiencia suprarrenal
Los síntomas de la insuficiencia suprarrenal pueden incluir:
Dolor abdominal o dolor de costado.
Confusión, pérdida del conocimiento o coma.
Deshidratación.
Vértigo o mareo.
Fatiga, debilidad intensa.
Dolor de cabeza.
Fiebre alta.
Pérdida del apetito.
Presión arterial baja.
Náuseas, vómitos.
Frecuencia cardíaca rápida (taquicardia).
Frecuencia respiratoria rápida.
Movimiento lento y aletargado.
Sudoración inusual y excesiva en la cara o las palmas de las manos.
Algunas personas no saben que tienen insuficiencia suprarrenal hasta que sus síntomas empeoran, lo que se denomina una crisis suprarrenal.
Tratamiento de la insuficiencia suprarrenal
El objetivo del tratamiento de la insuficiencia suprarrenal es asegurar el debido nivel hormonal diario. Quizá se necesite un reemplazo hormonal el resto de la vida o tomar glucocorticoides para reemplazar el cortisol que el cuerpo ya no produce.
Es posible que también se necesite mineralocorticoides si el cuerpo no produce aldosterona. Quizá se requiera glucocorticoides adicionales durante momentos de estrés, como una enfermedad u operación.
El médico dará consejos personalizados sobre cambios en los medicamentos durante situaciones estresantes. Comprender la enfermedad y saber cuándo y cómo ajustar los medicamentos puede ayudar a llevar una vida larga y sana con insuficiencia suprarrenal.
Pruebas complementarias de la insuficiencia suprarrenal
Para el diagnóstico, los médicos examinan los síntomas y la historia clínica del paciente.
Revisan por medio de una analítica el nivel de cortisol, otras hormonas, sodio, potasio y glucosa en la sangre para detectar la insuficiencia suprarrenal y ayudar a encontrar la causa. También obtienen imágenes de las glándulas suprarrenales o la glándula pituitaria con rayos X, tomografía computarizada o resonancia magnética.
Factores desencadenantes de la insuficiencia suprarrenal
No se conoce un factor específico que pueda desencadenar la insuficiencia suprarrenal.
Factores de riesgo de la insuficiencia suprarrenal
Un factor de riesgo muy frecuente de insuficiencia suprarrenal ocurre en el caso de aquellas personas que toman corticosteroides para el tratamiento de enfermedades crónicas, como asma o artritis, e interrumpen abruptamente el tratamiento.
Otro factor de riesgo es un daño en la glándula suprarrenal debido, por ejemplo, a la enfermedad de Addison u otra enfermedad de la glándula suprarrenal, y cirugía. La hipófisis está dañada y no puede secretar ACTH (corticotropina) es una hormona polipeptídica, producida por la hipófisis y que estimula a las glándulas suprarrenales.
Complicaciones de la insuficiencia suprarrenal
Las complicaciones están asociadas a otras enfermedades como:
Tiroiditis crónica.
Hipoparatiroidismo.
Hipofunción ovárica o insuficiencia testicular.
Anemia perniciosa.
Hipertiroidismo.
Prevención de la insuficiencia suprarrenal
No existe una forma efectiva de prevenir la insuficiencia suprarrenal.
Especialidades a las que pertenece
La insuficiencia suprarrenal pertenece a la especialidad de endocrinología. La endocrinología es la especialidad médica que estudia las glándulas que producen las hormonas. Estudia los efectos normales de sus secreciones, y los trastornos derivados del mal funcionamiento de las mismas.
Preguntas frecuentes:
¿Cuáles son las glándulas suprarrenales?
Las glándulas suprarrenales están formadas por dos secciones. El interior (médula) y la capa externa (corteza).
¿Qué hacen las glándulas suprarrenales?
Las glándulas suprarrenales se localizan justo en la parte superior de los riñones. Constan de dos partes. La parte externa, denominada corteza, produce cortisol . Esta es una hormona importante para controlar la presión arterial. La parte interna, denominada médula, produce la hormona adrenalina (también llamada epinefrina). Tanto el cortisol como la adrenalina son liberados en respuesta al estrés.
¿Qué es la corteza de las glándulas suprarrenales?
Es la capa externa de la glándula suprarrenal que produce un grupo de hormonas llamadas corticosteroides, que incluyen glucocorticosteroides, hormonas sexuales masculinas (andrógenos) y mineralocorticosteroides.
¿Qué son las hormonas esteroides?
Las hormonas esteroideas son hormonas de crecimiento secretadas por los órganos genitales . Existen muchos tipos, pudiendo agruparlas en cinco categorías: los glucocorticoides, los mineralocorticoides, los andrógenos (la testosterona), los estrógenos y los progestativos (progesterona). Cada hormona esteroidea juega un papel importante en el crecimiento del cuerpo (musculatura, desarrollo de los senos, pilosidad, distribución de las grasas, etc.), el deseo sexual y el humor.
¿Qué tipos de hormonas esteroides segregan las glándulas suprarrenales?
Las glándulas suprarrenales producen hormonas esteroides como:
Cortisol: ayuda al cuerpo a lidiar con el estrés, las enfermedades y lesiones. Regula la glucosa en la sangre y la presión arterial.
Aldosterona: ayuda a mantener el debido equilibrio de sal y agua en el cuerpo. Regula el volumen de sangre y la presión arterial.
Andrógenos suprarrenales: hormonas sexuales masculinas débiles presentes en ambos sexos. Ayuda a regular el crecimiento del vello púbico y axilar en las mujeres.

Enfermedad
Taponamiento Cardíaco
¿Qué es un taponamiento cardíaco?
Un taponamiento cardíaco es la compresión del corazón provocada por acumulo de sangre o líquido en el espacio entre el miocardio (músculo del corazón) y el pericardio (saco exterior que cubre el corazón) y que produce un severo trastorno hemodinámico , a consecuencia de un incremento en la presión intrapericárdica.
Es una urgencia médica ya que impide que el corazón pueda ejercer su función normal de bombeo de la sangre evitando que se llene correctamente, lo que produce una disminución del gasto cardíaco y shock cardiogénico. Ocurre aproximadamente en 2 de cada 10.000 personas. Es una afección grave que debe tratarse de emergencia y de forma adecuada para evitar la muerte de la persona que lo padece.
Tipos de taponamientos cardíacos
No se conocen variantes de esta enfermedad.
Causas de un taponamiento cardíaco
En esta afección, se acumula sangre o líquido dentro del saco que rodea el corazón. Esto impide que los ventrículos se expandan completamente. El exceso de presión del líquido impide que el corazón trabaje normalmente. Como resultado de esto, el cuerpo no recibe suficiente sangre . El taponamiento cardíaco puede ocurrir debido a:
Una aneurisma disecante de la arteria aorta torácica.
Cáncer pulmonar avanzado.
Tumores cardíacos.
Infarto de miocardio agudo.
Cirugía del corazón o procedimientos invasivos.
Fallo cardíaco.
Pericarditis causada por una infección viral o bacteriana.
Traumatismo torácico.
Enfermedades endocrinas, como tiroides hipoactiva.
Insuficiencia renal. Radioterapia del tórax.
Síntomas de un taponamiento cardíaco
Los síntomas de un taponamiento cardíaco pueden incluir:
Ansiedad e inquietud.
Dolor torácico agudo que se siente en el cuello, los hombros, la espalda o el abdomen.
Tensión arterial baja (hipotensión).
Dificultad para respirar.
Desmayos y mareos.
Piel pálida, fría, grisácea o azulada.
Palpitaciones.
Respiración acelerada (taquipnea).
Hinchazón del abdomen u otras áreas.
Pulso débil o ausente.
Pérdida de conocimiento.
Tratamiento de un taponamiento cardíaco
Es importante detectar la causa que ha provocado el taponamiento cardíaco y tratarla. En cualquier caso, el taponamiento cardíaco es una situación de emergencia médica que requiere tratamiento hospitalario urgente para drenar lo antes posible el líquido (sangre o líquido inflamatorio) que se encuentra alrededor del corazón.
Para este drenaje del pericardio se utiliza una aguja, mediante un procedimiento de punción y aspiración que logre extraer el líquido acumulado alrededor del corazón. Este procedimiento se llama pericardiocentesis.
Otra opción de tratamiento que se puede plantear es una operación para extirpar parte de la membrana del pericardio que envuelve el corazón. Este procedimiento se llama pericardiectomía quirúrgica o ventana pericárdica.
Además, se debe administrar tratamiento de soporte y mantenimiento de las funciones vitales. Por ejemplo: aportar oxígeno y líquidos intravenosos que logren mantener la presión arterial y llegada de sangre oxigenada a los tejidos, para mantener a la persona con vida hasta que se haya drenado y resuelto el taponamiento.
Pruebas complementarias de un taponamiento cardíaco
En el diagnóstico del taponamiento cardíaco, además de la historia clínica y exploración física, se realizan estudios con pruebas complementarias de forma urgente, como son:
Análisis de sangre.
Electrocardiograma.
Radiografía de tórax.
Ecografía cardiaca.
Tomografía computarizada (TAC) o resonancia magnética del tórax.
Angiografía coronaria o cateterismo cardíaco.
Factores desencadenantes de un taponamiento cardíaco
No se conoce un factor en específico que pueda desencadenar el taponamiento cardíaco.
Factores de riesgo de un taponamiento cardíaco
Estos factores aumentan la probabilidad de desarrollar esta afección:
Cirugía cardiaca.
Tumores cardíacos.
Infarto del miocardio.
Lesión en el corazón.
Cáncer pulmonar en etapa terminal.
Insuficiencia renal.
Radioterapia en el tórax.
Lupus eritematoso sistémico.
Hipotiroidismo.
Traumatismos torácicos (heridas de arma blanca o traumas cerrados como una contusión).
Complicaciones de un taponamiento cardíaco
Las complicaciones de un taponamiento cardíaco pueden incluir:
Insuficiencia cardíaca.
Edema pulmonar.
Sangrado.
Shock.
Muerte.
Prevención de un taponamiento cardíaco
Muchos de los casos no se pueden prevenir.
Especialidades a las que pertenece
El taponamiento cardíaco pertenece a la especialidad de cardiología . La cardiología es la especialización de la medicina que trata las enfermedades del corazón.
Preguntas frecuentes:
¿Qué es la tríada de Beck y para qué sirve?
La triada de Beck identifica tres características clínicas típicas del taponamiento cardíaco. Estas tres señales clínicas son:
Disminución o apagamiento de los ruidos cardiacos: la gran cantidad de sangre que rodea al corazón, funciona como un aislante por lo que al auscultar puede que se escuchen muy bajos o disminuidos los ruidos cardiacos.
Ingurgitación yugular : al existir una disminución de la contracción del corazón, la sangre se empieza a acumular y se transporta retrógradamente hasta que alcanza las venas yugulares, que se tornan dilatadas por la gran cantidad de sangre que poseen.
Hipotensión arterial: cuando el corazón bombea poca sangre en cada latido, sucede una disminución del gasto cardíaco, por lo que la presión arterial empieza a disminuir. Ocurre tardíamente; es indicativo de shock y mal pronóstico.
¿Qué significa tener líquido en el corazón?
Tener líquido en el espacio del corazón podría ser indicio de pericarditis (inflamación del pericardio), derrame pericárdico o de un taponamiento cardíaco.
¿Qué es un hemopericardio?
Un hemopericardio es la colección de sangre en la cavidad pericárdica. Casi siempre suele ser debida a una lesión cardíaca , con rotura de su pared, bien traumática o tras un infarto de miocardio. Si es de magnitud y rapidez suficiente puede dar lugar a un taponamiento cardíaco.
¿Qué es la pericarditis?
La pericarditis es la inflamación y la irritación del pericardio, la membrana delgada con forma de saco que rodea el corazón. A menudo, la pericarditis causa dolor en el pecho y, a veces, otros síntomas. El dolor agudo en el pecho asociado a la pericarditis se produce cuando las capas irritadas del pericardio se frotan entre sí.
¿Qué es un derrame en el corazón?
Es un derrame pericárdico que consiste en la acumulación de una cantidad excesiva de líquido en la estructura de dos capas, similar a una bolsa, que rodea al corazón (pericardio). Pero si el pericardio está enfermo o lesionado, la inflamación que se produce puede generar un exceso de líquido.

Enfermedad
Chancro Blando
¿Qué es el chancro blando?
El chancro blando o chancroide, es una enfermedad infecciosa de transmisión sexual . Esta enfermedad la produce una bacteria llamada haemophilus ducreyi , y se transmite en las relaciones sexuales con personas infectadas cuando no se utiliza protección.
Produce unas úlceras genitales dolorosas llamadas chancros blandos. Cualquier persona sexualmente activa puede infectarse con chancroide. Es más frecuente en los hombres que en las mujeres, especialmente en los hombres sin circuncisión y también en países tropicales. Es una enfermedad muy común que debe tratarse a tiempo y de forma adecuada para evitar complicaciones más graves.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Tipos de chancro blando
No se conocen variantes de esta enfermedad de transmisión sexual.
Causas del chancro blando
La bacteria que causa el chancro blando o chancroide se llama haemophilus ducreyi . Esta bacteria penetra en una llaga o úlcera abierta (un chancro) próxima a los órganos genitales tanto de hombres como de mujeres. Esta úlcera al sangrar o supurar propaga un fluido que puede contagiar las bacterias durante la práctica sexual (tanto vaginal, como oral o anal).
La bacteria causante del chancro blando también puede diseminarse por contacto directo de piel a piel con una persona infectada.
Síntomas del chancro blando
Los síntomas del chancro blando son muy característicos. La primera señal de infección es, generalmente, la aparición de una o más úlceras o bultos elevados en los órganos genitales.
Las úlceras están rodeadas por un borde rojo delgado que pronto se llena con pus y que en algún momento se rompe dejando una herida abierta que resulta dolorosa. En un plazo de 5 a 10 días de la aparición de las úlceras primarias, las glándulas de un lado (a veces ambos lados) de la ingle se hinchan, endurecen y provocan dolor. Surge una hinchazón redondeada y dolorosa que puede eventualmente reventarse.
Aproximadamente la mitad de los hombres infectados presenta una sola úlcera . Las mujeres a menudo presentan 4 o más úlceras. Estas úlceras aparecen en partes específicas. En las mujeres la ubicación más común es en los labios externos de la vagina (labios mayores). Pueden presentarse «úlceras besadoras» que son úlceras que aparecen en superficies opuestas de los labios genitales.
En los hombres es normal que aparezcan en el prepucio, la cabeza del pene, en el escroto, detrás de la cabeza del pene, etc. En general, los síntomas aparecen entre 4 – 7 días después de la exposición.
Tratamiento del chancro blando
El tratamiento de chancro blando se trata con antibióticos como: azitromicina, ceftriaxona, ciprofloxacino o eritromicina. Las inflamaciones más grandes y de los ganglios linfáticos requieren drenaje , ya sea por aguja o con cirugía local.
Es muy importante tomarse todos los antibióticos de principio a fin, aunque la persona se sienta bien. Si hay infección por el chancro, es importante evitar tocar el área infectada para prevenir el chancro de auto inoculación (re-infectarte tú mismo/a en otra parte del cuerpo).
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Pruebas complementarias del chancro blando
Las pruebas para el diagnosticar el chancro blando es la exploración de las úlceras buscando ganglios linfáticos inflamados y haciendo exámenes para detectar (y descartar) otras enfermedades de transmisión sexual. Se puede realizar un cultivo de la muestra es considerado el método de referencia (gold standard).
Factores desencadenantes del chancro blando
El factor desencadenante es tener un contacto directo o indirecto con la bacteria haemophilus ducreyi , que es la causante del chancro blando.
Factores de riesgo del chancro blando
Entre los factores que aumentan el riesgo de tener la enfermedad chancro blando están: ser sexualmente activo, no utilizar protección durante el acto sexual, no conocer a las parejas sexuales, hombres no circuncidados, transmisión del VIH o no recibir tratamiento para el chancro, entre otros factores.
Complicaciones del chancro blando
Las complicaciones del chancro blando si no se trata son:
Que la transmisión del VIH, sífilis y virus del herpes sea más fácil.
El chancro blando sin tratar suele provocar úlceras en los genitales . A veces, las úlceras persisten durante semanas o meses.
Fístulas uretrales.
Cicatrices en el prepucio del pene.
Prevención del chancro blando
Para prevenir el chancro blando es necesario:
Limitar la cantidad de parejas sexuales.
Utilizar condón siempre que se tenga relaciones sexuales.
Lavar los genitales después de las relaciones sexuales.
Especialidades a las que pertenece
Las especialidades que tratan el chancro blando son la medicina familiar y comunitaria, medicina interna y también la infectología.
Preguntas frecuentes
¿Es contagioso el chancro blando?
Si, el chancro puede ser contagioso. El chancro se transmite de dos maneras: la transmisión sexual a través del contacto piel a piel con una herida abierta o la transmisión por medio de inoculación cuando se hace contacto con el líquido o pus de la úlcera.
¿Qué son las llagas en los genitales?
Las llagas en los genitales son una condición referida a cualquier lesión (úlcera o llagas) que aparecen en los genitales masculinos o femeninos. Las causas se asocian a enfermedades de transmisión sexual (ETS), como herpes, sífilis y el chancro blando y con un factor de riesgo importante para contraer el virus del VIH.
¿Qué es una ETS?
Las ETS o enfermedades de transmisión sexual, son infecciones que se contagian de una persona a otra durante el sexo vaginal, anal u oral. Son muy comunes, y muchas personas que las tienen no presentan síntomas.
¿Cuáles son las ETS más comunes?
Entre las ETS más comunes se encuentran:
VIH : es la más letal de todas las que existen. Este virus destruye la capacidad del cuerpo para defenderse de las infecciones. Se transmite por el contacto con diversos líquidos corporales de personas infectadas, como la sangre, la leche materna, el semen o las secreciones vaginales. Las señales tempranas de la enfermedad incluyen mucha fatiga y fiebre. Si bien no existe cura para el SIDA, hay tratamientos que pueden tenerlo bajo control y hacer más lento su progreso.
Clamidia : es la enfermedad bacteriológica más común. En la mayoría de los casos no manifiesta síntomas. Puede infectar las células del cuello del útero, la uretra, el recto y, a veces, la garganta y los ojos. En las mujeres, los síntomas son flujo abundante, sangrado anormal entre los períodos menstruales o durante el acto sexual, dolor al tener relaciones o al orinar y en la parte baja del abdomen. En los hombres se manifiesta con un líquido blancuzco que sale de la uretra y dolor al orinar o en los testículos.
Herpes genital: es causado por dos tipos de virus. Estos virus se llaman herpes simple del tipo 1 y herpes simple del tipo 2. Los síntomas pueden aparecer mucho tiempo después de haber sido infectados. Una vez que nos hemos contagiado, el virus permanece de por vida. El virus produce unas úlceras alrededor de la vagina y en el pene, aunque la mayoría de las personas que tiene herpes no presenta síntomas o si los presenta son muy leves.
Gonorrea : es una infección bacteriológica que puede infectar la uretra, el cuello del útero, el recto, el ano y la garganta, si se ha practicado sexo oral. El período de incubación, es decir, el tiempo que pasa desde que se entra en contacto con la bacteria hasta la aparición de los síntomas, es de 2-5 días.
Sifilis : se cura fácilmente con antibióticos o penicilina. Puede causar complicaciones a largo plazo o la muerte, si no se trata de manera adecuada. Normalmente, se desarrolla en varias fases y puede manifestarse comenzando por una llaga indolora y pasando después a un sarpullido o síntomas parecidos a los de la gripe.
¿Qué es el granuloma inguinal?
Es una enfermedad de transmisión sexual causada por la bacteria klebsiella granulomatis . La enfermedad se encuentra en á reas tropicales y subtropicales , como el sudeste de India, Guyana y Nueva Guinea. La enfermedad se disemina sobre todo a través de la relación sexual vaginal o anal. En muy raras ocasiones, se propaga durante el sexo oral. Los hombres resultan afectados con una frecuencia de más del doble que las mujeres. La mayoría de las infecciones se presentan en personas entre los 20 y 40 años de edad.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Enfermedad
Conmoción Cerebral
¿Qué es una conmoción cerebral?
Una conmoción cerebral es una alteración del funcionamiento del cerebro , como consecuencia de una lesión traumática en la cabeza o cuando ésta se agita violentamente. Por lo general, los efectos son temporales y consisten en dolores de cabeza y problemas de concentración, memoria, equilibrio y coordinación. El hecho de que sea uno de los accidentes cerebrales más comunes, es por la facilidad con la que puede ocurrir, puesto que cualquier caída, accidente de coche, o cualquier deporte o actividad diaria que impliquen mucho movimiento, convierte a la persona en susceptible de sufrirlo. Es más frecuente en hombres que en mujeres, en adultos jóvenes, niños de menos de 5 años y en personas mayores. Aunque es la forma más leve de los traumatismos craneoencefálicos, si no se trata a tiempo, puede ser grave.
Tipos de conmociones cerebrales
Las conmociones cerebrales se clasifican como leve (grado 1), moderada (grado 2) o grave (grado 3).
Grado 1: los síntomas duran menos de 15 minutos. No hay pérdida de la conciencia.
Grado 2: no existe pérdida de conciencia, pero los síntomas duran más de 15 minutos.
Grado 3 : hay pérdida de conciencia, aunque solo sea por unos pocos segundos.
Causas de una conmoción cerebral
El cerebro está compuesto de tejido blando rodeado de líquido cefalorraquídeo, que actúa a modo de amortiguación, y está localizado dentro del cráneo que es duro y lo protege, pero cuando se sufre un traumatismo craneoencefálico, el cerebro puede moverse dentro del cráneo, lo que puede provocar hematomas, rotura de vasos sanguíneos y lesiones neuronales , produciendo una conmoción cerebral.
Un golpe violento en la cabeza, el cuello o la parte superior del cuerpo puede hacer que el cerebro se mueva abruptamente hacia adelante o hacia atrás contra las paredes internas del cráneo. La aceleración o desaceleración repentina de la cabeza, ocasionada por sucesos como traumatismos, un accidente automovilístico o sacudidas violentas, también puede causar lesiones cerebrales.
Estas lesiones afectan la función cerebral, normalmente por un período breve, y ocasionan signos y síntomas de conmoción cerebral. Este tipo de lesión cerebral puede causar sangrado dentro o alrededor del cerebro, lo que provoca síntomas como somnolencia prolongada y confusión.
Síntomas de una conmoción cerebral
Los síntomas de la conmoción cerebral pueden incluir:
Actuar de manera algo confusa, sentirse incapaz de concentrarse o no pensar con claridad.
Estar somnoliento , difícil de despertar o cambios similares.
Dolor de cabeza.
Pérdida del conocimiento durante un lapso bastante corto.
Pérdida de la memoria ( amnesia ) de hechos ocurridos antes de la lesión o inmediatamente después.
Náuseas y vómitos.
Ver luces centelleantes.
Anormalidades en el sueño.
Cambios en la lucidez mental y la conciencia.
Confusión que no desaparece.
Crisis epiléptica.
Pupilas de los ojos de tamaño diferente.
Movimientos oculares inusuales.
Problemas para caminar o mantener el equilibrio.
Tratamiento de una conmoción cerebral
El descanso es el tratamiento más adecuado para que el cerebro se recupere de una conmoción. El médico recomendará descanso físico y mental para una correcta recuperación de la misma. Esto significa evitar actividades que incrementen cualquiera de los síntomas, como esfuerzos físicos en general, deportes o movimientos vigorosos, hasta que estas actividades ya no provoquen síntomas. También implica limitar actividades que requieran pensar y concentrarse, como jugar a los videojuegos, mirar televisión, hacer tareas escolares, leer o usar el ordenador. El médico puede recomendar acortar la jornada escolar o laboral, que se tomen descansos durante el día o que se reduzcan la carga de tareas escolares o laborales mientras se recupera de la conmoción. A medida que los síntomas mejoran, se pueden ir incorporando gradualmente las actividades. El especialista dirá cuándo es seguro retomar el nivel de vida normal.
Pruebas complementarias de una conmoción cerebral
Para el diagnóstico y tratamiento se llevará a cabo un examen físico y neurológico del paciente. Otras pruebas complementarias que se pueden realizar son: Tomografía computarizada de la cabeza, Resonancia Magnética de la cabeza y Electroencefalograma (EEG, examen de las ondas cerebrales), que puede ser necesario si aparecen crisis epilépticas.
Factores desencadenantes de una conmoción cerebral
Una conmoción cerebral puede desencadenarse de un traumatismo, una caída, actividades deportivas o accidentes automovilísticos.
Factores de riesgo de una conmoción cerebral
Las actividades y los factores que pueden aumentar el riesgo de tener una conmoción cerebral comprenden:
Caídas , especialmente en niños pequeños y adultos mayores.
Participar en deportes de alto riesgo , como fútbol americano, hockey, fútbol, rugby, boxeo y otros deportes de contacto.
Participar en deportes de alto riesgo sin el equipo de seguridad o la supervisión adecuada.
Sufrir un accidente automovilístico.
Ser víctima de maltrato físico.
Haber tenido conmociones cerebrales previas.
Complicaciones de una conmoción cerebral
Las complicaciones de una conmoción cerebral pueden ser:
Dolores de cabeza postraumáticos.
Vértigo postraumático.
Síndrome del segundo impacto.
Síndrome posconmocional.
Prevención de una conmoción cerebral
Para prevenir este trastorno es necesario:
Usar equipos de protección al hacer deporte y otras actividades recreativas.
Usar cinturón de seguridad.
No beber alcohol antes de conducir.
Especialidades a las que pertenece
La conmoción cerebral pertenece a la especialidad de neurología, que es la especialidad médica que se encarga de la anatomía, la fisiología y las enfermedades del sistema nervioso.
Preguntas frecuentes
¿Es lo mismo conmoción que contusión?
Aunque la contusión y conmoción cerebral se producen por golpes en la cabeza y los síntomas son parecidos, hay un par de aspectos que diferencian una de la otra: las contusiones cerebrales son macroscópicas , mientras que las conmociones son microscópicas. Las contusiones cerebrales son más graves , porque tienen desgarros y lesión cerebral estructural.
¿Cuáles pueden ser las consecuencias de un golpe en la cabeza?
Un golpe en la cabeza podría generar una contusión o una conmoción cerebral, que podrían ser relativamente graves en función de la intensidad y de las lesiones que produzca tanto internas como externas.
¿Qué es un traumatismo de cráneo?
Un traumatismo de cráneo o traumatismo craneoencefálico es cualquier alteración física o funcional producida por una fuerza traumática externa que ocasione un daño físico sobre el cerebro o alguna de sus cubiertas.
¿Qué es un trauma de tórax?
El traumatismo torácico es todo aquel golpe fuerte que se produce sobre la caja torácica, pulmones, corazón , grandes vasos intratorácicos y resto de estructuras mediastínicas. Las causas más frecuentes son los accidentes de tráfico y en segundo lugar las caídas.
¿Cuáles son los traumatismos más comunes?
Existen muchos tipos de traumatismos siendo los más comunes:
Traumatismos dentales.
Traumatismos en las extremidades como esguince, luxaciones o fractura.
Traumatismo en el cráneo y la cara.
Traumatismo de los tejidos blandos.
Traumatismo de tórax.
Traumatismo en el abdomen.

Enfermedad
Enfermedad de Von Willebrand
¿Qué es la enfermedad de Von Willebrand?
La enfermedad de Von Willebrand es un trastorno hereditario que afecta la capacidad de la sangre para coagularse adecuadamente, ya que los niveles o el funcionamiento de los factores necesarios para la coagulación son anómalos. Las personas que la padecen tienen problemas con una proteína de su sangre llamada factor Von Willebrand (fvW) que ayuda a controlar las hemorragias. Es el más frecuente de los trastornos de coagulación, aunque es poco común y uno de lo más leves. Se estima que solo el 1% de la población mundial lo padece, con mayor incidencia en las mujeres. La enfermedad de Von Willebrand no tiene cura. Pero con un buen tratamiento y cuidado personal, la mayoría de las personas que padecen esta enfermedad pueden llevar vidas activas.
Tipos de enfermedades de las plaquetas
Los tipos de enfermedades que afectan a las plaquetas son:
Hemofilia: es un trastorno poco frecuente en el que la sangre no coagula de forma normal porque carece de suficientes proteínas coagulantes (factores de coagulación). Si se sufren pequeños cortes se resuelve sin problema. El mayor problema de salud es el s angrado intenso dentro del cuerpo, en especial en las rodillas, los tobillos y los codos. Ese sangrado interno puede dañar los órganos y los tejidos, y puede poner en riesgo la vida. La hemofilia es un trastorno hereditario (genético). El tratamiento comprende el reemplazo regular del factor de coagulación específico que se encuentra disminuido.
Trombocitopenia : consiste en tener menos plaquetas de las normales. Es el problema más frecuente, no obstante, la mayor parte de las veces no tiene repercusión porque, a menudo, aunque tengamos menos plaquetas, éstas son capaces de asegurar una hemostasia correcta (circulación sanguínea normal sin sangrado). Si la cifra de plaquetas es muy baja, el paciente tendrá problemas de cardenales y hemorragias.
Trombocitosis : consiste en tener más plaquetas de las normales. El aumento de la cifra de plaquetas es un mecanismo fisiológico de defensa en caso de inflamación e infección. Por tanto, en estos casos, la cifra de plaquetas puede ser superior a lo normal. Si la cifra de plaquetas está excesivamente alta, se produce un mayor riesgo de trombosis. El ejemplo más claro de este problema se da en una enfermedad de la sangre llamada trombocitemia esencial, en la que el paciente puede tener de 2 a 5 veces las cifras normales de plaquetas.
Trombocitopenia inmune primaria : también llamada Púrpura Trombocitopenia Idiopática. Es una bajada de plaquetas generalmente de causa inmunológica (el cuerpo destruye las propias plaquetas por una alteración de la autoinmunidad). Frecuentemente, la bajada de plaquetas no es grave. Cuando lo es, suele ser necesario un tratamiento con cortisona y, a veces, inmunoglobulinas.
Trombocitemia Esencial: es un tumor benigno de plaquetas que se producen de una manera incontrolada y que, si no se trata, puede conducir a tener trombosis. El tratamiento tiene dos objetivos, uno prevenir la trombosis con dosis pequeñas de aspirina, y en segundo lugar disminuir la cifra de plaquetas cuando ha alcanzado cifras peligrosas, generalmente con hidroxiurea.
Causas de la enfermedad de Von Willebrand
La causa habitual de la enfermedad de Von Willebrand es un gen anormal heredado que controla el factor de Von Willebrand, una proteína que tiene una función clave en la coagulación sanguínea. Esta proteína ayuda a las plaquetas a agregarse o pegarse a las partes dañadas de los vasos sanguíneos. Para que la sangre se pueda coagular, también son necesarias unas proteínas especiales conocidas como factores de coagulación.
El factor Von Willebrand es el transportador de uno de esos factores de coagulación, concretamente el factor VIII. Rara vez, la enfermedad de Von Willebrand puede manifestarse posteriormente en la vida, en personas que no heredaron un gen anormal de ninguno de los padres. Esto se conoce como enfermedad de Von Willebrand adquirida, y probablemente se deba a otra afección.
Síntomas de la enfermedad de Von Willebrand
Los síntomas pueden incluir:
Sangrado menstrual anormal.
Sangrado nasal que no se detiene en menos de 10 minutos.
Sangrado de las encías.
Marcada tendencia a la aparición de moratones.
Hemorragias prolongadas al hacerse cortes, sangrar demasiado o durante demasiado tiempo después de una extracción dental o de someterse a una intervención.
Sangre en la orina o en las heces.
Erupción cutánea.
Tratamiento de la enfermedad de Von Willebrand
Aunque la enfermedad de Von Willebrand es una afección crónica que no tiene cura, el tratamiento puede ayudar a prevenir o a detener los episodios de sangrado. La desmopresina , es la primera opción de tratamiento. Este medicamento está disponible como una inyección o como aerosol nasal. Es una hormona sintética, similar a la hormona natural «vasopresina». Controla el sangrado al estimular el organismo para que libere una mayor cantidad del factor de Von Willebrand que ya está almacenado en el revestimiento de los vasos sanguíneos.
Las terapias de reemplazo , es otra opción de tratamiento, comprenden infusiones de dosis preparadas con factores de coagulación de la sangre concentrados que contienen el factor de Von Willebrand y el factor VIII. Estas terapias pueden ser útiles para todos los tipos de la enfermedad.
Las mujeres, pueden tomar anticonceptivos para controlar el sangrado intenso durante los períodos menstruales. Las hormonas de estrógeno presentes en las píldoras anticonceptivas pueden aumentar los niveles del factor de Von Willebrand y la actividad del factor VIII.
Pruebas complementarias de la enfermedad de Von Willebrand
Debido a que muchas personas con la enfermedad de Von Willebrand tienen signos y síntomas leves, puede que resulte difícil diagnosticar la afección.
Entre las pruebas que se deben realizar están:
Tiempo de sangría.
Tipificación de la sangre.
Nivel del factor VIII.
Análisis de la actividad plaquetaria y recuento de plaquetas.
Prueba de cofactor de ristocetina (evalúa el funcionamiento de la proteína fvW, que interviene en la coagulación de la sangre).
Pruebas específicas para el factor de Von Willebrand.
Factores desencadenantes de la enfermedad de Von Willebrand
El factor desencadenante principal es tener una predisposición genética de la enfermedad de Von Willebrand.
Factores de riesgo de la enfermedad de Von Willebrand
El principal factor de riesgo de la enfermedad de Von Willebrand es tener antecedentes familiares. Un padre puede transmitir el gen anormal que provoca la enfermedad a sus hijos. En la mayoría de los casos, se trata de trastornos hereditarios autosómicos dominantes, lo que significa que solo se necesita un gen anormal de un solo padre para resultar afectado.
Complicaciones de la enfermedad de Von Willebrand
Las complicaciones de la enfermedad de Von Willebrand pueden incluir:
Anemia.
Si se produce un sangrado anormal en las articulaciones o en los tejidos blandos, esto puede provocar hinchazón y dolor intenso.
Muerte por sangrado.
Prevención de la enfermedad de Von Willebrand (listado)
Al ser una enfermedad hereditaria, no existe una forma específica de prevenir la enfermedad de Von Willebrand.
Especialidades a las que pertenece
La enfermedad de Von Willebrand pertenece a la especialidad de hematología. La hematología es la especialidad que se encarga de los elementos inmunológicos de la sangre y las enfermedades que se manifiestan por la alteración de estos elementos; trata también de los órganos que producen la sangre.
Preguntas frecuentes
¿Qué son las plaquetas?
Las plaquetas, también conocidas como trombocitos, son pequeños fragmentos de células sanguíneas . Se forman en la médula ósea, un tejido similar a una esponja en sus huesos. Las plaquetas juegan un papel importante en la coagulación de la sangre.
¿Cuál es el factor Von Willebrand?
El factor Von Willebrand ayuda a las plaquetas a agregarse o pegarse a las partes dañadas de los vasos sanguíneos. Para que la sangre se pueda coagular también son necesarias unas proteínas especiales conocidas como factores de coagulación. El factor Von Willebrand es el transportador de uno de esos factores de coagulación, concretamente el factor VIII.
¿Qué es el factor VIII en la sangre?
El factor VIII es una proteína específica perteneciente a los factores de coagulación que actúan en cascada en el proceso fisiológico de la hemostasia. A diferencia de otros factores de coagulación que se generan en el hígado, el factor VIII y el vWF, que circulan juntos por el organismo, se producen en las paredes de los vasos sanguíneos.
¿Qué es el cofactor de ristocetina?
El cofactor de ristocetina es una técnica cuantitativa para determinar la actividad del factor de Von Willebrand. La prueba de la actividad del factor Von Willebrand (FvW) o del cofactor ristocetina, permite que los médicos evalúen el funcionamiento de la proteína FvW, que interviene en la coagulación de la sangre.
¿Qué es la hemofilia?
Es un trastorno poco frecuente en el que la sangre no coagula de forma normal porque carece de suficientes proteínas coagulantes (factores de coagulación). Puede llegar a provocar un sangrado intenso dentro del cuerpo, en especial en las rodillas, los tobillos y los codos. Ese sangrado interno puede dañar los órganos y los tejidos, y puede poner en riesgo la vida. La hemofilia es un trastorno hereditario (genético). El tratamiento comprende el reemplazo regular del factor de coagulación específico que se encuentra disminuido.

Enfermedad
Enfermedad de Osgood Schlatter
¿Qué es la enfermedad de Osgood Schlatter?
La enfermedad de Osgood Schlatter u osteocondrosis juvenil es un crecimiento doloroso de la protuberancia de la tibia , justo debajo de la rodilla (tuberosidad tibial), que produce una inflamación del hueso, cartílago y/o tendón de la parte superior de esa zona tibial que es el lugar donde se adhiere el tendón de la rótula.
Generalmente, ocurre en niños y adolescentes de 12 a 14 años y en niñas de 10 a 13 años. La diferencia en el rango de edad se debe a que las niñas entran en la pubertad antes que los niños. La enfermedad suele desaparecer sola, una vez que los huesos del niño dejan de crecer. Es más frecuente en los niños que en las niñas pero, como cada vez hay más niñas que hacen deporte, esto está cambiando.
Es la causa más común de dolor en la rodilla en niños, sobre todo atletas adolescentes. Es una enfermedad leve, la mayoría de los casos mejoran espontáneamente después de algunas semanas o meses. Se puede decir que se cura una vez que el niño completa su crecimiento.
Enfermedades de la tibia
Existe otro tipo de enfermedad de la tibia además de la Osgood Schlatter que es la Enfermedad de Blount , también conocido como tibia vara, que consiste en un trastorno del crecimiento que afecta a los huesos de la parte inferior de la pierna, provocando que estos se arquean hacia fuera. Puede afectar a personas en cualquier momento del proceso de crecimiento, pero es más frecuente en niños menores de cuatro años y en adolescentes.
Causas de la enfermedad de Osgood Schlatter
La enfermedad de Osgood-Schlatter se caracteriza por la inflamación del tendón rotuliano y los tejidos blandos que lo rodean. La causa es un continuo tirón que soporta el tendón rotuliano en el área inferior a la rodilla.
Durante las actividades que comprenden correr, saltar y flexionar, como el fútbol, el baloncesto, el voleibol y el ballet, los músculos del muslo (cuádriceps) tiran del tendón que conecta la rótula con el cartílago de crecimiento en la parte superior de la tibia. Esta tensión repetitiva puede ocasionar que el tendón tire del cartílago de crecimiento donde se inserta en la tibia, lo que genera el dolor e inflamación relacionados con la afección.
En algunos casos, el organismo puede intentar cerrar ese hueco con el crecimiento de hueso nuevo, lo que puede formar un bulto óseo en ese lugar.
Síntomas de la enfermedad de Osgood Schlatter
El principal síntoma de la enfermedad de Osgood Schlatter es una hinchazón dolorosa sobre una protuberancia en el hueso de la pierna inferior (tibia). El dolor suele empeorar al realizar ciertas actividades, como correr, arrodillarse y saltar , y se alivia con el reposo. Por lo general, la enfermedad ocurre en una sola rodilla aunque también puede ser en ambas y genera un incremento de la tensión de los músculos que hay alrededor de la rodilla (los isquiotibiales y el cuádriceps). El malestar puede durar entre semanas y meses, y puede volver a aparecer hasta que se deje de crecer.
Tratamiento de la enfermedad de Osgood Schlatter
La enfermedad de Osgood-Schlatter casi siempre se resuelve sin tratamiento. Los síntomas suelen desaparecer cuando se detiene el crecimiento de los huesos. Los analgésicos como paracetamol, ibuprofeno o naproxeno sódico (AINES) pueden ser de ayuda.
Realizar fisioterapia con ejercicios para estirar los cuádriceps, puede ayudar a reducir la tensión en el lugar en donde el tendón de la rótula se une a la tibia.
Una cintilla colocada sobre el tendón rotuliano también puede aliviar la tensión. Los ejercicios de fortalecimiento de los cuádriceps y las piernas en general, pueden ayudar a estabilizar la articulación de la rodilla. En muy pocos casos, si el dolor es debilitante y no disminuye después del período de crecimiento, se puede recomendar cirugía para extirpar la protuberancia ósea.
Pruebas complementarias de la enfermedad de Osgood Schlatter
El diagnóstico de la enfermedad de Osgood Schlatter se realiza mediante una exploración física, donde el médico examinará la rodilla para buscar puntos sensibles, inflamación, dolor y enrojecimiento. Se pueden realizar radiografías para observar los huesos de la rodilla y la pierna y examinar más de cerca la región donde el tendón de la rótula se conecta a la tibia.
Factores desencadenantes de la enfermedad de Osgood Schlatter
No se conoce un factor específico que pueda desencadenar la enfermedad de Osgood Schlatter.
Factores de riesgo de la enfermedad de Osgood Schlatter
Los principales factores de riesgo de la enfermedad de Osgood-Schlatter incluyen:
Edad: la enfermedad ocurre durante los periodos de crecimiento de la pubertad. Los niños de 12 a 14 años y en niñas de 10 a 13 años.
El sexo: es más frecuente en niños.
Deportistas: la enfermedad sucede con más frecuencia en las personas que practican deportes que involucran correr, saltar y hacer cambios de dirección rápidos.
Personas que presentan rigidez de los cuádriceps ya que puede aumentar la tensión que ejerce el tendón de la rótula en el cartílago de crecimiento en la parte superior de la tibia.
Complicaciones de la enfermedad de Osgood Schlatter
Las complicaciones de la enfermedad de Osgood-Schlatter son poco frecuentes. Si ocurren, podrían ser:
Dolor crónico o inflamación localizada.
Bulto óseo en la tibia justo debajo de la rótula, incluso después de solucionar los síntomas. Este bulto puede permanecer, hasta cierto grado, durante toda la vida , pero no suele afectar el funcionamiento de la rodilla.
Rara vez, puede provocar que el cartílago de crecimiento se despegue de la tibia.
Prevención de la enfermedad de Osgood Schlatter
No existe una forma efectiva de prevenir la enfermedad de Osgood Schlatter.
Especialidades a las que pertenece
La enfermedad de Osgood Schlatter pertenece a la especialidad de ortopedia y la traumatología. La ortopedia es una especialidad médica dedicada a corregir o evitar las deformidades o traumas del sistema musculoesquelético del cuerpo humano. La traumatología es la enfermedad que aborda la patología del sistema musculoesquelético.
Preguntas frecuentes
¿Qué es la osteocondrosis?
La osteocondrosis es una enfermedad que afecta a los niños y adolescentes (más a menudo en varones de 4 a 13 años) en fase de crecimiento. Los extremos de los huesos se alargan y amplían el crecimiento de la epífisis y la diáfisis (zonas centrales y de los extremos) de los huesos. En esta etapa se pueden experimentar los fenómenos de necrosis y degeneración de huesos y cartílagos.
¿Qué es la epifisitis?
Es un problema óseo doloroso que se produce por la inflamación (hinchazón) del cartílago de crecimiento del talón. El cartílago de crecimiento, también llamado placa epifisaria, es una zona en el extremo de un hueso en desarrollo donde, con el tiempo, las células de cartílago se convierten en células óseas. Mientras sucede esto, los cartílagos de crecimiento se expanden y se unen entre sí. Es el mecanismo de crecimiento de los huesos.
¿Qué ejercicios se recomiendan para la enfermedad de Osgood Schlatter?
Los ejercicios de estiramiento y fortalecimiento del cuadricep son la mejor opción terapéutica para la enfermedad de Osgood Schlatter.
¿Cuál es la tibia anterior?
El tibial anterior es un músculo que se sitúa en la parte inferior de la pierna y se extiende desde la rodilla hasta el metatarso . Su función es estabilizar el tobillo y permitir la dorsiflexión del pie, es decir, elevar la punta del pie al caminar.
La tibia anterior es la cara delantera de la tibia.
Enfermedad
Síndrome Neuroléptico Maligno
¿Qué es el síndrome neuroléptico maligno?
El síndrome neuroléptico maligno se trata de una afección rara , originada por una respuesta adversa a los efectos de medicamentos neurolépticos, también conocidos como psicofármacos de acción antipsicótica. Son usados, normalmente, en el tratamiento de síntomas psicóticos como alucinaciones y delirios. La incidencia de este síndrome está entre 1 y 5% para aquellos pacientes que consumen este tipo de medicamentos, siendo en los hombres mucho más frecuente que en las mujeres y con mayor predisposición en adultos jóvenes, pero puede aparecer a cualquier edad. Es una enfermedad poco común, pero muy grave, con elevada mortalidad en los casos no tratados de manera precoz.
Tipos de síndromes más comunes
El síndrome neuroléptico maligno no tiene ningún tipo de síndrome más común.
Causas del síndrome neuroléptico maligno
Las causas del síndrome neuroléptico maligno actualmente son desconocidas. Se puede referir que aparece como resultado de una compleja interacción entre fármacos que actúan sobre las vías dopaminérgicas y un sujeto susceptible.
Se cree que el síndrome neuroléptico maligno se debe a un antagonismo sobre los receptores dopaminérgicos en el hipotálamo y el resultado es la rigidez muscular y los temblores extrapiramidales.
Síntomas del síndrome neuroléptico maligno
Los síntomas del síndrome neuroléptico maligno suelen aparecer, aproximadamente, a los 3 días después de que el paciente empiece el tratamiento, pudiendo incluir síntomas como:
Hipertermia (fiebre entre 38º a 40º).
Rigidez muscular.
Alteración del estado mental (confusión, alucinaciones, delirios).
Taquicardia.
Dificultad en el lenguaje.
Hipertensión o hipotensión arterial.
Incontinencia.
Alteración de los reflejos.
Convulsiones generalizadas.
Temblores.
Palidez.
Tratamiento del síndrome neuroléptico maligno
El tratamiento del síndrome neuroléptico maligno se deberá seleccionar en función de la gravedad y el estado del paciente, por lo que cada caso es individual. El primer paso es suspender de forma inmediata el fármaco con acción neuroléptica. También proporcionar las medidas de soportes necesarias como bajar la temperatura corporal , adecuada hidratación, corrección electrolítica, soporte ventilatorio y vigilancias de las complicaciones.
En la mayoría de los casos en los que el síndrome es detectado a tiempo, la intervención de soporte puede ser suficiente para que este remita y poder conducir al paciente a una recuperación sin ningún tipo de secuela.
El tratamiento farmacológico utilizado para tratar el síndrome son los fármacos anticolinérgicos para tratar los síntomas extrapiramidales (Bromocriptina, amantadina). Dantroleno sódico para relajar la musculatura y acabar con la tensión muscular. Benzodiazepinas para reducir la ansiedad y bajar los niveles de agitación. Clozapina para restablecer la medicación neuroléptica. La terapia electroconvulsiva en estudios recientes esta terapia ha reportado mejoría en algunos pacientes con este síndrome. Se cree que su efecto se deba al facilitar la actividad dopaminérgica, se recomienda en casos graves.
Pruebas complementarias del síndrome neuroléptico maligno
Las pruebas complementarias para el diagnóstico del síndrome neuroléptico maligno son :
Realizar una historia clínica completa y examen físico, ya que los síntomas son muy específicos.
Realizar analítica de sangre con hemograma completo, hemocultivos, electrolitos (magnesio y calcio), creatinina quinasa (CPK), prueba de función renal y hepáticas, y pruebas toxicológicas.
Concentración de litio. Medición de hierro. Gases arteriales. Análisis de orina. Estudios de coagulación.
Punción lumbar.
Tomografía axial computarizada.
Resonancia magnética cerebral.
Factores desencadenantes del síndrome neuroléptico maligno
El factor desencadenante del síndrome neuroléptico maligno es el efecto adverso que causa en los pacientes tratados con psicofármacos de acción antipsicótica o neurolépticos.
Factores de riesgo del síndrome neuroléptico maligno
Los factores de riesgo del síndrome neuroléptico maligno son:
Sexo: mayor predisposición en los hombres.
Edad: adultos jóvenes y personas mayores.
Uso de neurolépticos de múltiples psicotrópicos, como varios antipsicóticos al mismo tiempo, uso concomitante de litio.
Alteraciones electrolíticas, deshidratación y deficiencia de hierro.
Enfermedades orgánicas cerebrales: demencia, delirium, epilepsia, Parkinson, parálisis cerebral, enfermedad vascular y retardo mental.
Patología infecciosa de base.
Complicaciones del síndrome neuroléptico maligno
Las complicaciones del síndrome neuroléptico maligno son:
Neumonía aspirativa.
Embolismo pulmonar.
Urosepsis (infecciones urinarias complicadas).
Dificultad respiratoria.
Oxigenación disminuida.
Lisis muscular.
Edema pulmonar.
Paro cardiorrespiratorio.
Trastornos electrolíticos.
Infarto al miocardio.
Convulsiones.
Fallo hepático y renal.
Trombosis venosa.
Prevención del síndrome neuroléptico maligno
La prevención del síndrome neuroléptico maligno incluye:
El paciente deberá tener una buena hidratación para evitar la recurrencia.
Se recomienda comenzar con un neuroléptico atípico a dosis bajas e ir aumentado progresivamente la dosis mientras se monitorizan los signos del síndrome neuroléptico maligno.
Realizar un diagnóstico precoz y tratamiento adecuado para lograr reducir la mortalidad.
Especialidades a las que pertenece
Las especialidades a las que pertenece el síndrome neuroléptico maligno son los médicos de urgencias , neurología medicina intensiva, y también la medicina general y de familia.
Preguntas frecuentes
¿Qué fármacos causan el síndrome neuroléptico maligno?
Los fármacos que pueden causar el síndrome neuroléptico maligno son los neurolépticos atípicos antipsicóticos como, tiapride, sulpiride, clozapina, quetiapina, risperidona y olanzapina, el haloperidol, flufenazina y la clorpromazina.
También existen fármacos antidopaminérgicos usados como antibióticos (metoclopramida) y la retirada brusca de agentes dopaminérgicos usado como antiparkinsonianos (levodopa, bromocriptina).
¿Qué es el síndrome serotoninérgico?
El síndrome serotoninérgico es un síndrome inducido por drogas caracterizado por un conjunto de efectos adversos relacionados a la dosis debido al aumento de su concentración en el sistema nervioso central. La serotonina es un neurotransmisor que produce el cuerpo, y es necesario para el buen funcionamiento del organismo por diversas razones ya que se encarga de regular ciertos procesos fisiológicos, el exceso de serotonina provoca el Síndrome serotoninérgico.
¿Qué es la tríada del síndrome neuroléptico?
La tríada del síndrome neuroléptico es:
Hipertermia (fiebre entre 38.5º a 40º).
Rigidez muscular.
Alteración del estado mental (confusión, alucinaciones, delirios).
¿Cómo puedo prevenir un síndrome neuroléptico?
El síndrome neuroléptico se puede prevenir:
El paciente deberá tener una buena hidratación para evitar la recurrencia.
Se recomienda comenzar con un neuroléptico atípico a dosis bajas e ir aumentado progresivamente la dosis mientras se monitorizan los signos del síndrome neuroléptico maligno.
Realizar un diagnóstico precoz y tratamiento adecuado para lograr reducir la mortalidad.
¿Qué es la epilepsia?
La epilepsia es una enfermedad crónica del sistema nervioso central de etiología diversa que se manifiesta por dos o más crisis convulsivas o paroxísticas espontáneas con sintomatología motora, psíquica, sensorial y sensitiva, debida a la descarga excesiva de las células de la corteza cerebral.

Enfermedad
Entorsis
¿Qué es la entorsis?
La entorsis, también conocida como esguince grado I , consiste en la distensión parcial del ligamento.
No existe laxitud en la articulación por lo que, se pueden realizar movimientos completos, asociados a un dolor leve y variable, y a un ligero proceso inflamatorio . Suele presentar hinchazón y dolor de intensidad variable. Son más frecuentes en personas mayores y en deportistas, aunque puede ocurrir a cualquier persona de cualquier edad y en ambos sexos.
Es una afección muy común y es leve, ya que si se trata adecuadamente puede sanar sin problemas.
Tipos de entorsis
No existen tipos de entorsis.
Causas de la entorsis
Las causas de la entorsis se producen como resultado de un movimiento brusco que excede la capacidad de movimiento de la articulación, por caídas, torceduras o golpes que desplazan la articulación de su posición normal.
Síntomas de la entorsis
Los síntomas de la artrosis son:
Dolor en la zona afectada de intensidad variable.
Inflamación o hinchazón leve y local.
Ligero derrame articular o hematoma.
Tratamiento de la entorsis
Los objetivos del tratamiento de la entorsis son: disminuir el dolor, la inflamación y evitar la inestabilidad crónica de la articulación afectada. La entorsis en la mayoría de las ocasiones se resuelve con medidas conservadoras como son:
Protección, reposo, hielo, compresión y elevación.
La crioterapia , que es la aplicación de frío durante unos 10 minutos cada dos horas durante las primeras 48 horas.
En estos 2-3 primeros días debe evitarse el apoyo de la extremidad y mantener reposo con la extremidad elevada.
La protección y compresión de la articulación se realiza mediante vendajes elásticos o tape, vendaje compresivo, tobillera con cordones u ortesis semirrígida.
Se recomienda realizar ejercicios de rehabilitación para mejorar el movimiento y la fuerza de la articulación.
Los AINEs (analgésicos y antiinflamatorios no esteroideos) han demostrado mejorar el dolor y acelerar la recuperación.
Pruebas complementarias de la entorsis
Las pruebas complementarias de la entorsis son:
La radiografía simple (RX) debe ser siempre la primera imagen a solicitar, pues resolverá la gran mayoría de dudas del examen físico. Es la mejor herramienta para el diagnóstico.
En caso de dudas diagnósticas o del patrón de fractura, se pueden solicitar imágenes complementarias como el TAC, la resonancia magnética o la ecografía.
Factores desencadenantes de la entorsis
No existe factor desencadenante de la entorsis.
Factores de riesgo de la entorsis
Los factores de riesgo de la entorsis son:
La edad: las personas mayores tienen mayor rigidez de la articulación, por lo que cualquier movimiento brusco puede provocar la lesión.
Los deportes intensos : algunas actividades deportivas generan más predisposición a la afectación de las articulaciones, en especial aquellos deportes que requieren saltar, cambiar de dirección rápidamente o estirar o torcer los pies como el baloncesto, tenis, fútbol americano, fútbol, esquí, etc.
Superficies irregulares : caminar o correr en superficies irregulares o en un campo en malas condiciones puede aumentar el riesgo de sufrir un esguince de tobillo.
Lesiones anteriores en la articulación.
Sobrepeso.
Calzados inadecuados.
Traumatismos.
Complicaciones de la entorsis
Las complicaciones de la artrosis son:
Dolor crónico en la articulación afectada.
Inestabilidad crónica.
Artritis articular.
Prevención de la entorsis
Se pueden adoptar algunas precauciones para evitar que ocurra como son:
Realizar un precalentamiento antes de hacer ejercicio o practicar deporte.
Tener cuidado al caminar, correr o trabajar en superficies irregulares o con hoyos.
Mantener una buena fuerza y flexibilidad muscular.
Evitar el sobrepeso .
Utilizar un calzado adecuado para cada actividad que realice.
Evitar los zapatos de tacón.
Asegurarse de que las lesiones anteriores de algún ligamento estén curadas.
Especialidades a las que pertenece
La especialidad médica a la que pertenece la entorsis es la traumatología, que es la que se encarga del estudio, tratamiento y prevención de las lesiones del aparato músculo esquelético.
Preguntas frecuentes
¿Qué es un esguince?
Un esguince es una lesión por rotura o estiramiento que afecta a las estructuras ligamentosas que rodean una articulación.
¿Cuál es la causa de un esguince?
Los esguinces son causados por traumatismo directos , golpes, caídas o por la transmisión de una fuerza que sobrepasa el límite funcional de la articulación. Surgen de movimientos de inversión o eversión y también de rotación excesiva.
¿Qué tipos de esguinces hay?
Hay tres tipos de esguince que son:
Esguince grado I: distensión parcial del ligamento.
Esguince grado II: rotura parcial o total del ligamento.
Esguince grado III: rotura total del ligamento con arrancamiento óseo. La rotura de varios ligamentos puede causar una luxación si se pierde completamente la congruencia articular.
¿Qué es un esguince de primer grado?
Un esguince de primer grado es también llamado entorsis y consiste en distensión parcial del ligamento . Se corresponde con lesiones que no incluyen rotura ni arrancamiento de los ligamentos respecto al hueso. No existe laxitud en la articulación por lo que se pueden realizar movimientos completos. Se asocia un dolor leve, variable y un ligero proceso inflamatorio.
¿Cómo se quita un esguince?
La mayoría de los esguinces se curan en un plazo de 6 a 8 semanas. Las recomendaciones generales para el tratamiento de un esguince leve son: protección, reposo, hielo, compresión y elevación .
En ocasiones es conveniente realizar inmovilización llevando un vendaje o férula. También administrar analgésicos y antiinflamatorios para el dolor y la hinchazón así como hacer ejercicios de rehabilitación para mejorar el movimiento y la fuerza de la articulación.

Enfermedad
Artritis Séptica
¿Qué es la artritis séptica?
La artritis séptica también conocida como artritis bacteriana, es la inflamación de una articulación debido a una infección bacteriana o por hongos.
La infección puede provenir de los gérmenes que se propagan a través del torrente sanguíneo desde otra parte del cuerpo.
La artritis séptica también puede ocurrir cuando, debido a una lesión penetrante, los gérmenes ingresan directamente a la articulación.
Los lactantes tienen más probabilidades de padecer artritis séptica. Las rodillas son las que más frecuentemente se ven afectadas, pero la artritis séptica también puede afectar las caderas, los hombros y otras articulaciones.
La infección puede dañar rápida y gravemente el cartílago y el hueso dentro de la articulación, por lo que es crucial el tratamiento rápido. Puede ocurrir a cualquier edad desde la infancia, pero alrededor de la mitad de los casos ocurre en personas mayores de 60 años. Es una afección común, si no se trata a tiempo y de forma rápida, puede ser grave llegando a producir daños permanentes en las articulaciones.
Tipos de artritis
Entre los tipos de artritis se encuentran:
Osteoartritis : es el tipo más común de artritis. Afecta sobretodo al cartílago común, que es el tejido que amortigua los extremos de huesos dentro de la junta. Una vez que este proceso comienza, el cartílago comienza a erosionar. Esto lleva al dolor común y a la rigidez.
Artritis reumatoide : es una enfermedad inflamatoria autoinmune de la guarnición de la junta, que afecta generalmente a varias juntas al mismo tiempo. Puede afectar a ambas manos y a ambos pies.
Fibromialgia : es un síndrome del dolor que tiene influencias sistémicas. Además, los pacientes experimentan cansancio y adormecimiento de las extremidades.
Artropatía psoriásica: es un fenómeno autoinmune que produce inflamación y dolor de las juntas, los ligamentos, los tendones y la piel. Genera artritis, inflamación del tejido o enthesitis suave y psoriasis.
Gota: es una forma de la artritis causada por el depósito de cristales del urato en la cavidad común de una articulación y alrededor de ella, en los tejidos suaves que producen inflamación y dolor severo. El dedo gordo del pie es el más afectado, pero otras juntas pueden también padecer gota.
Causas de la artritis séptica
La artritis séptica puede deberse a infecciones bacterianas, virales o micóticas . La infección bacteriana por staphylococcus aureus (estafilococo) es la causa más frecuente. El estafilococo vive generalmente en la piel saludable. La artritis séptica puede manifestarse cuando una infección en la piel o en las vías urinarias, se propaga a través del torrente sanguíneo a una articulación.
Con menor frecuencia, una herida punzante, una inyección de medicamento o una cirugía en una articulación o cerca de ésta pueden dejar pasar gérmenes en el espacio de la articulación.
En otros casos, la infección puede entrar directamente en la articulación a través de una lesión en la misma o, en raras ocasiones, durante una cirugía o inyecciones articulares. Una vez que la infección ingresa en la articulación, los leucocitos (células del sistema inmunológico encargadas de eliminar la infección), se agrupan y provocan la inflamación articular.
Síntomas de la artritis séptica
Los síntomas de la artritis séptica difieren dependiendo de la gravedad y el tipo de infección que se trate. Los síntomas pueden incluir: dolor articular (moderado o severo), calor (aumento de la temperatura local), eritema (enrojecimiento) y edema (hinchazón).
Cualquier movimiento de la articulación es extremadamente doloroso. La artritis séptica generalmente provoca malestar extremo y dificultad para utilizar la articulación afectada.
Tratamiento de la artritis séptica
El tratamiento, como la sintomatología, depende del agente infeccioso y otros factores. Si la infección es causada por una bacteria, el tratamiento consiste en dos a cuatro semanas de antibióticos intravenosos, a veces seguidos de una dosis alta de antibióticos orales dependiendo de la respuesta al primer tratamiento.
En aquellos casos más difíciles, el tratamiento pasa por el drenaje frecuente del líquido sinovial o cirugía para retirar el fluido o los tejidos infectados. También se pueden utilizar antiinflamatorios no esteroideos y otros analgésicos para mitigar los síntomas.
El tratamiento también consiste en descansar y proteger la articulación durante la fase aguda. Entablillar la articulación permite limitar el movimiento y ayuda a reducir el dolor y el daño tisular.
Una vez controlada la infección, los doctores a menudo recomiendan terapia física para generar fortaleza muscular y aumentar la amplitud de movimiento en las articulaciones afectadas.
Pruebas complementarias de la artritis séptica
Para el diagnóstico y tratamiento de la artritis séptica es necesario realizar pruebas como: análisis del líquido sinovial ya que las infecciones pueden alterar el color, la consistencia, el volumen y la composición del líquido dentro de las articulaciones, los análisis de laboratorio pueden determinar qué organismo está provocando la infección, el análisis de sangre que determina si hay signos de infección en la sangre, las radiografías y otras pruebas de diagnóstico por imágenes de la articulación afectada pueden ayudar a evaluar el daño.
Factores desencadenantes de la artritis séptica
El factor principal desencadenante de la artritis séptica es un contacto directo o indirecto con una bacteria o un hongo.
Factores de riesgo de la artritis séptica
Los factores de riesgo son: edad avanzada y tener una enfermedad coexistente como diabetes mellitus, enfermedad hepática crónica o cualquier condición en la cual el sistema inmunológico está comprometido.
Las enfermedades y trastornos crónicos que afectan las articulaciones, tales como artrosis, gota, artritis reumatoide o lupus, pueden aumentar el riesgo de artritis séptica.
Las personas con artritis reumatoide tienen un mayor riesgo, ya que los medicamentos que toman pueden suprimir el sistema inmunitario y así aumentar la probabilidad de infecciones.
Las mordeduras de animales, las heridas de punción o cortes en las articulaciones pueden generar riesgo de artritis séptica.
Complicaciones de la artritis séptica
Si el tratamiento se demora, la artritis séptica puede provocar la degeneración de la articulación y un daño permanente.
Prevención de la artritis séptica
Los antibióticos preventivos (profilácticos) pueden ser de gran ayuda para las personas que tienen alto riesgo.
Especialidades a las que pertenece
La artritis séptica pertenece a la especialidad de reumatología, que es la especialidad médica que se encarga de prevenir, diagnosticar y tratar las enfermedades musculoesqueléticas y autoinmunes sistémicas.
Preguntas frecuentes
¿Qué bacteria produce la artritis séptica?
La infección bacteriana por staphylococcus aureus (estafilococo) es una de las bacterias que con mayor frecuencia produce la artritis.
¿Qué es la artritis inflamatoria?
La artritis inflamatoria es un grupo de enfermedades, entre las que se incluyen: la artritis reumatoide, la espondilitis anquilosante, la artritis psoriásica y otras espondiloartritis.
Cuando se presenta artritis inflamatoria el sistema inmunitario, que es el que normalmente combate la infección, ataca las articulaciones.
¿Qué diferencia hay entre artritis y artrosis?
La mayor diferencia entre artritis y artrosis es que la primera puede surgir a partir de otras causas no degenerativas como una infección, un traumatismo o una enfermedad autoinmune. La artrosis u osteoartritis está relacionada con el desgaste y envejecimiento de las articulaciones.
¿Qué es la artritis Piógena?
La artritis piógena o séptica es la inflamación de una articulación debido a una infección bacteriana o micótica . La infección puede provenir de los gérmenes que se propagan en el torrente sanguíneo desde otra parte del cuerpo.
 Savia
Savia