Enfermedades
Enfermedad
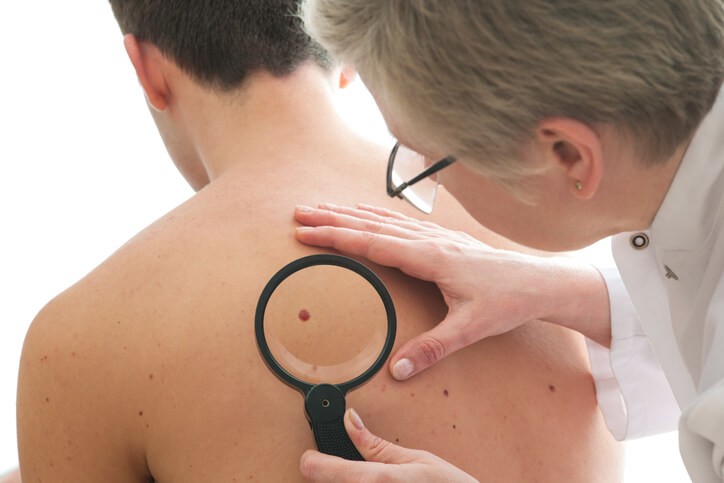
Melanoma
¿Qué es un melanoma?
El melanoma es la tumoración maligna que parte de los melanocitos (las células que dan color a la piel). La mayoría de los melanomas están en la piel , aunque también pueden estar en las mucosas, y un 3% de las personas tiene melanomas ocultos, en cuyo caso solo se ven en las metástasis. También se conoce como nevus maligno, solo representa un 4% de los tumores de piel, pero da lugar al 80% de las muertes por tumores de piel . En España se da en 9 de cada 100.000 personas, siendo más común en las mujeres con una edad de inicio de 55 años, y el más frecuente es el de extensión superficial. Es una enfermedad grave.
Tipos de melanomas
Los tipos de melanomas son:
Melanoma de extensión superficial : es la forma más frecuente, supone el 70% de los melanomas, se da en varones en la zona del torso y en las mujeres es más frecuente en las piernas. La edad media de aparición es de 44 años y suele tener una evolución de uno 5 años antes del diagnóstico.
Melanoma nodular : supone entre 10 y 15% de los casos, crece en 6 a 18 meses, suele tener entre uno y dos centímetros de diámetro, y en el momento del diagnóstico es una lesión negra con el bordado sonrosado.
Lentigo melanoma : lesión pigmentada que se suele dar en personas mayores, en zonas expuestas al sol, generalmente en cara y cuello.
Melanoma lentiginoso acral : es el menos frecuente, suele aparecer en un 2% de los casos y más frecuentemente en personas de raza negra y asiáticos. Se localiza en palmas, las plantas y alrededor de las uñas. Suele aparecer en personas mayores de 65 años.
Causas de un melanoma
Se relaciona con la luz solar , debe haber tres o más quemaduras solares antes de los 20 años con ampollas. La radiación ultravioleta también se relaciona con el melanoma, las camas de rayos UVA dan más radiación ultravioleta que la luz solar.
Síntomas de un melanoma
El diagnóstico del melanoma tiene sobre todo una base clínica que se conoce como ABCD, así, si se dan lesiones asimétricas, de bordes irregulares, coloración heterogénea y diámetro mayor de 6 milímetros , nos deben hacer sospechar de estas lesiones como malignas.
También son síntomas las alteraciones en lesiones previas en su coloración, la presencia de picor , el aumento de tamaño o lesiones satélites, son síntomas para ir al especialista.
Tras la sospecha clínica, se deberá usar la dermatoscopia , ya sea convencional o digital, lo que nos confirmará el diagnóstico.
Por último, la lesión debe ser biopsiada con un margen de tejido sano a su alrededor para confirmar, mediante el examen en un laboratorio de anatomía patológica, el diagnóstico clínico.
Tratamiento para el melanoma
El tratamiento del melanoma tendrá una parte quirúrgica, un tratamiento adyuvante y, por último, un tratamiento de las metástasis, si las hubiera.
El tratamiento quirúrgico ante un melanoma obliga a hacer una extirpación del mismo con un margen de piel sana de unos dos milímetros, y profundidad hasta la fascia muscular. Si se confirma el diagnóstico histológico, puede ser necesario ampliar los bordes de extirpación entre 2 y 5 mm, esto hace que disminuya la posibilidad de recidiva. Los tumores de más de 4 mm de profundidad tienen hasta un 25% de posibilidades de tener metástasis ganglionares, por ello, se procede a retirar el ganglio centinela. En estos casos, para elegir el ganglio a extirpar, se inyecta una sustancia colorante en la zona de la lesión y el primer ganglio que se colorea será extirpado para su estudio histológico.
El tratamiento adyuvante más utilizado es el Interferón alfa a dosis altas de 20.000.000 por metro cuadrado intravenoso durante 5 dias a la semana, durante 4 semanas, seguido de dosis de mantenimiento del mismo fármaco, a mitad de dosis, 3 días a la semana durante 48 semanas, administrados por vía subcutánea. Se debe usar en pacientes con buen estado general y sin comorbilidad importante.
La radioterapia local se usa en caso de márgenes afectados de enfermedad, cuando hay más de cuatro ganglios afectados por la enfermedad, o el ganglio afectado tiene más de 3 centímetros.
El melanoma metastásico es incurable y su tratamiento será paliativo, necesitando una valoración extensa por parte del oncólogo que decidirá la mejor terapia a adoptar.
Pruebas complementarias del tratamiento del melanoma
Biopsias de la lesión con estudio histológico para valorar su profundidad, estudio de ganglio centinela y, en casos de posibilidad de metástasis, estudio con escáner y PET-TAC.
Factores desencadenantes de un melanoma
Los factores desencadenantes de un melanoma son la exposición a radiaciones ultravioletas, sobre todo si producen quemaduras con ampollas en más de tres ocasiones antes de los 20 años.
Factores de riesgo de un melanoma
El factor de riesgo es la exposición solar sin medidas de protección y las cabinas de radiación ultravioleta.
Complicaciones de un melanoma
Las complicaciones más importantes son la metástasis a diferentes partes del cuerpo, siendo al pulmón y al hígado las más frecuentes.
Prevención del melanoma
Evitar cabinas de radiación ultravioleta.
Cremas de protección solar en niños y adolescentes de alta protección.
Evitar el sol en las horas centrales del día.
Especialidades a las que pertenece el melanoma
El melanoma será tratado por el dermatólogo y el oncólogo.
Preguntas frecuentes:
¿Cuáles son los síntomas del cáncer de piel?
Los síntomas del cáncer de piel son le siones en general hiperpigmentadas en la piel con crecimiento rápido, asimétricas, bordes irregulares, de tamaño mayor de 0,5 centímetros y picor. En algunas ocasiones estas lesiones pueden estar ulceradas.
¿Qué es el cáncer de melanoma?
El cáncer de melanoma es la le sión tumoral maligna que se produce por el crecimiento de los melanocitos, que son las células que dan el color a la piel. Su nombre correcto es melanoma maligno.
¿Qué es el lentigo maligno?
El lentigo maligno es una lesión pigmentada, que se suele dar en personas mayores, en zonas expuestas al sol, en general cara y cuello. Es un tipo de cáncer de piel melanocítico, esto es, dependiente de las células que dan coloración a la piel.
¿Qué es el lentigo simple?
El lentigo simple es una lesión benigna de la piel , con hiperpigmentación, en la cual se produce un aumento de melanocitos, pero que no crece ni se extiende a otras zonas del organismo, solo se da en la capa superficial de la piel
¿Qué es el nevus de Becker?
El nevus de Becker es una lesión hiperpigmentada de la piel en la cual se encuentran folículos pilosos . Es más frecuente en varones, se desarrolla en la adolescencia, es un proceso benigno que se trata con láser por razones estéticas.
Enfermedad
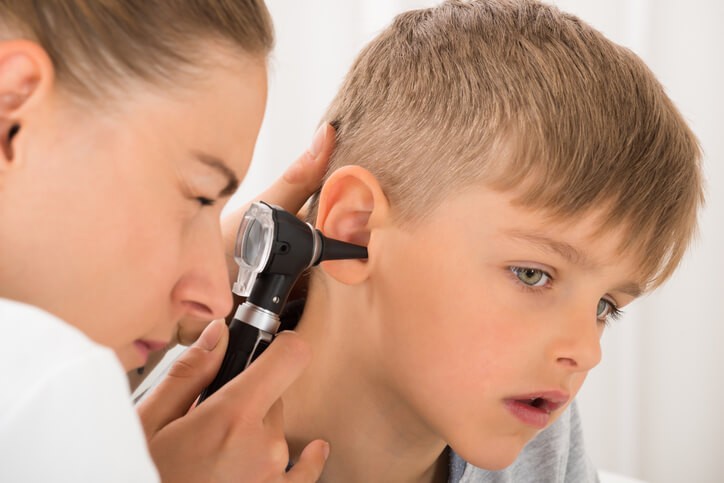
Mastoiditis
¿Qué es la mastoiditis?
La mastoiditis es una in flamación o infección de la apófisis mastoidea o del hueso mastoideo , que es una parte del hueso temporal del cráneo, que se encuentra situado detrás del oído. El hueso mastoideo está compuesto por celdas que drenan el oído medio.
La mastoiditis es generalmente una complicación de una otitis media aguda, donde el hueso se llena de material purulento que puede llegar a destruir su estructura en panal. Es más frecuente en niños entre 2 y 5 años . Antes de la época de los antibióticos, era una de las causas principales de muerte infantil.
En la actualidad es una enfermedad poco común y mucho menos peligrosa, ya que la otitis media se trata muy bien con los antibióticos y no da lugar a que se complique con una mastoiditis, por lo que puede ser una infección leve.
Tipos de mastoiditis
Existen tres estadios en su evolución:
Mastoiditis simple: definida como inflamación de la mucosa, aparece en la mayoría de las otitis media aguda, no se acompaña de signos inflamatorios retroauriculares y no debe considerarse una complicación de la otitis media.
Mastoiditis con afectación al hueso (perióstica): por propagación venosa de la infección del oído medio suele acompañarse de signos inflamatorios retroauriculares característicos, sobre todo a la percusión y palpación del hueso.
Mastoiditis con osteítis: se considera la forma más grave y evolucionada. En este caso se produce la destrucción del hueso trabecular de las celdillas mastoideas con el riesgo de formación de un absceso subperióstico.
Causas de mastoiditis
Las causas de las mastoiditis es una infección del oído medio (otitis media aguda), que generalmente se produce por diferentes bacterias. Esto ocurre cuando la infección del oído medio se propaga hacia el hueso mastoideo. Normalmente una persona con mastoiditis tiene antecedentes de infección de oído recientes o sufre infecciones reiteradas del oído medio. La mayoría de las infecciones mastoideas son causadas por bacterias neumocócicas.
Síntomas de mastoiditis
Los síntomas de la mastoiditis incluyen:
Dolor, enrojecimiento o inflamación detrás de la oreja.
Secreción del oído.
El lóbulo de la oreja sobresale hacia afuera debido a la inflamación del hueso mastoideo. Fiebre, que puede ser alta o incrementarse súbitamente.
Dolor de cabeza.
Irritabilidad o nerviosismo.
Pérdida de audición.
Dolor a la palpación y percusión del hueso.
Borramiento del surco retroauricular.
Desplazamiento del pabellón auricular hacia delante y abajo. Entre otros síntomas.
Tratamiento para la mastoiditis
El tratamiento dependerá de los síntomas, la edad y la salud general del paciente. También variará según la gravedad de la afección. En ocasiones, la afección requiere un tratamiento repetitivo o prolongado. A la mayoría de las personas se les administra inmediatamente un antibiótico por vía intravenosa.
En cambio, a las personas que no estén gravemente enfermas puede administrarse un antibiótico por vía oral durante un periodo de 10-14 días, y administrar analgésico y/o antinflamatorios no esteroideos para el dolor y tratar la fiebre, con una hidratación adecuada. Sin embargo, a veces es necesario recurrir a una cirugía para ayudar a drenar el líquido del oído medio.
En la mayoría de los casos se puede sugerir una miringotomía , procedimiento quirúrgico que consiste en realizar una pequeña abertura en el tímpano para drenar el líquido y aliviar la presión del oído medio. Se coloca un pequeño tubo en la abertura del tímpano para ventilar el oído medio e impedir la acumulación de líquido. Una vez que se drena el líquido, se recupera la audición. Los tubos normalmente se caen por sí solos entre seis y doce meses después de su colocación.
Pruebas complementarias del tratamiento de mastoiditis
Para el diagnóstico y tratamiento de la mastoiditis es necesario realizar pruebas como:
Radiografía de la apófisis mastoidea , en general esta prueba ofrece poca información. Tomografía computarizada del oído,
Tomografía computarizada de la cabeza,
Análisis de sangre , un cultivo del oído infectado, entre otras pruebas.
Factores desencadenantes de mastoiditis
La mastoiditis se desencadena a partir de una infección del oído medio (otitis media aguda).
Factores de riesgo de mastoiditis
Los factores de riesgo de la mastoiditis incluyen : la edad , los niños de 2-5 años son los más propensos a tener este trastorno. La coalescencia , que es una infección persistente aguda en la cavidad mastoidea puede conducir a una osteítis rarificada, que destruye las células que forman trabéculas óseas. Otitis media aguda recurrente. Colesteatoma que es un crecimiento anormal de la piel del oído medio, detrás de la membrana del tímpano. Entre otros factores.
Complicaciones de la mastoiditis
Las complicaciones de la mastoiditis incluyen:
Pérdida de la audición.
Infección grave en tejidos cercanos.
Destrucción del hueso mastoideo.
Parálisis facial (complicaciones intracraneales).
Meningitis.
Problemas en el oído interno.
Absceso en mastoide y tortícolis
Daños en los nervios de la cara.
Mastoiditis crónica.
Osteomielitis del temporal.
Prevención de la mastoiditis
La mejor forma de prevenir la mastoiditis es tratar la infección del oído antes de que se extienda al hueso mastoideo.
Especialidades a las que pertenece la mastoiditis
La mastoiditis pertenece a la especialidad de otorrinolaringología, que es la parte de la medicina que se ocupa del tratamiento y diagnóstico de las enfermedades de la nariz, oído, y boca.
Preguntas frecuentes:
¿Dónde se encuentra la apófisis mastoides?
La apófisis mastoides se localiza en la parte posteroinferior del hueso temporal en el cráneo. El hueso temporal es un hueso par del cráneo y tiene forma irregular.
¿Qué es un colesteatoma de oído?
Es un crecimiento anormal de piel del oído medio detrás de la membrana del tímpano.
¿Qué es el hueso mastoides?
Es un hueso prominente situado justamente detrás del oído, está compuesto por celdillas neumáticas que drenan el oído medio.
¿A quién afecta la mastoiditis?
La mastoiditis afecta en la mayoría de los casos a niños entre los 2 y los 5 años.
¿Cómo se forma el arco cigomático?
El arco cigomático se forma en la unión de la apófisis cigomática del hueso temporal y el hueso cigomático o malar.

Enfermedad
Miositis
¿Qué es la miositis?
La miositis es una inflamación muscular. Sus causas pueden ser variadas, aunque en general son más frecuentes las de naturaleza autoinmune . También se conoce como miopatías inflamatorias idiopáticas y se consideran enfermedades raras dándose uno o dos casos por millón de habitantes al año. Aparecen dos pìcos de edad uno entre los 5 y 14 años y otro entre los 45 y 64 años. Puede afectar al diafragma y los músculos respiratorios dando lugar a una insuficiencia respiratoria. Es una enfermedad grave .
Tipos de miositis
Polimiositis del adulto con afectación de la musculatura estriada.
Miositis por cuerpos de inclusión : Es un trastorno degenerativo, inflamatorio de los músculos que progresa lentamente.
Dermatomiositis: Es una afectación de la musculatura estriada y de la piel en la cual aparecen lesiones, en especial, en zonas articulares de aspecto eritematoso y violáceas en la zona de la cara.
Causas de la miositis
No se conoce la causa exacta de las miositis, se relacionan con p rocesos infecciosos, en los que una base genética interactúa con factores ambientales , como pueden ser las radiaciones solares, que harán más frecuente la enfermedad en las zonas cercanas a los trópicos. Se asocia en muchos casos a neoplasias , por ello ante el diagnóstico de una miositis se deberá de explorar esta posibilidad.
Síntomas de la miositis
Cansancio tras estar parado o tras caminar, tropezar o caerse con facilidad, problemas para tragar o respirar. Los músculos más afectados son la zona de las caderas y los hombros, que producen dificultades para peinarse o levantar la cabeza de la cama. Puede sumarse a ello alteraciones cardíacas como miositis que evoluciona a miocardiopatía dilatada.
Tratamiento para la miositis
El tratamiento serán los c orticoesteroides a altas dosis como la prednisona, en un inicio intravenoso para continuar con terapias orales. Los corticosteroides pueden ser interrumpidos por temporadas volviendo a usarse si fuera necesario ante un nuevo brote de la enfermedad.
Se pueden usar otros fármacos como azatioprina, metotrexato,ciclosporina y ciclofosfamida para ayudar a la inmunomodulación.
La terapia rehabilitadora en piscina puede ayudar a mantener la movilidad articular durante los episodios agudos de enfermedad.
Pruebas complementarias del tratamiento de la miositis
Biopsia muscular: Nos permite atacar las zonas vasculares para diagnosticar la enfermedad. Puede ser negativa, ya que no tiene porqué estar afectado toda la musculatura por eso en algunos casos se considera adecuado realizar previamente.
Resonancia: Nos permite conocer qué músculos tienen mayor afectación, para realizar la biopsia sobre estas zonas.
Analitica de sangre: Se observa elevación de la creatin-quinasa, aldolasa y transaminasas.
Electromiograma: Permite ver la conducción y movilidad muscular alterada.
Al ser una enfermedad en adultos asociada al cáncer, puede ser necesario estudiar la posibilidad de ésta, mediante pruebas complementarias como mamografías, TAC y resonancias magnéticas de diferentes zonas del cuerpo.
Factores desencadenantes de la miositis
No se conocen los factores desencadenantes claros de las miositis, si bien hasta un tercio de los casos se asocia a la presencia de neoplasias , siendo las más frecuentes las de ovario, mama y próstata.
Factores de riesgo de la miositis
No se conocen factores de riesgo para la miositis, aunque la presencia en niños asociadas a épocas de frío hace sospechar, en estos casos, de infecciones previas víricas y en adultos parece sospechar de la exposición a radiaciones ultravioletas , ya que la presencia de la enfermedad es más frecuente en adultos que viven cerca de los trópicos.
Complicaciones de la miositis
Afecciones respiratorias como la neumonitis intersticial.
Afecciones cardíacas o miocarditis que evolucionan a miocardiopatía dilatada.
Afectación digestiva: La disfagia es la más frecuente y la perforación de vísceras en jóvenes, no en pacientes adultos
Prevención de la miositis
No es una enfermedad que se pueda prevenir a día de hoy.
Especialidades a las que pertenece la miositis
La miositis será controlada por un especialista en medicina interna.
Preguntas frecuentes:
¿Qué provoca la inflamación de los músculos?
La inflamación de los músculos se puede producir por un virus, bacterias, por lesiones musculares o por causas autoinmunes. También se puede producir como manifestación paraneoplásica de un tumor en otro lugar del cuerpo.
¿Qué es la distrofia muscular?
La distrofia muscular es un conjunto de e nfermedades hereditarias y progresivas que producen un debilitamiento progresivo de la musculatur a estriada del cuerpo. Esta musculatura es la que se ocupa de los movimientos voluntarios del mismo y del músculo cardíaco. Progresivamente se va produciendo la alteración celular de las células musculares que evolucionan hacia la muerte de las mismas.
¿Qué es la polimiositis?
La polimiositis es una enfermedad inflamatoria crónica autoinmune, que produce daño sobre la musculatura del individuo . Da lugar a una debilidad muscular bilateral simétrica, que suele iniciarse en la cintura escapular y pélvica, con extensión a la parte superior de las piernas y los brazos. Esta debilidad suele ser progresiva.
¿Qué es la dermatomiositis?
La dermatomiositis es una enfermedad inflamatoria crónica, que produce la inflamación de los músculos y la piel. Su causa es desconocida y hasta en un 50% de los casos se asocia a cáncer en los adultos. Produce lesiones características en la piel como son lesiones violáceas en la cara y lesiones eritematosas en las zonas de flexura acompañadas de debilidad muscular.
¿Qué es la dermatomiositis amiopática?
La dermatomiositis amiopática es una dermatomiositis atípica en su presentación, en la cual no se observa en un primer momento daño muscular, aunque las lesiones de la piel son las de la dermatomiositis.

Enfermedad
Mastitis
¿Qué es la mastitis?
La mastitis es la inflamación de la mama , ya sea en una mama lactante también conocida como mama puerperal o en una mama no lactante. Se produce en un 10% de los casos de lactancia , de ellos un 3% puede ser bilateral. La urgencia en este tipo de lesión puede ser el absceso mamario y suele ser una enfermedad leve.
Tipos de mastitis
Mastitis en mama lactante : Cuando la mastitis se produce en una mama que está lactando y es debido a la dilatación de algún conducto de la leche, por la que ésta se queda retenida y puede infectarse.
Matitis en mama no puerperal: Es la mastitis en una mama no lactante y se produce por la entrada de gérmenes en la mama.
Causas de la mastitis
La causa de la mastitis es la entrada de gérmenes en el interior de la mama. Puede ser por:
Pequeñas heridas en la piel: en los casos de mamas no puerperales.
Ectasia de la leche en la mama : Ante la falta de vaciamiento de la mama.
Gérmenes: Que se encuentran en la piel y entran a través de los pezones al amamantar al niño.
Síntomas de la mastitis
Los síntoma de la mastitis son la inflamación de la mama, enrojecimiento, aumento de temperatura, fiebre de más de 38 grados , aumento de la sensibilidad en la misma, que puede acompañarse de malestar general, escalofríos, náuseas y vómitos.
Tratamiento para la mastitis
En los casos de mamas puerperales, puede ser necesario mantener la lactancia. Para ello es conveniente poner calor antes de empezar a dar de mamar, seguido de frío al acabar. También será necesario vaciar la mama si esta no es totalmente vaciada por el niño, además de llevar un sujetador que sujete bien el pecho. Se podrá tomar ibuprofeno como analgésico o antiinflamatorio.
Si el proceso dura más de 48 horas, sea en una mama puerperal o no, será necesario dar tratamiento antibiótico. Los más usados son la cloxacilina o la combinación de amoxicilina con ácido clavulánico.
Pruebas complementarias del tratamiento de la mastitis
El diagnóstico de mastitis es un diagnóstico clínico , que en casos muy excepcionales puede necesitar de un cultivo de la leche . En mamas no puerperales puede cultivarse la secreción que se obtenga.
Cuando el proceso no mejora puede ser necesario realizar una ecografía para descartar otras patologías mamarias asociadas.
Factores desencadenantes de la mastitis
Los factores desencadenantes de la mastitis son la o bstrucción de un conducto mamario . Al obstruirse, se produce un acumulo de leche que da lugar a que se infecte con posterioridad.
Factores de riesgo de la mastitis
Los factores de riesgo de la mastitis son:
Pezones agrietados o dañados.
Lactancia en una sola posición, con lo cual la mama no se vacía de modo correcto.
Presión excesiva sobre el pecho, cansancio o estrés.
En las mamas no puerperales cualquier herida puede hacer de puerta de entrada. Llevar piercing aumenta el riesgo , las mastopatías fibroquísticas pueden favorecer el proceso.
Complicaciones de la mastitis
Absceso mamario.
Sepsis.
Prevención de la mastitis
Extraer la leche completamente tras dar de mamar el bebé.
Intentar que el bebé vacíe de modo correcto la mama antes de cambiarle de pecho.
Cambiar la postura para dar de mamar al bebé.
Procurar colocar al bebé de modo adecuado sobre los pezones para evitar las grietas o maceración de los mismos.
Las mujeres que llevan piercing en los pezones deben de ser extremadamente cuidadosas en el mantenimiento de los mismos.
Especialidades a las que pertenece la mastitis
La mastitis puede ser tratada por el médico de familia, cuando presenta complicaciones se deberá de valorar por el ginecólogo, quien procederá a abrir el absceso y realizará pruebas complementarias si fuera necesario.
Preguntas frecuentes:
¿Qué es la mastitis subclínica?
La mastitis subclínica es aquella en la que se presenta dolor en la mama con pezones macerados o agrietados, pero que no presenta inflamación, ni enrojecimiento local. Tampoco suele tener fiebre asociada, suele ser más difícil de diagnosticar y el uso de antiinflamatorios suele mejorar el proceso.
¿Qué es la mastitis infecciosa?
La mastitis infecciosa es cuando, además de la inflamación por la obstrucción del conducto de la mama, se produce una sobreinfección de la mama que, en general, suele ser por la bacteria estafilococo que se encuentra en la piel de forma normal pero al penetrar en el interior de la mama produce una infección.
Si tengo mastitis… ¿He de dejar de dar el pecho a mi bebé?
La mastitis no debe de ser causa de dejar la lactancia, de hecho el vaciamiento de la mama no solo dificulta la aparición de la mastitis si no que produce una mejoría de la misma. Está indicado en estos casos aplicar calor antes de dar de mamar , esto favorece el vaciamiento de la zona afectada mejorando la dolencia.
¿Se desarrollará peor mi bebé si no le doy el pecho?
El mejor alimento para un bebé es la lactancia materna, ésta no sólo alimenta al bebé sino que le transmite anticuerpos, que son sustancias que le protegen frente a posibles infecciones. Además, la lactancia materna va variando según el momento de desarrollo del bebé.
La lactancia artificial permite alimentar al bebé y dar lugar a un correcto desarrollo del mismo, pero no debe de sustituir a la lactancia natural salvo que sea imprescindible.
¿Qué es un absceso en la mama?
El absceso en la mama es una infección que se encuentra encapsulada . A este tipo de lesiones infecciosas se prescriben antibióticos y, en muchos casos, es necesario que se proceda a un drenaje quirúrgico del mismo para poder extraer el pus que en él se encuentra.
Enfermedad
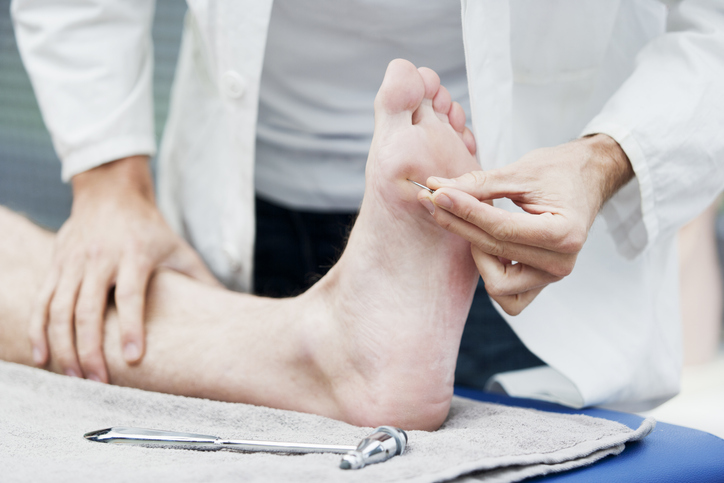
Neuropatía
¿Qué es una neuropatía?
La neuropatía o neuropatía periférica es una enfermedad marcada por una función alterada de los nervios periféricos y que es el resultado de una lesión de los los mismos . A menudo provoca debilidad, entumecimiento o insensibilidad y dolor , por lo general en las manos y en los pies. También puede afectar otras partes del cuerpo.
Los nervios periféricos son una serie de cables que conectan al sistema nervioso central, médula espinal y encéfalo con el resto de las partes del cuerpo y por ellos circula el impulso nervioso. Esto ocurre cuando las células nerviosas, o neuronas, se dañan o se destruyen, lo cual distorsiona la manera en que las neuronas se comunican las unas con las otras así como con el cerebro. La neuropatía puede afectar a un nervio o tipo de nervio, o una combinación de los mismos. Es más frecuente en un 60-80% en personas que sufre de Diabetes mellitus. Puede afectar a todas las edades, aunque las personas mayores tienen mayor riesgo de padecerla y es más común en hombres que en mujeres .
Es una enfermedad muy común, la gravedad va a depender del tipo de lesión nerviosa, y es importante tratarla y controlarla, ya que afecta mucho la calidad de vida de las personas que la padecen.
Tipos de neuropatías
Las neuropatías pueden incluir más de 100 tipos y se pueden clasificar según su forma de comienzo y evolución y según el tipo de lesión nerviosa, entre otros.
Según su comienzo y evolución se clasifican en:
Neuropatía aguda : progresan en 3 semanas como el Síndrome de Guillain- Barré, la polineuropatía diftérica, la polineuropatía porfírica, la amiotrofia neurálgica, y la polineuropatías de las colagenosis. Los síntomas aparecen de repente, progresan rápidamente y mejoran lentamente a medida que los nervios sanan.
Neuropatías crónicas : progresan en más de un mes en forma recurrente o crónicamente progresiva, como la neuropatía diabética, la neuropatía amiloidótica, la neuropatía tóxico nutricional, las neuropatías hereditarias, y la mononeuropatía diabética. Los síntomas comienzan suavemente y progresan lentamente. Algunas personas pueden tener períodos de alivio seguidos de periodos de recaída. Muchas empeoran con el tiempo, pueden ser dolorosas y potencialmente debilitantes.
Según el tipo de lesión nerviosa:
Mononeuropatías simples : compromiso unilateral de troncos nerviosos individuales.
Mononeuropatías múltiples : compromiso de un nervio de una extremidad de un lado y otro de la otra para, de forma indistinta en el tiempo, irse sumando nervios al proceso.
Polineuropatías (PNP) : compromiso bilateral, simétrico, de un nervio de ambas extremidades, es decir, que se ven afectados varios nervios. La neuropatía puede afectar los nervios que suministran la sensibilidad o causan el movimiento. Más frecuente en síndrome de Guillain-Barre, infecciones y toxinas o procesos metabólicos. Es de evolución lenta y supone afección motora y sensitiva. Predominante en casos de enfermedades sensitivas, diabéticas, personas alcohólicas, por cáncer, o por motivos nutricionales.
Mononeuropatías : son algunas formas de neuropatías que involucran daño en un solo nervio situado fuera del cerebro y la médula espinal (neuropatía periférica). Suelen ser de adaptación aguda y tienen causas evidentes, como traumatismo o afección motora y sensitiva en la distribución de una raíz o un nervio periférico aislado, estas pueden ser simples y múltiples.
También algunas neuropatías se deben a daños periféricos se deben:
Degeneración de los axones : los axones son la porción larga y filamentosa de la célula nerviosa. Se suele dar en casos de déficit de vitaminas B12 y E, neuropatías inducidas por drogas, metales pesados y toxinas, neuropatía alcohólica, neuropatía por infección de VIH y neuropatía sensitivomotora hereditaria.
Degeneración de la mielina : la mielina es la proteína grasa que recubre y aísla el axón. Se suele dar en casos de síndrome de Guillain- Barré y de lepra, entre otros.
Degeneración axonal mielínica : es una combinación de lesión axonal y desmielinización. Se suele dar en casos de neuropatía diabética, neuropatía urémica y neuropatías hipotiroidea e hipotiroidea.
Causas de una neuropatía
La causa más común de la neuropatía es la Diabetes mellitus . Los niveles altos de azúcar en la sangre durante un período largo de tiempo pueden causar daño a los nervios. También se pueden ver asociadas a otros trastornos del metabolismo secundario o mal funcionamiento del hígado, riñón o las glándulas tiroideas . Otras causas pueden incluir: traumas o presión en el nervio, consumo excesivo y prolongado de alcohol, trastornos autoinmunitarios como artritis reumatoidea o lupus, enfermedad renal crónica, infecciones como VIH/SIDA, herpes, hepatitis C, niveles bajos de vitamina B1, B6, B12 o de otras vitaminas, intoxicación debido a metales pesados como el plomo, ciertos trastornos hereditarios y el síndrome del túnel carpiano.
Síntomas de una neuropatía
Los síntomas de una neuropatía incluyen: aparición gradual de entumecimiento, cosquilleo u hormigueo en los pies o las manos que pueden extenderse hacia arriba y afectar las piernas y los brazos, dolor intenso, punzante y pulsátil , sensación de congelación o de quemazón, calambres, sensibilidad extrema al tacto, debilidad o parálisis muscular si se ven afectados los nervios motores, pérdida de la coordinación y caídas, cambios de color de la piel, sudoración, contracciones musculares, reflejos nerviosos alterados y dolor a la compresión del tronco nervioso.
Tratamiento para la neuropatía
Los objetivos del tratamiento son controlar la afección que causa la neuropatía y aliviar los síntomas. Los medicamentos son una opción de tratamiento si solo se padecen síntomas ligeros, los analgésicos como los antiinflamatorios no esteroideos ( Ibuprofeno , Naproxeno …etc), pueden ser útiles.
Si las molestias son mayores, hay que acudir a otros medicamentos más potentes. La fisioterapia siempre es un arma útil en el proceso de rehabilitación, pero esta debe ser personalizada. Incluye la estimulación eléctrica de los nervios a través de pequeñas dosis de corriente en la piel a diferentes frecuencias, la realización de ejercicios diseñados para fortalecer los músculos debilitados y técnicas de masajes, entre otras.
Hay pacientes que requerirán el uso de dispositivos de ayuda como aparatos ortopédicos, bastones o férulas , ya que es muy recomendable que las personas con neuropatías protejan las áreas de su cuerpo en las que han perdido sensibilidad, para evitar cualquier complicación como cortaduras y quemaduras.
Se recomienda una mejor nutrición, comer una dieta rica en nutrientes específicos para ayudar a mejorar la neuropatía, como, vitamina B, B1, B12, ácido fólico y antioxidantes.
Para el diagnóstico y tratamiento de la neuropatía es necesario realizar las siguientes pruebas:
Análisis de sangre : estos pueden detectar deficiencias vitamínicas, diabetes, función inmunitaria anormal y otras indicaciones de afecciones que pueden provocar neuropatía periférica.
Pruebas complementarias como tomografía computarizada o resonancia magnética, las cuales permiten detectar hernias de disco, tumores u otras anomalías.
Electromiografía : registra la actividad eléctrica de los músculos para detectar lesiones de los nervios.
Factores desencadenantes de una neuropatía
No se conoce un factor específico que puede desencadenar la neuropatía.
Factores de riesgo de una neuropatía
Los factores que aumentan el riesgo de una neuropatía incluyen: Diabetes mellitus, consumo excesivo de alcohol, deficiencias vitamínicas (particularmente de las vitaminas del grupo B), trastornos renales, hepáticos o tiroideos , enfermedades autoinmunitarias como la artritis reumatoide y el lupus, exposición a toxinas y antecedentes familiares de neuropatía, entre otros factores.
Complicaciones de una neuropatía
Las complicaciones incluyen:
Infección.
Quemaduras, traumatismos y lesiones de la piel.
Caídas, la debilidad y la pérdida de sensibilidad pueden estar asociadas a esta complicación.
Prevención de la neuropatía
La mejor manera de prevenir la neuropatía es:
Controlar las afecciones médicas que ponen en riesgo al paciente como la Diabetes, el alcoholismo o la artritis reumatoide.
Llevar una dieta saludable con adecuado aporte de vitaminas y minerales.
Llevar un estilo de vida más sano y saludable.
Evitar el consumo excesivo de alcohol.
Realizar actividad física de manera regular.
Evitar movimientos repetitivos y posiciones que comprimen los nervios periféricos.
Protegerse y alejarse de las sustancias tóxicas y manipularlas con cuidado y medios de protección.
Especialidades a las que pertenece la neuropatía
La neuropatía pertenece a la especialidad de neurología, que es la parte de la medicina que se ocupa de la anatomía, la fisiología y las enfermedades del sistema nervioso.
Preguntas frecuentes:
¿Qué es la mononeuropatía?
Una mononeuropatía es la que ocurre cuando es un solo nervio el que está dañado , situado fuera del cerebro y la médula espinal (neuropatía periférica). Suelen ser de adaptacion aguda, tienen causas evidentes como traumatismo y afección motora y sensitiva en la distribución de una raíz o un nervio periférico aislado. Estas pueden ser simples y múltiples.
¿Cuál es la neuropatía más frecuente?
La neuropatía periférica, asociada a la Diabetes mellitus es la forma más frecuente de neuropatía.
¿Qué es la polineuropatía?
Una polineuropatía se refiere a que muchos nervios en diferentes partes del cuerpo están comprometidos. La neuropatía puede afectar los nervios que suministran la sensibilidad o causan el movimiento.
¿Qué es la neuropatía desmielinizante?
La neuropatía desmielinizante es un trastorno neurológico caracterizado por debilidad progresiva y función sensorial alterada en las piernas y los brazos . El trastorno, que en ocasiones se denomina polineuropatía crónica recurrente, es causado por daño en la vaina de la mielina (la cubierta grasa que cubre y protege las fibras nerviosas) de los nervios periféricos.
¿Qué es la neuropatía idiopática?
Una neuropatía idiopática es un trastorno neurológico en el sistema nervioso periférico de causa desconocida.

Enfermedad
Orquitis
¿Qué es la orquitis?
La orquitis es la inflamación de los testículos . Éstos son las gónadas masculinas responsables de la producción de espermatozoide y hormonas sexuales masculinas. En la mayoría de los casos, las causas que la producen son las infecciones por virus o bacterias a nivel del epidídimo o del propio testículo, y en otras ocasiones por traumatismos.
Es más frecuente que se desarrolle en un solo testículo, aunque en raras ocasiones puede aparecer en ambos (bilateral). La incidencia demuestra que un 20% aproximadamente de todos los casos de paperas aparecidas después de la pubertad van acompañados de una inflamación de los testículos (orquitis).
De los producidos por virus, el más frecuente es el que produce las paperas y es más común en menores de 10 años. Sólo un 30% puede desarrollar orquitis en los hombres . Además, la tasa por orquitis producida por transmisión sexual es más alta en los hombres de entre 19-35 años. Es una enfermedad común, es leve, y en la mayoría de los casos mejora sin problemas, si se trata adecuadamente se evitan complicaciones importantes.
Tipos de orquitis
La orquitis se clasifica en dos fases que son, orquitis aguda y crónica.
La orquitis aguda: Es la que produce un aumento de tamaño testicular debido a la inflamación aguda, acompañado de una subida de temperatura (tumefacción) y mucho dolor.
La orquitis crónica: Es cuando el dolor persiste más de 6 semanas, el testículo está menos inflamado y la subida de temperatura (tumefacción) desaparece, se pega al escroto, se vuelve fibroso y se endurece, lo que es llamado atrofia testicular.
Causas de la orquitis
La orquitis puede ser causada por una infección de diferentes bacterias y virus, siendo este último el más frecuente. Entre los virus que con más frecuencia pueden producir la orquitis se encuentra el virus de las paperas que produce una parotiditis (inflamación de las glándulas parótidas) y que se desarrollan en una semana aproximadamente después del comienzo de las paperas.
La orquitis también puede aparecer en infecciones de próstata debido a una infección de transmisión sexual (ETS). Las más comunes son las bacterias que causan gonorrea o clamidia. Las infecciones de orina recurrentes pueden extenderse al tracto urinario hasta llegar al testículo. La bacteria más común en este caso es la escherichia coli.
La infecciones de la próstata y el epidídimo pueden extenderse hacia el testículo y producir la alteración que se conoce como orquiepididimitis (cuando la infección afecta al testículo y al epidídimo). La introducción de sondas o instrumentos médicos en el pene, puede dar lugar a una orquitis traumática.
Síntomas de la orquitis
Los síntomas de la orquitis son:
Dolor en el testículo.
Inflamación en el escroto.
Fiebre.
Sangre en el semen.
Dolor inguinal.
Dolor al orinar (disuria).
Secreción en el pene.
Dolor en las relaciones sexuales, sensibilidad y sensación de pesadez en el testículo afectado.
Piel que recubre el escroto enrojecida y caliente.
Náuseas.
Parotiditis (inflamación de las glándulas salivales parótida).
Tratamiento para la orquitis
El tratamiento para la orquitis va depender de la causa originaria. Las medidas generales son, guardar reposo en cama, mantener el testículo en alto y aplicar frío.
Tomar antiinflamatorios y analgésicos no esteroideos como ibuprofeno y paracetamol, para aliviar el dolor.
Si la orquitis es producida por una infección bacteriana se deberá usar antibióticos.
En caso de que sea por una enfermedad de transmisión sexual (gonorrea o clamidia) la pareja sexual también debe recibir tratamiento.
Pruebas complementarias del tratamiento de la orquitis
Las pruebas diagnósticas y complementarias para la orquitis son: realizar la palpación del testículo , donde se va a detectar la presencia de dolor, enrojecimiento, inflamación, asimetría escrotal (un testiculo mas grande que otro), agrandamiento y sensibilidad del testículo.
Las pruebas complementarias que se deben realizar son, un análisis de sangre y orina para identificar el virus de la paperas y otras infecciones. Exámenes para detectar la enfermedad de transmisión sexual.
Una ecografía testicular o ecografía doppler, que es una prueba por imagen que determina con seguridad el diagnóstico de la orquitis y se usa para evaluar el flujo sanguíneo y descartar una torsión testicular.
Factores desencadenantes de la orquitis
No existen factores desencadenantes de la orquitis.
Factores de riesgo de la orquitis
Los factores de riesgo de la orquitis son:
Tener más de 45 años.
No estar vacunado contra la paperas.
Infección de orina de manera regular.
Anomalías congénitas de las vías urinaria.
Cirugía genito-urinaria.
Uso prolongado de sonda de Foley (drenaje y recolección de la orina de la vejiga).
Sufrir orquitis por una transmisión sexual, es más frecuente en hombres con una edad comprendida de 19-35 años.
En este caso, tiene otros factores más directos como son: múltiples parejas sexuales, personas con antecedentes de gonorrea u otra enfermedad de transmisión sexual (ETS), tener pareja con infección por transmisión sexual diagnosticada y no usar protección (preservativos).
Complicaciones de la orquitis
Las complicaciones de la orquitis pueden ser:
Inflamación crónica del epidídimo (epididimitis).
Abscesos escrotales (acumulacion de secresion en el escroto).
Atrofia testicular (el testículo afectado se encoge).
Infertilidad.
Cáncer testicular.
Prevención de la orquitis
La prevención de la orquitis consiste en:
Vacunarse contra la paperas.
Usar preservativo al tener relaciones sexuales para disminuir el riesgo de sufrir una infección por transmisión sexual.
Especialidades a las que pertenece la orquitis
La especialidad a la que pertenece la orquitis es la urología, que es una especialidad que se ocupa de la prevención, diagnóstico y tratamiento de las enfermedades renales y del aparato urinario.
Preguntas frecuentes:
¿Qué son las paperas?
Las paperas son una enfermedad viral aguda y contagiosa que causa una inflamación dolorosa en las glándulas salivales llamada parotiditis.
¿Qué relación tiene la orquitis por paperas?
La relación que tiene la orquitis con las paperas es que el virus de las paperas es la causa más frecuente de la orquitis, el testículo se inflama y duele.
¿Cuánto dura la orquitis por paperas?
La orquitis por paperas puede durar 7- 10 días aproximadamente, después de la inflamación de la parótida (parotiditis).
¿Qué es la orquitis urliana?
La orquitis urliana es un proceso inflamatorio de los testículos producido por el virus de la parotiditis.
¿Qué es la torsión testicular?
La torsión testicular ocurre cuando un testículo gira, retorciendo el cordón espermático que lleva sangre al escroto . La reducción del flujo sanguíneo causa dolor e hinchazón repentina y aguda. Es una urgencia médica que generalmente requiere cirugía inmediata para poder salvar el testículo.
Enfermedad
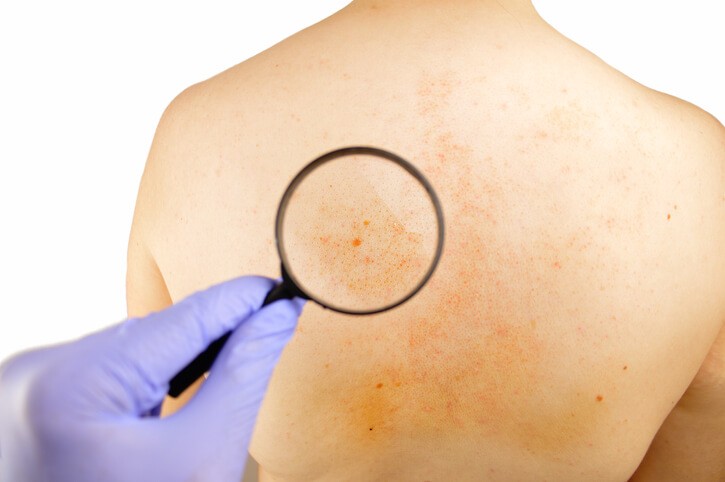
Neurofibromatosis
¿Qué es la neurofibromatosis?
La neurofibromatosis es un conjunto de trastornos genéticos neurocutáneos (con manifestaciones neurológicas y cutáneas), que afecta la manera en que las células crecen y se forman, lo que hace que se formen tumores en el tejido del nervio. Estos tumores pueden desarrollarse en cualquier lugar del sistema nervioso, ya sea el cerebro, la médula espinal, o los nervios, y también en tejido no nervioso como huesos y piel. En general, los tumores son mayormente benignos (no cancerosos), pero a veces pueden convertirse en cáncer (malignos). Estos tumores pueden crecer en cualquier lugar del interior o de la superficie del organismo. Son enfermedades multisistémicas progresivas, hereditarias, raras o poco comunes. Puede desarrollarse en todo el mundo y no existen diferencias de sexo o de grupo racial. La neurofibromatosis se puede heredar de los padres o puede ocurrir por una mutación (cambio) en los genes.
Tipos de neurofibromatosis
Existen 3 tipos de neurofibromatosis, estos son:
Neurofibromatosis tipo 1: también conocida como enfermedad de Von Recklinghausen. Es el tipo de neurofibromatosis más común, aparece en la infancia y está causada por una anomalía en un gen en el cromosoma 17. Los signos suelen ser evidentes en el momento del nacimiento o poco después, y casi siempre antes de los 10 años. Estos son: manchas cutáneas sin relieve de color marrón claro o de color café con leche, pequeños bultos en el iris del ojo, los cuales son nódulos inofensivos no se pueden ver fácilmente y no afectan la visión, bultos suaves sobre la piel o debajo de ella o deformidades óseas, entre otros.
Neurofibromatosis tipo 2: también se denomina neurofibromatosis acústica bilateral. Es mucho menos frecuente que la neurofibromatosis tipo 1. Causada por una mutación en un gen localizado en el cromosoma 22, se presenta típicamente en la adolescencia o en la adultez temprana. Los signos y síntomas de la neurofibromatosis tipo 2 aparecen, por lo general, como resultado del desarrollo de tumores benignos que crecen lentamente (neurinoma del acústico) en los dos oídos.
Schwannomatosis: es un tipo bastante raro de neurofibromatosis, normalmente, afecta a las personas después de los 20 años. La schwannomatosis provoca la formación de tumores en los nervios del cuero cabelludo (craneales), espinales y periféricos, pero no en el nervio que transporta la información de sonido y equilibrio desde el oído interno hasta el cerebro.
Causas de la neurofibromatosis
La neurofibromatosis se produce por d efectos genéticos (mutaciones) que transmiten los padres , o se producen espontáneamente en la concepción. En la neurofibromatosis tipo 1, el cromosoma alterado es el 17, mientras que el cromosoma 22 es el responsable de la neurofibromatosis de tipo 2.
Síntomas de la neurofibromatosis
Los síntomas de la neurofibromatosis incluyen: manchas cutáneas sin relieve de color marrón claro, pecas en la zona de las axilas y la ingle, pequeños bultos en el iris del ojo (nódulos de Lisch), bultos suaves sobre la piel o debajo de ella , deformidades óseas, tamaño de la cabeza superior al promedio, pérdida de la audición gradual, zumbido en los oídos, equilibrio deficiente, dolores de cabeza, entumecimiento o debilidad en diversas partes del cuerpo y pérdida muscular.
Tratamiento para la neurofibromatosis
La neurofibromatosis no tiene cura, pero los signos y síntomas se pueden tratar. El tratamiento médico puede incluir: cirugía para quitar los tumores que causan dolor u otros problemas. Cuando la cirugía no es posible, se aconseja hacer seguimiento continuo y control del dolor.
Otras opciones de tratamiento son la radiación o quimioterapia para los tumores que se convierten en cáncer o que causan otros problemas, colocación de audífonos o implante auditivo de tronco encefálico para adolescentes y adultos que tienen neurofibromatosis tipo 2 con pérdida auditiva, y a quienes se les quitó parte del nervio auditivo.
Pruebas complementarias del tratamiento de la neurofibromatosis
Para el diagnóstico y tratamiento de la neurofibromatosis se necesitan pruebas como: examen ocular, examen de oído, radiografías, tomografías computarizadas y resonancias magnéticas , que pueden ayudar a identificar anomalías óseas, tumores en el cerebro y la médula espinal, y tumores muy pequeños. También se pueden realizar análisis genéticos entre otras pruebas.
Factores de riesgo de la neurofibromatosis
El factor de riesgo más importante de la neurofibromatosis es tener antecedentes familiares del trastorno. Aproximadamente la mitad de las personas con neurofibromatosis tipo 1 y tipo 2 heredaron la enfermedad. Cuando la neurofibromatosis tipo 1 y la neurofibromatosis tipo 2 no son heredadas, ocurren por nuevas mutaciones genéticas.
El patrón hereditario en el caso de la Schwannomatosis no es tan claro. Actualmente, los investigadores calculan que el riesgo de heredar Schwannomatosis de un padre afectado es de alrededor del 15%.
Complicaciones de la neurofibromatosis
Las complicaciones de la neurofibromatosis incluyen:
Problemas neurológicos.
Problemas respiratorios.
Cáncer.
Sordera parcial o total.
Lesión al nervio facial.
Múltiples tumores cerebrales benignos o tumores de la columna vertebral que requieren cirugías frecuentes.
Debilidad o entumecimiento en las extremidades.
Prevención de la neurofibromatosis
No se conocen formas específicas de prevenir esta afección, pero sí se recomiendan ciertos consejos genéticos a las personas con antecedentes familiares de este trastorno.
Especialidades a las que pertenece la neurofibromatosis
Las especialidades que afectan la neurofibromatosis forman un equipo multidisciplinar, ya que esta puede desarrollarse en diferentes partes del cuerpo. Estas son: neurología, neurocirugía, dermatología, genética, oftalmología, ortopedia, psicología y rehabilitación.
Preguntas frecuentes:
¿Cómo se hereda la neurofibromatosis?
La neurofibromatosis se hereda de forma autosómica dominante . Es decir, que, para tener la enfermedad, se necesita solo un cambio (mutación) en una copia del gen responsable de cada célula. Una persona afectada hereda la mutación de un padre afectado. Lo que quiere decir que se hereda de padres a hijos.
¿A qué cromosoma afecta la neurofibromatosis?
En la neurofibromatosis tipo 1, el cromosoma alterado es el 17, mientras que el cromosoma 22 es el responsable de la neurofibromatosis de tipo 2.
¿Qué son los nódulos de Lynch?
Los nódulos de Lynch son pequeños bultos en el iris del ojo . Estos nódulos inofensivos no se pueden ver fácilmente y no afectan la visión.
¿Qué es la esclerosis tuberosa?
La esclerosis tuberosa es un trastorno genético poco frecuente que hace que se formen tumores no cancerosos o benignos con crecimientos excesivos e imprevistos de tejido normal en muchas partes del cuerpo.
¿Qué es la enfermedad de Von Hippel Lindau?
La enfermedad de Von Hippel-Lindau (VHL) es una enfermedad rara que causa tumores y quistes en el cuerpo . Pueden crecer en el cerebro y en la médula espinal, en los riñones, en el páncreas, en las glándulas suprarrenales y en el tracto reproductivo. En general, los tumores son benignos o no cancerosos.

Enfermedad
Mononucleosis
¿Qué es la mononucleosis?
La mononucleosis o enfermedad del beso es una enfermedad infecciosa de origen vírico, producida por el virus de Epstein-Barr. La mayor incidencia es en adolescentes, y alrededor del 95% de los adultos de entre 35 y 40 años han sido infectados. El virus se transmite a través de la saliva , puede precisar asistencia de urgencia si se da un gran aumento del bazo o se presenta el síndrome de Guillain Barré. Es una enfermedad de tipo leve.
Tipos de mononucleosis
La mononucleosis es una enfermedad infecciosa que puede presentarse en forma poco sintomática en niños, o bien presentar más síntomas, pero esto es más típico de adultos. No existen distintos tipos de mononucleosis, solo diferencia de gravedad en los síntomas.
Causas de la mononucleosis
La mononucleosis tiene como causa la infección por el virus de Epstein Barr. Este virus se contagia por contacto con saliva de un paciente infectado.
Síntomas de la mononucleosis
Los síntomas de la mononucleosis son: fiebre, malestar general, dolor muscular, amígdalas aumentadas de tamaño con secreciones pegadas a las mismas, adenopatías cervicales y aumento del bazo.
Tratamiento para la mononucleosis
La mononucleosis no tiene tratamiento para la infección, será necesario tratamiento sintomático con analgésicos, reposo y líquidos abundantes , así como evitar los deportes de contacto.
Pruebas complementarias del tratamiento de la mononucleosis
Se harán analíticas de sangre en las que se busca presencia de glóbulos blancos más altos de lo normal, con presencia de linfocitos atípicos, anticuerpo frente al virus de Epstein Barr.
Factores desencadenantes de la mononucleosis
El factor desencadenante es la infección con virus de Epstein Barr.
Factores de riesgo de la mononucleosis
El factor de riesgo central de la mononucleosis es el contacto con saliva de pacientes enfermos , ya sea mediante besos o por contacto con vasos o cubiertos de la persona enferma.
Complicaciones de la mononucleosis
Síndrome de Guillain Barré.
Convulsiones.
Anemia.
Hepatitis con ictericia.
Aumento y rotura del bazo.
Erupción cutánea.
Prevención de la mononucleosis
No compartir vasos o cubiertos de personas enfermas.
No besar a personas enfermas.
Especialidades a las que pertenece la mononucleosis
El especialista que controla la mononucleosis es el médico de familia, pero en caso de complicaciones, puede ser necesario el control por un médico de medicina interna o de la especialidad de neurología.
Preguntas frecuentes:
¿Cómo se contagia la mononucleosis?
La mononucleosis se contagia a través del contacto con saliva de las personas infectadas, ya sea por besos o por compartir vasos o cubiertos. En casos excepcionales se puede contagiar por trasplante de médula ósea.
¿Por qué se inflama el bazo?
En la mononucleosis se produce una esplenomegalia inmune, esto se da como reacción a la infección por el virus de Epstein-Barr.
¿Cuál es la función del bazo?
El bazo tiene un a función inmunológica, produciendo sustancias que tratan de dañar a las bacterias y virus infecciosos, pero también actúa como sistema de filtro de la sangre eliminando células sanguíneas anormales, o aquellas que se deben eliminar por su envejecimiento.
¿Qué es la esplenomegalia?
La esplenomegalia es aumento del tamaño del bazo por encima de lo normal, eso se puede producir por enfermedades infecciosas como la mononucleosis, o inflamatorias, como la artritis reumatoide.
¿Cómo se llama la operación del bazo?
La operación del bazo se conoce como esplenectomía , y en ella se procede a retirar el bazo. Puede ser consecuencia de un traumatismo en el cual se rompe, siendo necesaria su extirpación para controlar el sangrado, o bien en casos de secuestro de células sanguíneas, en el cual el bazo procede a mantener en su interior células como las plaquetas, alterando la función de ellas y siendo necesario extirparlo. La esplenectomía no lleva consigo más riesgos que el poder tener más infecciones, por ello, tras la esplenectomía, le recomiendan al paciente que se vacuna de neumonía y gripe.

Enfermedad
Molusco Contagioso
¿Qué es el molusco contagioso?
El molusco contagioso también conocido como molluscum contagiosum , es una enfermedad infecciosa producida por un virus conocido como poxvirus , que produce pápulas en la piel de menos de 5 mm.
Es una enfermedad que se da con mucha frecuencia en climas fríos, se transmite a niños de 8 a 12 años y tiene mucha relación con el baño en piscinas públicas.
En climas cálidos la infección es rara, pero puede transmitirse entre menores de un año en las guarderías. Tiene un pico máximo de incidencia entre los 2 y 4 años.
En adultos jóvenes tiene que ver con las relaciones sexuales, y suele aparecer en la zona púbica. Es una enfermedad leve.
Tipos de molusco contagioso
No se puede hablar de diferentes tipos de molluscum pero sí de diferentes virus que dan lugar a la enfermedad. Aunque todos ellos producen la misma clínica, estos son MCV I, MCV II, MCV III, MCV IV , de ellos el más frecuente es el MCV I que produce hasta el 90% de las infecciones.
Causas del molusco contagioso
La causa del molusco es la infección por el virus pox-virus en sus diferentes subespecies siendo la más frecuente la MCV I.
Síntomas del molusco contagioso
El síntoma del molusco contagioso es la presencia de pápulas de aspecto blanco céreo. Las pápulas son múltiples, presentan hundimiento central y suelen tener como máximo 5 mm. Se sitúan en grupos que pueden tener un borde enrojecido . Pueden autoinocularse o transmitirse por contacto a otros individuos. En el caso de los niños, se presenta sobre todo en la cara y los pliegues del cuello. En adultos pueden encontrarse en la zona púbica cuando se contagia por contacto sexual. En paciente con inmunosupresión por VIH, puede presentar un crecimiento muy rápido.
Las lesiones pueden presentarse en cualquier parte del cuerpo salvo palmas de manos y plantas de pies.
Tratamiento para el molusco contagioso
En la mayoría de las ocasiones, las lesiones se autoeliminan sin necesidad de tratamiento:
Terapias de destrucción de lesiones : Se usa en lesiones rebeldes o cuando hay riesgo de contagio para otra persona. Entre ellas está la crioterapia, la extrusión, el curetaje y la electrodesecación.
La crioterapia: Es la congelación mediante nitrógeno líquido de la lesión. Suelen ser necesarias varias sesiones para su retirada y pueden dar lugar a cambios en la coloración de la piel.
La extrusión: Se realiza una pequeña abertura extrayendo el centro de la lesión. Este método puede enseñarse a los pacientes, quienes pueden realizarlo sobre las nuevas lesiones.
El curetaje: Se trata de eliminar la lesión desde su base con una método cortante. Es doloroso y se puede dar una crema anestésica previamente, pero es tolerada muy mal por los niños.
La electrodesecación: Se trata de retirar las lesiones con un bisturí eléctrico, no se recomienda en niños.
Láser de colorante pulsado: Se realiza en una sóla sesión y tardan entre 2 y 8 semanas en desaparecer las lesiones. Se tolera mejor que otros tratamientos.
Tratamientos farmacológicos tópicos: Son la cantaridina, la podofilina, hidróxido de potasio. El cidofovir es un antivírico que se usa exclusivamente en pacientes con lesiones y con HIV que no han respondido al resto de tratamientos.
Por último, en pacientes inmunodeprimidos se pueden usar agentes que aumentan la inmunidad como son el imiquimod y la cimetidina.
Pruebas complementarias del tratamiento del molusco contagioso
El diagnóstico del molusco contagioso es un diagnóstico clínico , pero en algunos casos se pueden examinar las lesiones al microscopio . Tras el curetaje, para estar seguro del diagnóstico, se usan tinciones de giemsa . Esta tinción marca los cuerpos de inclusión característicos de estas lesiones.
Factores desencadenantes del molusco contagioso
El contacto con otra persona infectada o con agua de baño que contenga el virus.
Factores de riesgo del molusco contagioso
Contacto con personas que presenten lesiones o con fomites que contengan el virus, como toallas o el agua del baño. La inmunodepresión facilita la infección y la propagación del virus.
Complicaciones del molusco contagioso
Dermatitis en zona de alrededor de lesiones.
Sobreinfección bacteriana de las lesiones.
Dispersión importante en pacientes con inmunodepresión.
Prevención del molusco contagioso
Evitar contacto con zonas de lesiones de otras personas.
Uso de preservativo en personas con lesiones en zonas genitales.
Evitar el rascado que puede dar lugar a inoculación del virus en otras zonas de la piel.
No compartir toallas, ni agua al bañarse.
Especialidades a las que pertenece el molusco contagioso
El molluscum contagioso va a ser tratado por el dermatólogo.
Preguntas frecuentes:
¿Cómo se contagia el virus del molusco contagioso?
El contagio del virus se realiza por el contacto del virus con la piel sana, ya sea a través de fomites, de agua del baño o contacto directo con personas que tengan las lesiones.
¿Qué es un curetaje dermatológico?
El curetaje dermatológico se realiza con un pequeño instrumental. Una especie de pequeña cucharilla que presenta una superficie cortante , dicha superficie se sitúa en la parte inferior de la lesión que se quiere retirar, y se procede a realizar un movimiento como de recogida con una cuchara. La lesión quedará en la cubeta de la cuchara pudiendo ser enviada al laboratorio para su examen.
¿Cuánto puede durar la infección del molusco contagioso?
Las lesiones de molusco contagioso pueden desaparecer de forma espontánea en las personas inmunocompetentes en períodos de hasta tres años , aunque la mayoría suelen desaparecer entre uno y dos años. Por ello, en muchos casos, el dermatólogo sólo debe vigilar las lesiones, sin tratarlas esperando a su resolución espontánea.

Enfermedad
Miastenia Gravis
¿Qué es la miastenia gravis?
La miastenia gravis es una enfermedad autoinmune, que afecta a la unión neuromuscular de un músculo estriado que produce una debilidad muscular tras realizar ejercicio . Puede haber entre 15 a 20 casos por cada 1.000.000 habitantes/año. Es una enfermedad grave que puede conducir a la muerte por una crisis respiratoria.
Tipos de miastenias
Miastenia gravis ocular: Supone el 20 de los diagnósticos.
Miastenia gravis generalizada : Se ven afectados los músculos oculares, tronco y extremidades. Dentro de ella hay diferentes subtipos como por ejemplo la bulbar, que afecta a músculos de la cara, el paladar y la deglución.
Respiratoria: Es la más grave y afecta a músculos respiratorios.
Seronegativa: No tiene anticuerpos, anti colinérgicos sin anticuerpos ni anti-musk, y tiene peor pronóstico.
Neonatal transitoria: Se da en niños de madres con miastenia y desaparece en 2 o 3 meses después del nacimiento. Se debe al paso de anticuerpos de la madre a través de la placenta.
Inducida por medicamentos como la penicilamina.
Remisión espontánea: Hasta un 20% remiten solas en el inicio de su evolución.
Causas de la miastenia gravis
No se conoce la causa actual de la miastenia, aunque al haber anticuerpos frente a la acetilcolina, se piensa tiene una base autoinmune.
Síntomas de la miastenia gravis
El síntoma principal de la miastenia gravis es la debilidad muscular, que aparece con mayor intensidad tras ejercicio intenso. Dicha fatiga se va produciendo a lo largo del día y desaparece con el reposo.
Los primeros síntomas que aparecen son:
La ptosis palpebral (caída del párpado superior) y la diplopía (visión doble) ya que lo primero a lo que afecta es a la musculatura del ojo. Aparece en casi en el 80% de los pacientes.
Dificultad para tragar, para hablar o para masticar .
Afectación a las extremidades no siendo simétrica, esto quiere decir que un lado del cuerpo puede estar más débil que el otro.
Afectación de la musculatura respiratoria: Produce disnea e insuficiencia respiratoria. Esto se conoce como crisis miasténica y puede necesitar ingreso hospitalario.
Tratamiento para la miastenia gravis
Tratamiento farmacológico: Con anticolinesterásicos y piridostigmina, es el tratamiento el más frecuente. Su acción es prolongar el efecto de la acetilcolina en el receptor de la unión neuromuscular.
Las inmunoterapias crónicas: Tienen como efecto controlar la cantidad de anticuerpos en la sangre. Se trata de glucocorticoides, azatioprina, ciclosporina y tacrolimus.
La inmunoterapia rápida: Se usa en la crisis miasténica. Se utiliza la plasmaféresis para retirar los anticuerpos del plasma sanguíneo y las inmunoglobulinas intravenosas para neutralizar los anticuerpos.
El tratamiento quirúrgico: Dicho tratamiento se realiza sobre el timo. El timo es un órgano glandular situado detrás del esternón, donde maduran los linfocitos, imprescindibles en el sistema inmune adaptativo por el cual el organismo se adapta a los invasores externos. Puede ser necesario extirparlo en estos pacientes durante los tres primeros años de la enfermedad, que es el momento en que es más efectivo
Pruebas complementarias del tratamiento de la miastenia gravis
Analíticas de sangre: Para buscar los anticuerpos anti colinérgicos y anticuerpos anti musk.
La prueba de edrofonio : Este fármaco es administrado al paciente para revertir el cuadro de miastenia durante unos cinco minutos.
Estudios electrofisiológicos : Como en el estudio de fibra única, se estudian dos fibras musculares y se alarga el tiempo de reacción de la segunda frente a la primera, y la estimulación nerviosa repetitiva de un nervio comprobando si altera la contracción muscular.
TAC o RMN para reconocer la posibilidad de un timoma (inflamación del Timo).
Factores desencadenantes de la miastenia gravis
No se conocen factores desencadenantes de la miastenia gravis
Factores de riesgo de la miastenia gravis
No hay factores de riesgo conocidos, los hombres desarrollan la enfermedad con mayor frecuencia por encima de los 60 años y las mujeres entre los 20 y los 60. Las personas con antecedentes familiares de miastenia gravis tienen mayor riesgo de sufrir la enfermedad.
Complicaciones de la miastenia gravis
Crisis miasténica y crisis colinérgica por exceso de medicación.
Prevención de la miastenia gravis
No existe forma de prevenir la miastenia gravis.
Especialidades a las que pertenece la miastenia gravis
Pueden ser tratadas por médicos de medicina interna y en algunos casos por neurólogos.
Preguntas frecuentes:
¿Qué es una crisis de miastenia?
La crisis de miastenia es un proceso grave, en cual se produce la a fectación de los músculos respiratorios del paciente. Éste va a necesitar de ingreso hospitalario urgente en una UVI, ya que de no tratarse puede dar lugar a la muerte.
¿Cómo es la debilidad muscular?
La debilidad muscular es la falta de capacidad de los músculos para contraerse, esto es una falta de fuerza en los mismos lo que se traduce en sensación de cansancio importante para el individuo que lo padece. Se puede definir también como fatigabilidad muscular. No es simétrica, sino que se produce en mayor medida en un lado del cuerpo que en el otro.
Enfermedad
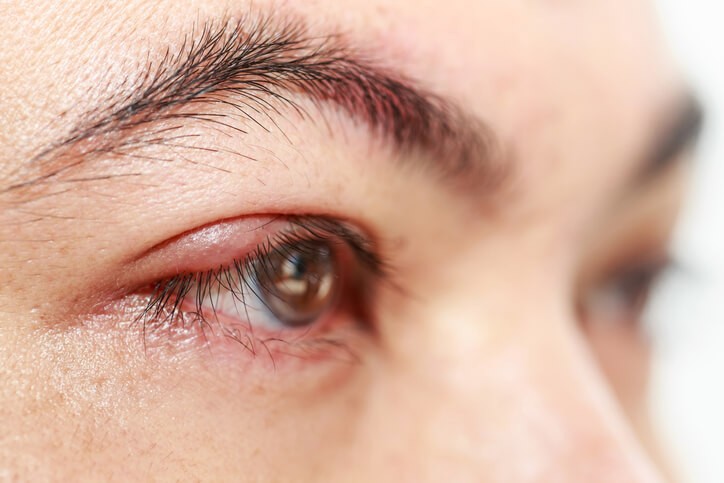
Orzuelo
¿Qué es un orzuelo?
El orzuelo es la inflamación de una de las glándulas de las pestañas , que se produce por el bloqueo de la misma. Es un motivo de consulta muy frecuente que se da en especialmente en niños, ya que estos tienen tendencia a tocarse los ojos con las manos sucias. Es una enfermedad categorizada como leve.
Tipos de orzuelo
Orzuelo externo : aparece en la parte exterior del párpado.
Orzuelo interno : aparece en la parte interior del párpado
Causas de un orzuelo
La causa del orzuelo es la infección por Estafilococo , bacteria que se encuentra en la piel de modo habitual.
Síntomas de un orzuelo
Los síntomas de un orzuelo son una protuberancia roja en el párpado superior o inferior , con hinchazón de este y dolor. Puede haber lagrimeo y presencia de legaña, y los nódulos suelen estar calientes y ser dolorosos.
Tratamiento para el orzuelo
El orzuelo se debe tratar con medidas locales, como son colocar un paño caliente sobre la zona , que se deberá de mantener entre 5 y 10 minutos unas 4 ó 5 veces al día. Se debe mantener el borde párpado limpio, para ello, se puede lavar con jabones especiales para los párpados de venta en farmacias, o bien con champú de bebé. No se deberá tocar el orzuelo ya que esto puede dar lugar a que el proceso se extienda. En la mayoría de las ocasiones el orzuelo desaparece en unos pocos días sin ningún tratamiento más. Puede ser necesario el uso de pomadas con antibiótico en el borde afectado.
Pruebas complementarias del tratamiento de orzuelo
El diagnóstico de un orzuelo es un diagnóstico clínico , solo en aquellos casos en los que tras un tratamiento antibiótico no remita, puede ser necesario realizar un cultivo de la sustancia del orzuelo para detectar qué germen ha producido el proceso y qué antibiótico es el más adecuado para tratarlo.
Factores desencadenantes de un orzuelo
El factor desencadenante es tocarse los ojos con las manos sucias.
Factores de riesgo de un orzuelo
Tocarse los ojos con las manos sucias, manipular las lentillas con las manos sucias, no retirarse el maquillaje de ojos al acostarse , usar productos cosméticos caducados, son los principales factores de riesgo. En pacientes inmunodeprimidos pueden producirse infecciones de párpados reiteradas.
Complicaciones de un orzuelo
Chalazión : lesión pequeña de aspecto tumoral que aparece en el borde libre de los párpados.
Celulitis preseptal : infección del párpado y la piel periocular por delante del tabique orbitario.
Celulitis orbitaria : infección que afecta a los tejidos incluidos dentro de la órbita, en las proximidades del ojo.
Prevención de un orzuelo
No tocarse los ojos sin lavarse las manos previamente.
Manejar las lentillas con las manos limpias.
Retirar los productos de maquillaje de forma correcta todas las noches.
Uso de productos de maquillaje de buena calidad y no caducados.
Higiene correcta de los párpados en casos de blefaritis (hinchazón de los párpados).
Especialidades a las que pertenece el orzuelo
El orzuelo será tratado y diagnosticado por un médico de familia, y solo en casos de complicaciones puede ser necesaria la consulta a un oftalmólogo.
Preguntas frecuentes
¿Dónde pueden salir orzuelos?
Los orzuelos salen en los párpados inferiores y superiores , pueden ser externos cuando el crecimiento es hacia el borde del párpado, o pueden ser internos cuando se desarrollan en la parte más interna del mismo.
¿Cómo se contagia el orzuelo?
Los orzuelos no se contagian de unas personas a otras, están producidos por el Estafilococo, que es una bacteria que tenemos en la nariz y en la piel, y que, al tocarse los ojos con las manos sucias , queda depositado en el borde del párpado. Ante pequeñas erosiones del mismo se puede producir el desarrollo de un orzuelo.
¿Qué es un chalazión?
El chalazión es la i nfección que se produce en un párpado, no en las glándulas de las pestañas, sino en las glándulas del interior del mismo . Se produce por el bloqueo y la posterior infección de las glándulas de meibomio del párpado (glándulas que producen una secreción grasa que forma parte de la película del lagrimal y la estabiliza), estas glándulas son necesarias para la lubricación del ojo.
¿Cuánto dura un orzuelo?
El orzuelo es una enfermedad que suele durar entre una y dos semanas , en muchos casos desaparece sin ningún tratamiento.
¿Duele un orzuelo?
Sí, uno de los síntomas principales del orzuelo es el dolor que produce en el párpado. Se debe a la inflamación local y a que el párpado es una zona con muchas terminaciones nerviosas, se suele aliviar con el uso de compresas calientes.

Enfermedad
Insuficiencia Cardiaca
¿Qué es la insuficiencia cardíaca?
La insuficiencia cardíaca es un estado en el que el corazón es incapaz de bombear toda la sangre que el organismo necesita para aportar el oxígeno y los nutrientes necesarios a cada parte. Es una patología frecuente, sobre todo en las personas mayores de 65 años, siendo la principal causa de hospitalización de este segmento de la población. Es una patología grave con un pronóstico a largo plazo malo, siendo la tercera causa de muerte cardiovascular en España.
Tipos y causas de insuficiencias cardíaca
En relación a las formas y causas de insuficiencia cardíaca, se dividen distintos tipos según la rapidez de instauración de los síntomas o en la función del corazón:
Insuficiencia cardíaca sistólica VS. diastólica:
Insuficiencia cardíaca sistólica : se produce cuando el corazón tiene dificultad para impulsar la sangre hacia el resto del organismo, ya que existen patologías o alteraciones que dañan su pared muscular y esta no es capaz de contraerse para impulsar la sangre adecuadamente. Habitualmente el corazón se encuentra dilatado.
Insuficiencia cardíaca diastólica : se produce cuando existe una dificultad en la relajación del músculo cardíaco, con lo que el corazón no puede llenarse adecuadamente de sangre para luego impulsarla hacia el organismo. Habitualmente la pared muscular cardíaca se encuentra hipertrofiada (aumentada de tamaño).
(*) En la mayoría de los pacientes coinciden en mayor o menor medida ambas situaciones.
Insuficiencia cardíaca aguda VS. crónica:
Insuficiencia cardíaca aguda : es aquella que aparece de forma súbita por una alteración cardíaca repentina en la que se produce una alteración de su funcionamiento de contracción y relajación, como ocurre por ejemplo en un infarto de miocardio (con una muerte del tejido del corazón). También se denomina aguda a las descompensaciones súbitas que sufre un paciente que presente insuficiencia cardíaca crónica.
Insuficiencia cardíaca crónica : es aquella que se produce de forma paulatina por una alteración progresiva de la función del corazón y que permite activar mecanismos compensadores en el organismo que le permiten adaptarse a la reducción de la sangre que bombea el corazón.
Insuficiencia cardíaca derecha VS. izquierda : esta clasificación hace referencia a los síntomas derivados del fallo predominante de uno de los dos ventrículos cardíacos, presentado unas manifestaciones predominantes de congestión pulmonar si es izquierda, y de congestión venosa sistémica (edemas en miembros inferiores, congestión hepática y del bazo), si es derecha.
Síntomas de la insuficiencia cardíaca
Se presentan dos tipos de síntomas: los derivados del deficiente aporte de sangre a los tejidos y los secundarios, debidos a una sobrecarga de líquidos que se produce en el sistema de retorno sanguíneo al corazón.
La sensación de falta de aire o disnea es uno de los síntomas más frecuentes e importantes que se produce por acúmulo de líquido en el pulmón, lo que dificulta la oxigenación de la sangre.
La fatiga al inicio , aparece cuando el paciente hace esfuerzos pero en los estados más avanzados de la insuficiencia cardíaca. Esta sensación de falta de aire y ahogo se da con mínimos esfuerzos o estando en reposo. En ocasiones aparece esa sensación cuando el paciente se tumba (al acostarse), lo que se denomina ortopnea.
Otras veces el paciente presenta crisis repentinas de sensación de ahogo cuando está dormido en la cama que le hacen tenerse que levantar de forma súbita, lo que se llama disnea paroxística nocturna. En ocasiones en estas circunstancias aparecen ruidos respiratorios como “silbidos” (sibilancias), es lo que se llama “asma cardial”.
La congestión pulmonar también da lugar a la aparición de tos persistente y no productiva (sin expectoración de flemas).
Además de en el pulmón, existe un acúmulo de líquidos en el organismo que da lugar a la aparición de edemas en las piernas, y que en ocasiones llegan hasta el abdomen (ascitis). Hay congestión en el hígado que puede producir dolor en la parte superior derecha del abdomen, sensación de plenitud gástrica, náuseas y estreñimiento por edema en el tubo digestivo.
Es frecuente además la presenta de sensación de fatiga y debilidad al llegar una cantidad de sangre insuficiente a los músculos.
Igualmente, al no estar bien irrigado el cerebro aparece somnolencia, confusión, ansiedad, pérdida de memoria , dolor de cabeza, insomnio, e incluso alteraciones psiquiátricas.
El sistema renal también se ve afectado, produciéndose en las fases precoces un aumento de la micción nocturna (nicturia), y disminuyendo de forma global la cantidad de orina (oliguria) que hace el paciente.
Tratamiento para la insuficiencia cardíaca
Si es posible, siempre se debe establecer el tratamiento de la causa subyacente que produce la insuficiencia cardíaca, por ejemplo, tratamiento del infarto de miocardio, de la pericarditis, de la alteración de las válvulas del corazón, el control de la tensión arterial…etc.
Como medidas específicas del tratamiento de la insuficiencia cardíaca se establecen distintos tratamientos farmacológicos con distintos objetivos:
Prevención del deterioro de la función cardíaca.
Reducción del trabajo cardíaco.
Incremento de la contractilidad del músculo cardíaco.
Prevención de la muerte súbita y resincronización de arritmias.
Para ello se utilizan varios tipos de fármacos:
Inhibidores de la enzima de conversión de la angiotensina (IECAS) → Enalapril , Captopril y Ramipril .
Fármacos Betabloqueantes → Bisoprolol, Carvedilol, Metoprolol.
Fármacos antagonistas de los receptores de la Angiotensina II (ARA-II) → Olmesartán, Valsartán y Telmisartán .
Fármacos antagonistas de la aldosterona → Espironolactona y Eplerenona.
Diuréticos de asa → Furosemida y Torasemida .
Diuréticos tiazídicos → Hidroclorotiazida y Clortalidona .
Fármaco reductor de la frecuencia cardíaca → Ivabradina.
Asociación de nitratos e Hidralazina.
Fármacos para control de la disfunción del ventrículo y su frecuencia → Digoxina.
(*) Otros fármacos utilizados para el tratamiento de la alteraciones cardiovasculares que pueden aparecer en pacientes con insuficiencia cardíaca son anticoagulantes de la sangre, antiagregantes de las plaquetas, fármacos reductores del colesterol como Estatinas.
(*) Otro tipo de tratamiento que se realiza, cuando es preciso por la evolución de la enfermedad y la ausencia de respuesta al tratamiento farmacológico, es la instauración de dispositivos para mejorar los síntomas (desfibrilador implantable con terapia de resincronización cardiaca o TRC), o disminuir la probabilidad de morirse de repente (desfibrilador automático implantable o DAI).
Pruebas complementarias del tratamiento de la insuficiencia cardíaca
El diagnóstico de la insuficiencia cardíaca es fundamentalmente clínico. Además, se utilizan pruebas complementarias para apoyo y detección de las alteraciones que se producen en la insuficiencia cardíaca, como:
Analítica de sangre : con determinación de hemograma, que detecta la presencia de anemia que puede aparecer en esta patología, función renal con creatinina, que puede estar alterada por mala función del riñón al no tener suficiente aporte de sangre, enzimas hepáticas que serán elevadas cuando hay congestión y mala perfusión del hígado, iones (sodios, potasio, calcio…etc), y determinación del péptido natriurético cerebral (BNP) y el péptido natriurético auricular (ANP), sustancias que aumentan en insuficiencia cardíaca y son útiles para la monitorización del tratamiento.
Electrocardiograma : detecta alteraciones del ritmo del corazón que pueden ser causa o consecuencia de la insuficiencia cardíaca.
Radiografía de tórax : se objetivan con ella alteraciones de la forma del corazón (cardiomegalia o agrandamiento del corazón), y signos de congestión pulmonar.
Ecocardiograma : prueba de imagen que es fundamental para detectar las causas de la insuficiencia cardíaca con valoración de la anatomía y alteraciones del corazón.
Cardio-resonancia : valora la morfología cardíaca, la función cardíaca y las alteraciones del músculo cardíaco.
Otras pruebas que se pueden realizar son Holter, espirometría, ergometría para valoración de la función, y evaluación del pronóstico y del tratamiento de la insuficiencia cardíaca.
Factores desencadenantes de la insuficiencia cardíaca
Las alteraciones en las que pueden desencadenar la insuficiencia cardíaca son:
Retirada de tratamientos o transgresión de dietas.
Aparición de arritmias cardíacas (alteraciones del ritmo del corazón).
Cardiopatía isquémica.
Infecciones sistémicas o generalizadas.
Miocarditis (inflamación del músculo del corazón).
Embolismo pulmonar.
Insuficiencia renal.
Anemia.
Abuso de alcohol.
Drogas o fármacos que deprimen la función del corazón.
Factores de riesgo de la insuficiencia cardíaca
Los factores de riesgo son alteraciones de la estructura del corazón (adquiridas o congénitas), que afectan a las válvulas cardíacas, al pericardio, al músculo cardíaco, y/o a los vasos sanguíneos. Así, la enfermedad coronaria, la hipertensión arterial y la miocardiopatía dilatada , son los principales factores de riesgo para padecer una insuficiencia cardíaca.
Complicaciones de la insuficiencia cardíaca
Edema agudo de pulmón.
Derrame pleural.
Insuficiencia venosa y úlceras en las piernas.
Infarto cerebral.
Infarto agudo de miocardio.
Insuficiencia renal.
Insuficiencia hepática.
Trombosis venosa profunda.
Desnutrición.
Shock cardiogénico (fallo multiorgánico por fallo del funcionamiento del corazón).
Muerte.
Prevención de la insuficiencia cardíaca
Control de peso: la dieta debe ser rica y variada, pobre en sal, sin grasas y baja en azúcar.
No fumar ni beber alcohol así como no tomar otras drogas.
Controlar de manera frecuente la tensión arterial y la frecuencia cardíaca.
En pacientes de riesgo se aconseja la vacunación de la gripe y del anti-neumococo.
Control del estrés y la ansiedad.
Dormir y descansar adecuadamente.
Especialidades a las que pertenece la insuficiencia cardíaca
La insuficiencia cardíaca es una patología que cuando se produce en un grado inicial, puede diagnosticarse y tratarse ambulatoriamente por el médico de atención primaria. Cuando los síntomas son más intensos y graves, el paciente debe ser hospitalizado y tratado por cardiólogos o médicos internistas.
Preguntas frecuentes:
¿Qué es una arritmia cardíaca?
La arritmia cardiaca es un trastorno y alteración del ritmo cardíaco del corazón producido por algún cambio de sus características y frecuencia.
¿Qué es un ataque al corazón?
El ataque al corazón es una forma coloquial de referirse al infarto agudo de miocardio. Es la circunstancia patológica que sufre el corazón cuando el flujo de sangre que transporta el oxígeno y los nutrientes necesarios hacia el propio músculo del corazón por las arterias se interrumpe cuando estos vasos sanguíneos se obstruyen, desencadenando la muerte del tejido cardíaco.
¿Qué es un preinfarto?
Un preinfarto es una forma de denominar a las alteraciones previas que pueden aparecer antes de que se produzca un infarto cardíaco. Estas alteraciones se denominan anginas cardíacas o anginas de pecho , en las que de forma momentánea se produce una interrupción del aporte de sangre al tejido del corazón por obstrucción de alguna de sus arterias, que posteriormente vuelve a restablecerse.
¿Qué es un soplo en el corazón?
Un soplo en el corazón es un sonido auscultado por el médico con su fonendoscopio producido por la alteración del paso del flujo de sangre a través de las válvulas del corazón cuando estas están alteradas.
¿Cuáles son los primeros auxilios en caso de infarto?
Al inicio de los síntomas se debe colocar al paciente sentado o tumbado para evitar caídas o traumatismos si llega a perder la consciencia. Rápidamente se debe llamar al teléfono de emergencias 112. Tranquilizar al paciente y retirarle aquellas ropas que le aprieten . Preguntarle si tiene antecedentes cardiológicos y si porta alguna medicación para el tratamiento del dolor torácico (nitroglicerina). Si lo tiene, se le ha de administrar. En todo momento se debe observar al paciente y estar pendiente de si respira y si tiene pulso y consciencia. Si el paciente tiene pulso y respira pero pierde la consciencia se le debe colocar en posición lateral de seguridad. Si no tiene pulso y no respira se deben iniciar las maniobras de RCP básicas (reanimación cardiopulmonar básica), hasta que lleguen los servicios médicos de emergencias.

Enfermedad
Hipopotasemia
¿Qué es la hipopotasemia?
La hipopotasemia o hipokaliemia es la disminución de la concentración de potasio en la sangre por debajo de 3.5 mEq/L . Es probablemente el trastorno electrolítico más frecuente, apareciendo hasta en el 20% de los pacientes ingresados en hospitales. Es frecuente en pacientes que toman algunos tipos de fármacos diuréticos.
Tipos de hipopotasemia
Según la disminución de la concentración de potasio, la hipopotasemia se puede dividir en:
Leve : cuando las concentraciones en plasma de potasio disminuyen entre 3.5-3 mEq/L
Moderada: las concentraciones de potasio en plasma disminuyen hasta 3-2.5 mEq/L.
Grave : las concentraciones de potasio en plasma están por debajo de 2.5 mEq/L.
También puede existir una pseudo hipopotasemia cuando existe un aumento en la muestra de la sangre de glóbulos blancos.
Causas de la hipopotasemia
La hipopotasemia puede ser debida a la pérdida de potasio por pérdidas a través de vómitos, diarrea o toma de diuréticos (diuréticos del asa o tiazidas ) asociada a la pérdida de líquidos. También por la toma de otros fármacos como antibióticos a dosis elevadas ( Penicilina , Ampicilina …etc), o fármacos laxantes , por la sudoración excesiva o quemaduras graves. También puede suceder en patologías donde existen alteraciones de los mineralocorticoides, como hiperaldosteronismo primario, toma de regaliz de forma muy frecuente, tratamiento con corticoides, disminución del flujo por la arteria renal por estenosis, o estrechamiento de su luz. En otras circunstancias se produce una disminución del potasio porque el existente a nivel sanguíneo y del líquido que existe fuera de las células se introduce dentro de estas. Esto ocurre por ejemplo cuando se corrige con insulina un aumento de la glucosa en los pacientes diabéticos, o la disminución de temperatura (hipotermia), o la alcalosis metabólica.
Además existen grupos de riesgo en los que por razones sociales, culturales o económicas tienen una disminución de alimentos ricos en potasio, pudiendo conducir hipopotasemia.
Síntomas de hipopotasemia
Los síntomas que aparecen en los pacientes dependen de la rapidez con la que disminuye el potasio y los valores en los que éste desciende. Así, los pacientes pueden presentar síntomas como cansancio, dolores (mialgias) o debilidad a nivel muscular, problemas digestivos como estreñimiento, íleo paralítico (alteración del movimiento intestinal), parálisis muscular que puede desencadenar alteraciones respiratorias, afectación cardíaca con aparición de arrítmicas, sobre todo en aquellos pacientes con antecedentes de patologías cardíacas. También pueden aparecer alteraciones del sistema nervioso central como ir ritabilidad, síntomas psicóticos, enlentecimiento del pensamiento o letargia, etc. Además, pueden aparecer alteraciones del funcionamiento del riñón (nefropatía intersticial, diabetes insípida, etc), o alteraciones metabólicas como intolerancia a los hidratos de carbono o alcalosis metabólica.
Tratamiento para la hipopotasemia
En los pacientes asintomáticos y con disminución moderada de potasio se realiza una reposición progresiva de este por vía oral, utilizándose el cloruro potásico ( Potasion cápsulas® ) de forma habitual. Se puede aumentar además el aporte de potasio en la dieta con zumos y otros alimentos ricos en potasio.
Cuando aparecen síntomas o exista una hipopotasemia grave se administra el potasio (cloruro potásico) de forma diluida en suero fisiológico por vía intravenosa de forma progresiva, con una monitorización constante del paciente para el control exhaustivo del potasio en sangre.
Pruebas complementarias del tratamiento de hipopotasemia
Para realizar el diagnóstico de la hipopotasemia y sus posibles causas se realiza una analítica de sangre con determinación de iones (potasio, sodio y magnesio, entre otros), resto de bioquímica con glucosa creatinina, urea y enzimas musculares. Según el caso, en la analítica se pueden determinar los niveles de renina y aldosterona. Además, se realiza un electrocardiograma.
Factores desencadenantes de la hipopotasemia
El factor desencadenante de la hipopotasemia es la falta de aporte en la dieta de potasio, la pérdida aumentada de potasio debido a alteraciones del riñón u otras alteraciones extrarrenales o una distribución en el organismo diferente de la normal (aumento del potasio dentro de las células y disminución en el espacio extracelular).
Factores de riesgo de la hipopotasemia
Toma de fármacos como agonistas beta2-adrenérgicos, aminoglucósidos , rifampicina , penicilinas no potásicas, laxantes, diuréticos no ahorradores de potasio, nifedipino …etc.
Edad avanzada.
Padecimiento de enfermedades poco frecuentes como el Síndrome de Liddle, Síndrome de Gitelman o Síndrome de Bartter, que producen una alteración en el transporte de potasio a nivel renal.
Padecer anorexia nerviosa y bulimia
Padecimiento de enfermedades infecciosas , tumorales o de otro tipo, que producen vómitos y diarrea.
Complicaciones de la hipopotasemia
La disminución persistente del potasio puede producir alteraciones como:
Retraso del crecimiento que se ha relacionado con disminución de los niveles de hormona de crecimiento producida por la disminución del potasio.
Alteraciones en el riñón.
Aparición de arritmias graves en el corazón que pueden desencadenar la muerte.
Trastornos psiquiátricos graves.
Prevención de la hipopotasemia
Vigilancia de los niveles de potasio en pacientes que precisen la toma de fármacos diuréticos no ahorradores de potasio y en aquellos otros fármacos que puedan disminuir las concentraciones de potasio en sangre.
Se debe realizar una dieta variada que contenga alimentos ricos en potasio como
frutos secos, legumbres, zumos…etc.
Tratamiento adecuado de las patologías de base que pueden provocar una disminución de potasio en sangre.
Especialidades a las que pertenece la hipopotasemia
La hipopotasemia puede tratarse según el grado de alteración que se presente por el médico de atención primaria, por un especialista en nefrología y en medicina interna. Si existen déficit graves se corrigen en los servicios de urgencias hospitalarias continuando la corrección con el ingreso del paciente.
Preguntas frecuentes:
¿Qué pasa cuando baja el potasio?
Al disminuir la concentración de potasio en sangre se producen alteraciones en las funciones musculares apareciendo debilidad, dolores, atrofia de la masa muscular , parálisis, calambres, alteraciones del ritmo del corazón y de la función renal, estreñimiento, y alteraciones metabólicas y del sistema nervioso central.
¿Qué es la hiperpotasemia?
La hiperpotasemia es una alteración hidroelectrolítica en la que se produce un aumento de la concentración de potasio en la sangre por encima de 5.5 mEq/L.
¿Cuál es el nivel normal de potasio en la sangre?
La concentración de potasio en sangre es normal si se sitúa entre 3,5 a 5,3 mEq/L.
¿Qué alimentos contienen potasio?
Los alimentos que más potasio contienen son la leche en polvo, los quesos, carnes como liebre y el conejo, embutidos, peces, moluscos y crustáceos como la vieira, palometa, caviar, jurel, boquerón, surimi, caballa, salmón, pulpo, pez espada, percebe, pescados ahumados, los huevos, todos los frutos secos, todas las legumbres, verduras y hortalizas como la pimienta negra, el perejil, patata, ajo, espinaca, acelga, champiñón, trufa, col de Bruselas, cardo, escarola, brócoli, endivia, col, coliflor, remolacha, cereales y derivados como la harina de soja, germen de trigo, cebada, avena, maíz y frutas como dátiles, coco, grosella negra, plátano, aguacate, kiwi, y el melón.
¿Qué pasa cuando tienes el potasio alto?
Según los niveles en los que se sitúe el potasio por encima de la concentración normal de potasio en la sangre, los pacientes pueden estar asintomáticos hasta presentar alteraciones gastrointestinales como náuseas y vómitos, debilidad, hormigueo , íleo paralítico (alteración de la movilidad del intestino), dificultad para la deglución (difagia), dificultad para caminar, parálisis muscular y en casos graves alteración de la función del músculo del corazón y aparición de arritmia ventriculares graves que pueden producir la muerte. Todo ello se produce porque al elevarse el potasio en la sangre existe una alteración en la transmisión de los impulsos neuromusculares (entre los nervios que llevan la información y los músculos).

Enfermedad
Hipoglucemia
¿Qué es la hipoglucemia?
La hipoglucemia es una bajada de la cantidad de azúcar en la sangre por debajo de 60 mg/ml. En los recién nacidos son más frecuentes en los niños pretérmino, llegando a ser hasta del 14% de los casos. En los niños a término suele darse como mucho en un 7%. Las hipoglucemias en los diabéticos son más frecuentes en pacientes con insulina o secretagogos que con otros tratamientos hipoglucemiantes. Es una situación urgente de revertir ya que es grave porque puede poner en peligro la vida del individuo.
Causas de la hipoglucemia
La causa principal de la hipoglucemia es la alteración hormonal a nivel de hipófisis y tiroides . También se puede producir en pacientes normales sin alteraciones hormonales por causa de falta de alimento, exceso de ejercicio , o descarga insulínica en el páncreas.
Síntomas de la hipoglucemia
Los síntomas son: malestar, cansancio, adormecimiento, temblor, sudoración profusa, palpitaciones, mareos, visión borrosa, dolor de cabeza, convulsiones y trastorno del comportamiento.
Tratamiento para la hipoglucemia
El tratamiento para la hipoglucemia es dar azúcar de forma rápida. Se puede dar un producto azucarado como pueden ser los zumos de frutas , o también se puede dar directamente un sobre de azúcar disuelto en un vaso de agua. En casos muy difíciles de revertir y en pacientes diabéticos, puede ser necesario darles Glucagón mediante inyección subcutánea.
Pruebas complementarias del tratamiento de la hipoglucemia
La prueba complementaria será la determinación de glucosa en sangre capilar, hasta normalización de la misma, cada media hora.
Factores desencadenantes de la hipoglucemia
Los factores desencadenantes de la hipoglucemia son la falta de aporte de hidratos de carbono en la dieta , o el exceso de insulina en la sangre.
Factores de riesgo de la hipoglucemia
Son factores de riesgo para sufrir hipoglucemia en los pacientes en tratamiento con insulina y con secretagogos como Repaglinida y Glibenclamida . Los largos periodos de ayuno sin ingesta de hidratos de carbono , el periodo neonatal en niños pretérmino que tienen más problemas en regular hormonalmente sus niveles de glucemia, y también en niños a término en especial si son hijos de madres diabéticas.
Complicaciones de la hipoglucemia
Daños neurológicos.
Convulsiones.
Pérdida de conocimiento.
Coma.
Prevención de la hipoglucemia
No realizar ejercicio en ayunas.
Ingesta adecuada de hidratos de carbono.
Control capilar de glucemia.
Especialidades a las que pertenece la hipoglucemia
En el caso de hipoglucemias neonatales se trata de control con pediatras neonatólogos, en el resto de casos, se controla por el endocrino.
Preguntas frecuentes:
¿Qué es la hipoglucemia en bebés?
La hipoglucemia en bebés es la bajada de azúcar que se puede producir en los recién nacidos, más frecuente en niños prematuros, en niños nacidos a término que presentan madres diabéticas en el embarazo, y en niños con retraso en el crecimiento intrauterino.
¿Qué puede ocasionar la hipoglucemia?
Las hipoglucemias se producen por el exceso de insulina o por la falta de hidratos de carbono. En personas con tratamiento con insulina o fármacos secretagogos (fármacos que producen la secreción de insulina), se pueden producir hipoglucemias. En los neonatos que no tienen aún una buena regulación hormonal también se produce por parte del organismo un exceso de insulina que es la que causa la hipoglucemia. Las personas que tienen largos periodos de ayuno pueden presentar una hipoglucemia por falta de ingesta.
¿Qué diferencia hay entre hiperglucemia e hipoglucemia?
Las hiperglucemias son valores por encima de lo normal de azúcar en sangre (son niveles normales entre 70 y 129 mg/dl). La hipoglucemia son valores por debajo de lo normal de azúcar en sangre . Para tener síntomas de hipoglucemia, la glucosa deberá de estar por debajo de 60 mg/dl.
¿Cuáles son los niveles normales de azúcar en sangre?
Los niveles normales de azúcar en sangre son diferentes antes y después de la ingesta, así, en ayunas se consideran normales niveles de entre 70 y 128 mg/ml, por encima de estas cifras se habla de hiperglucemia, cuando se ha consumido alimento se considera que a las dos horas de haberlo ingerido los niveles de azúcar deben estar por debajo de 140 mg/ml
¿Qué es la hipoglucemia reactiva?
La hipoglucemia reactiva o hipoglucemia postprandial es la que se produce unas cuatro horas después de comer y no necesita un tratamiento especial, salvo el regular la ingesta de alimentos. Suele ser suficiente con no comer alimentos azucarados con el estómago vacío y hacer cinco comidas al dia.

Enfermedad
Rickettsia
¿Qué es la Rickettsia?
Las Rickettsias son un género de bacterias que producen diferentes enfermedades infecciosas , las cuales se contagian por aerosoles, mordeduras, picaduras, rasguños, aguas y/o alimentos contaminados. La incidencia en España de infecciones por Rickettsia es de 0,36 por cada 100.000 habitantes y año. La comunidad autónoma con mayor número de casos es Andalucía, seguida de Cataluña, y se produce más en hombres que en mujeres y en edades superiores a los 55 años, aumentando los casos durante el verano y disminuyendo durante el invierno. La Rickettsia produce problemas neurológicos y puede producir endocarditis en pacientes inmunodeprimidos, es una enfermedad de tipo leve.
Tipos de Rickettsias
Rickettsia rickettsii : es la bacteria que causa la fiebre de las enfermedades rocosas .
Rickettsia conorii : es la causante de la fiebre botonosa mediterránea, es la rickettsiosis más frecuente en España.
Rickettsia prowazekii : causa el tifus epidémico .
Causas de la Rickettsia
La causa de la Rickettsia suele ser por transmisión desde un insecto que suele ser un artrópodo:
La fiebre botonosa mediterránea se transmite por la picadura de una garrapata dura , el reservorio de la enfermedad es el perro. Por tanto, se trata de una zoonosis .
La fiebre de las montañas rocosas se transmite por la picadura de una garrapata, se transmite por la garrapata de la madera y la garrapata del perro .
El tifus epidémico se transmite a través del piojo del cuerpo , cuando sus heces infectadas entran por lesiones que pueda haber en la piel.
Síntomas de la rickettsia
Fiebre botonosa mediterránea : se encuentra una mancha negra en el lugar de la picadura de la garrapata, fiebre elevada , exantema , conjuntivitis y faringitis con cefalea intensa, y pueden asociarse también mialgias y artralgias , así como dolor abdominal con náuseas y vómitos asociado a hepatomegalia y esplenomegalia. En algunos pacientes solo se encuentran las adenopatías como síntomas.
Fiebre de las montañas rocosas : suele dar lugar a fiebre , dolor de cabeza , confusión , dolor muscular y erupción cutánea . Puede asociarse a vómitos, diarrea, falta de apetito, dolor abdominal, sensibilidad a la luz y alucinaciones.
Tifus epidémico : los síntomas principales son fiebre , cefalea intensa y cansancio súbito , y máculas pequeñas en las axilas y en la parte superior del tórax. Este exantema puede convertirse en petequial y hemorrágico , y además el paciente puede tener esplenomegalia (aumento del bazo) e hipertensión , que le lleve a un colapso circulatorio.
Tratamiento para la rickettsia
El tratamiento de las Rickettsiosis será antibiótico , que se debe empezar a suministrar en el momento más precoz posible. Se pondrá Tetraciclina en dosis de 250 mg. cada 6 horas en adultos y en niños se usa en dosis de 50mg. cada 8h. La Doxiciclina se va a usar en dosis de 100mg. cada 12 horas en adultos y en dosis de 2-4mg. por kg de peso cada 12 horas en niños. Se pueden usar otros fármacos como el Cloranfenicol , la Josamicina , y las Quinolonas .
Pruebas complementarias del tratamiento de la Rickettsia
Diagnóstico clínico por la sospecha de la sintomatología en zonas endémicas .
Analítica de sangre con recuento celular, velocidad de sedimentación y bioquímica con transaminasas, función renal y pruebas de coagulación.
Cultivo de sangre buscando la Rickettsia .
Serología determinando Igm. específica contra la bacteria.
La PCR para búsqueda de ADN en coágulos de sangre.
Factores desencadenantes de la Rickettsia
El factor desencadenante es la picadura de la garrapata o la presencia de piojos del cuerpo en el individuo.
Factores de riesgo de la Rickettsia
Son factores de riesgo para la Rickettsia son: la convivencia con animales infectados por garrapatas o personas que pasean o viven habitualmente en el campo, y también las personas que viven en la calle en el caso del piojo del cuerpo.
Complicaciones de la rickettsia
Hepatomegalia.
Esplenomegalia.
Hemorragias.
Hipotensión.
Meningitis.
Fracaso renal.
Artritis.
Anemias.
Coagulación intravascular diseminada.
Insuficiencia cardíaca.
Insuficiencia respiratoria.
Neumonitis.
Prevención de la Rickettsia
Evitar la picadura de garrapata.
Uso de repelentes .
Eliminación de la garrapata si esta ha picado.
Uso de ropa de manga larga, pantalón largo con los bajos por dentro de las botas al andar por el campo.
Especialidades a las que pertenece la Rickettsia
La Rickettsiosis suele ser tratada por médicos de medicina interna y especialistas en enfermedades infecciosas.
Preguntas frecuentes
¿Qué es Rickettsiosis ?
La Rickettsiosis son el conjunto de enfermedades producidas por la infección de una Rickettsia que el individuo puede adquirir por la picadura de una garrapata, un piojo o por inhalación de restos de heces de animales que contengan la bacteria. Los diferentes tipos de Rickettsia dan lugar a diferentes enfermedades.
¿Qué enfermedades ocasionan las Rickettsias ?
Son enfermedades producidas por las Rickettsias la fiebre botonosa mediterránea , la fiebre de las montañas rocosas , el tifus epidémico , el tifus murino , el tifus de las malezas y la fiebre africana por picadura de garrapata.
¿Qué es el tifus?
El tifus epidémico es un Rickettsiosis que se produce por la Rickettsia prowazekii , se produce por el paso de la bacteria que se encuentra en las heces del piojo del cuerpo, hacia el interior de la piel a través de zonas de arañazos o lesiones en la piel. El paciente, tras infectarse, a los 7 ó 12 días presenta súbitamente fiebre elevada con cefalea intensa y postración importante. La fiebre puede ser de hasta 40 grados y permanecer elevada hasta dos semanas. Las máculas sobreelevadas y rojizas se suelen situar en las axilas y en el tronco, y respetan las palmas de manos y pies, así como la cara. Cuando se agrava el proceso, las máculas se convierten en petequiales y hemorrágicas , dando lugar a una hipotensión arterial, acompañada de insuficiencia renal, encefalitis y equimosis con gangrena y neumonía.
¿Qué es la fiebre botonosa?
La fiebre botonosa es una infección producida por una Rickettsia del género coronoi , que es transmitida por la picadura de la garrapata del perro . Produce fiebre, cefalea y lesiones maculosas que pueden ser equimóticas y que se suelen iniciar en las extremidades inferiores y extenderse posteriormente. Afecta al cuero cabelludo, cara, palmas y plantas de los pies, y pueden aparecer mialgias, artralgias y dolor abdominal, así como náuseas, vómitos, hepatomegalia esplenomegalia y quemosis.
¿Qué es la fiebre mediterránea familiar?
La fiebre mediterránea es un trastorno hereditario que se transmite de padres a hijos y en el cual se produce una inflamación del revestimiento del tórax, el abdomen y las articulaciones. Se produce por una mutación en el gen MEFV . Afecta a personas de la cuenca mediterránea, en especial a personas de ascendencia sefardí, armenia y arábica. El episodio agudo lleva asociado fiebre alta junto con inflamación que dará lugar a artritis , dolor articular , y dolor abdominal y torácico asociado con úlceras cutáneas.
Enfermedad
Lepra
¿Qué es la lepra?
La lepra o enfermedad de Hansen (el médico noruego Gerhard Armauer Hansen en 1873 descubrió el microorganismo que la produce), es una enfermedad crónica producida por la bacteria Mycobacterium leprae, que afecta en su expresión primaria a los nervios periféricos y de forma secundaria a la piel y a otros tejidos. Es una enfermedad de distribución mundial que afecta de forma endémica en regiones de Asia y Sudamérica. Se trata de una patología grave por sus posibles repercusiones y complicaciones.
Tipos de lepra
La lepra se divide según su estado de presentación y el estado de las defensas del paciente en:
Lepra indeterminada : estadío precoz y transitorio.
Lepra tuberculoide : ocurre en pacientes con inmunidad o defensas activas.
Lepra borderline tuberculoide .
Lepra borderline lepromatosa .
Lepra lepromatosa : la que ocurre en pacientes con inmunidad alterada. En las lesiones dérmicas se encuentran muchas bacterias.
Causas de la lepra
La causa de la enfermedad es la infección por la bacteria Mycobacterium leprae, cuyo reservorio es el ser humano. La transmisión se produce por el contacto entre personas a través de gotas nasales infecciosas. La transmisión a través de las lesiones cutáneas es más rara.
Síntomas de la lepra
La forma de inicio es la Lepra indeterminada, afectando más a niños. Aparecen lesiones dérmicas a modo de manchas rojizas o con disminución del color (hipocrómicas), redondeadas y con bordes mal definidos. Se localizan en la espalda, en la parte superior de los brazos, en los muslos y en las nalgas. En las lesiones existe una alteración de la sensibilidad al calor y al dolor . Un 75% de los pacientes evoluciona a la curación tras meses o años.
La lepra tuberculoide es la más frecuente. Aparecen un número escaso de lesiones en la piel, ovaladas de color rojizo parduzco, con bordes bien definidos y con la región central más clara, que surgen en nalgas, tronco, hombros muslos y cara. En las lesiones no existe sensibilidad en esa piel, ya que existe un engrosamiento de los troncos nerviosos periféricos que además produce parálisis de la musculatura .
La lepra lepromatosa es la forma más grave y contagiosa. Las lesiones que aparecen de forma simétrica son pequeñas manchas (máculas) rojizas con bordes difusos y superficie brillante. Otra de las lesiones son nódulos o leproma, que son las lesiones más características. Son pequeñas tumoraciones de hasta 3-4 cm, duras y recubiertas por una piel alterada (atrófica, rojiza o roja parduzca). En estas lesiones también está comprometida la sensibilidad de la piel. Además, es frecuente que estas lesiones se ulceren. Es típica la afectación del tracto respiratorio superior, los ojos y la pérdida del vello corpora l, incluyendo las cejas y pestañas, y la deformación del tabique nasal.
Tratamiento para la lepra
El tratamiento de la lepra comprende medidas generales para proteger las áreas en las que el paciente no tiene sensibilidad. Se le explican al paciente los cuidados y prevenciones que debe llevar a cabo para evitar contagios, así como se atiende a las alteraciones psicológicas y sociales que puede padecer de forma crónica.
La pauta del tratamiento farmacológico según el tipo de presentación clínica es:
En la lepra tuberculoide (y la borderline tuberculoide), se pautan dos antibióticos por vía oral , Dapsona y Rifampicina , en distintas pautas de dosificación, manteniendo este tratamiento durante 6-9 meses.
En la lepra lepromatosa (y la borderline lepromatosa), se indica la toma de Clofazimina , Dapsona y Rifampicina , en distintas pautas de dosificación manteniendo este tratamiento durante 24-36 meses.
Pruebas complementarias del tratamiento de la lepra
A parte de la entrevista clínica y la exploración física, se procede a la toma de muestras para su estudio. Así, se coge una muestra del borde de las lesiones para la visualización directa mediante el uso de un colorante de la bacteria presente en el tejido. Además, se pueden realizar biopsias cutáneas (toma de un pequeña porción de tejido alterado), para su estudio por el laboratorio de anatomía patológica y la detección de bacterias. En ocasiones, para diferenciar en qué estadío de la enfermedad está el paciente, se realiza una prueba llamada prueba de la lepromina , con la inyección cutánea de una suspensión de la bacteria de forma inactiva, desencadenando una reacción en la piel característica de cada fase.
Factores desencadenantes de la lepra
El factor desencadenante es el contacto con las secreciones del aparato respiratorio de un paciente enfermo, cuando se establece un contacto cercano y prolongado.
Factores de riesgo de la lepra
Condiciones socioeconómicas bajas.
Hacinamiento.
Bajo grado de escolarización.
Mala higiene e insalubridad.
Desnutrición.
Inmunidad alterada (disfunción de las defensas).
Convivencia con un enfermo de lepra.
Alteraciones metabólicas.
Complicaciones de la lepra
Leprorreacciones : cambios bruscos en la estabilidad clínica del enfermo producidas como consecuencia de una alteración del estado de las defensas del paciente. Existen dos tipos:
Tipo I: aparecen edemas en las lesiones cutáneas y hay mayor afectación neurológica.
Tipo II: aparecen edemas en las lesiones cutáneas y hay mayor afectación neurológica. En la II existen alteraciones cutáneas importantes con aparición de múltiples placas y nódulos, que pueden sufrir grandes ulceraciones, además de surgir mayor inflamación de los nervios periféricos y dolor, acompañado de fiebre y malestar general. Pueden verse afectados los músculos, el hígado, lo ganglios linfáticos, los testículos…etc.
Alteración psiquiátrica: depresión, ansiedad…etc.
Pérdida de visión por la afectación ocular.
Obstrucción nasal, sinusitis crónica y epistaxis (sangrado nasal).
Aislamiento social.
Pérdida de piezas dentales.
Afectación renal.
Prevención de la lepra
Tratamiento o quimioprofilaxis de las personas que conviven con enfermos en la forma más contagiosa, la lepra lepromatosa, administrando un antibiótico , la Sulfona , durante un tiempo prolongado.
Realizar un tratamiento precoz de aquellas personas infectadas para disminuir el riesgo de contacto.
Especialidades a las que pertenece la lepra
La lepra es una enfermedad que puede ser valorada y tratada por el dermatólogo, por el médico de enfermedades infecciosas, el neumólogo, el oftalmólogo, o el neurólogo, en muchas ocasiones de forma conjunta, según la afectación del paciente.
Preguntas frecuentes:
En la actualidad… ¿Sigue existiendo la lepra?
Sí, aparece sobre todo en regiones tropicales y subtropicales. En Europa su aparición está limitada a los países de la cuenca mediterránea.
¿Cómo se contagia la lepra?
La lepra se contagia a través del contacto persona a persona, por medio del contacto con las secreciones respiratorias (mucosidad, goteo nasal, o al estornudar).
En la actualidad… ¿Tiene cura la lepra?
Sí, se utilizan varios antibióticos de forma conjunta (sinérgica) para evitar la aparición de resistencias. El tratamiento se debe mantener hasta que se objetiva mediante análisis que las lesiones cutáneas no presentan bacterias.
¿En qué países es más propensa la gente a contraer la lepra?
Las zonas donde la lepra aparece de forma endémica sobre todo son Asia y América del sur. En Europa, su mayor incidencia aparece en España y Portugal.
¿Qué es la enfermedad de Hansen?
La enfermedad de Hansen es otra forma de denominar a la lepra . Hace referencia al nombre de este médico noruego que descubrió a la bacteria que produce la lepra, el médico noruego Gerhard Armauer Hansen.

Enfermedad
Síndrome de Cushing
¿Qué es el síndrome de Cushing?
El síndrome de Cushing o hipercortisolismo, es la enfermedad que se produce por exceso de cortisol , ya sea por producción excesiva de las glándulas suprarrenales del enfermo, o por efecto yatrógeno, esto quiere decir, como consecuencia secundaria de la administración de fármacos para tratamientos. También hay tumores neuroendocrinos que pueden producir una sustancia similar al cortisol que puede dar lugar a este síndrome. Es un síndrome muy poco frecuente que se producen de entre 35 a 40 casos por cada millón de personas, y se considera una enfermedad grave.
Tipos de síndromes de Cushing
Los tipos de síndrome de Cushing son:
Síndrome de Cushing ACTH (Hormona AdenoCorticoTropa): dependiente, se produce por tumores en la hipófisis o por tumores que provocan que se segregue esta hormona.
Síndrome de cushing ACTH independiente : se produce por tumores suprarrenales o hiperplasia suprarrenal yatrogénicos .
Causas del síndrome de Cushing
La causa es el trastorno hormonal que produce un aumento de cortisol o la toma de manera mantenida de medicamentos que contienen corticoides por enfermedades de origen inflamatorio.
Síntomas del síndrome de Cushing
Son síntomas de síndrome de Cushing: obesidad central, cara de luna llena ( cara redondeada ), acné , hipertensión arterial, diabetes , dolor de espalda , alteraciones en el ciclo menstrual , hirsutismo , impotencia en los varones, aumento de la sed , aumento de la micción , debilidad muscular , estrías de color vino, hematomas frecuentes, debilidad , irritabilidad , depresión , ansiedad y la alteración de la autoestima .
Tratamiento para el síndrome de Cushing
El tratamiento del síndrome de Cushing debe estar enfocado a reducir el nivel de cortisol.
Cuando el nivel de cortisol esté elevado por una causa yatrogénica , esto es, por ingerir medicamentos, el médico desciende la dosis de manera paulatina. Si esto no es posible, se intentará que el paciente consuma la menor dosis posible y se establecerá una vigilancia estrecha de este.
Si la causa es un tumor en la glándula hipofisaria, el médico indicará tratamiento quirúrgico, radioterapia o quimioterapia, según sea necesario.
Cuando la producción se debe a un tumor suprarrenal , el médico indicará un tratamiento quirúrgico para extraer el tumor. Si el tumor no puede extraerse se tratará de bloquear la acción de la hormona mediante medicamentos.
Pruebas complementarias para el diagnóstico del síndrome de Cushing
Las pruebas complementarias para el diagnóstico del síndrome de Cushing consisten en técnicas para medir la cantidad de cortisol:
Análisis de orina de 24 horas.
La prueba de supresión se dará 1 mg. de Dexametasona y se mide el cortisol a las 24 horas. Se puede hacer con 2 mg. de Dexametasona y haciendo la tasación de cortisol a las 48 horas, en ambos casos se realiza sobre sangre venosa ,
Se realizarán también pruebas de imagen, ya sean ecografías, tomografías o escáneres para valorar tanto las glándulas suprarrenales como la hipófisis .
Factores desencadenantes del síndrome de Cushing
El principal factor desencadenante es el exceso de cortisol .
Factores de riesgo del síndrome de Cushing
El principal factor de riesgo para el síndrome de Cushing es la toma indiscriminada de fármacos corticoides de forma diaria.
Complicaciones del síndrome de Cushing
Diabetes mellitus.
Hipertensión arterial.
Disfunción eréctil.
Hirsutismo: desarrollo de vello en cantidad mayor de lo normal.
Depresión.
Ansiedad.
Insomnio.
Alucinaciones.
Ideas paranoides.
Pérdida de memoria.
Prevención del síndrome de Cushing
No tomar fármacos corticoides sin control médico .
Especialidades a las que pertenece el síndrome de Cushing
El especialista en el control del síndrome de Cushing será el especialista en endocrinología . En cuanto al tratamiento, este será responsabilidad, tanto del endocrinólogo, como del cirujano general en los casos de tumores en las glándulas suprarrenales que deben ser extirpados, o bien neurocirujanos en el caso de alteraciones en la glándula hipófisis.
Preguntas frecuentes
¿Qué es el cortisol en el cuerpo humano?
El cortisol es una hormona que, producida por la glándula suprarrenal , se encuentra circulando en la sangre. Aumenta en las situaciones de estrés y actúa elevando el nivel de azúcar en la sangre y disminuyendo la inmunidad. Interviene en el metabolismo de grasas, proteínas y carbohidratos, y también actúa manteniendo en niveles adecuados los iones en sangre, así como la cantidad de agua en el organismo.
¿Qué es la enfermedad de insuficiencia suprarrenal?
La insuficiencia renal es la enfermedad en la que las glándulas suprarrenales no funcionan . Esto da lugar a una menor producción de cortisol, que deberá ser suministrado en forma de medicamento al paciente.
¿Qué es la glándula suprarrenal?
La glándula suprarrenal es una glándula endocrina que se encuentra situada encima de los riñones, de ahí su nombre. Su misión principal es la producción de sustancias como el cortisol, la aldosterona, la adrenalina y noradrenalina. También producen, pero en menor cantidad hormonales sexuales, como los estrógenos y la testosterona.
¿Cuál es la función de la glándula suprarrenal?
La función de la glándula suprarrenal es la producción de hormonas como el cortisol, la aldosterona, la adrenalina y la noradrenalina, que van a controlar el equilibrio de iones del organismo, mantener los niveles de azúcar, regular la respuesta inflamatoria, permitir que el cuerpo responda ante una situación de lucha o huida, mantener el embarazo, y comenzar la maduración sexual durante la pubertad.
¿Dónde se producen los mineralocorticoides?
Los mineralocorticoides son las hormonas que se van a producir en la parte exterior o corteza de las glándulas suprarrenales. Su misión en el organismo es mantener el equilibrio hidroelectrolítico actuando a nivel del riñón. La más importante es la aldosterona .

Enfermedad
Leishmaniasis
¿Qué es la leishmaniasis?
La leishmaniasis es una enfermedad parasitaria producida por la Leishmania , que es un protozoo que se transmite por la picadura de un insecto flebotomo (que se alimenta de sangre). En España se detectan unos 110 casos de leishmaniasis humana al año, se presenta principalmente en casos de adultos y niños inmunodeprimidos. Los perros son el reservorio animal y se considera una enfermedad endémica en los mismos. Es una enfermedad considerada como grave.
Tipos de leishmaniasis
Los diferentes tipos de leishmaniasis son:
Leishmaniasis cutánea : es la forma más común de leishmaniasis y produce úlceras en las zonas expuestas del cuerpo.
Leishmaniasis mucocutánea : conduce a la destrucción de la mucosa de nariz, boca y garganta.
Leishmaniasis visceral o Kala-azar : en un 95% de casos es mortal si no se trata, produce fiebre, pérdida de peso, aumento del tamaño del hígado, del bazo y provoca anemia.
Causas de la leishmaniasis
La causa es la picadura del mosquito flebotomo infectado transmitiendo el protozoo por la picadura.
Síntomas de la leishmaniasis
Los síntomas de la leishmaniasis cutánea son, en primer lugar, un bulto en la zona de la picadura , que posteriormente puede dar lugar a bultos en más zonas. El bulto inicial se irá agrandando y dará lugar a una úlcera costrosa. Estas úlceras pueden curar por sí mismas pasados unos meses, pero dejarán lesiones cicatriciales.
Los síntomas de la leishmaniasis mucocutánea se inician con una úlcera en la piel, que se cura por sí misma, seguida de lesiones en el interior de la nariz , la garganta y la boca , pudiendo producir sangrado.
Los síntomas de la leishmaniasis visceral son: fiebre de forma discontinua, diarrea, pérdida de peso, sensación de cansancio , anemia y aumento de tamaño del hígado del bazo y de los ganglios linfáticos.
Tratamiento para la leishmaniasis
En el tratamiento de la leishmaniasis cutánea se usará terapia de calor o frío sobre las úlceras y Paramomicina en pomada sobre las úlceras. En casos de leishmaniasis más agresiva se pueden usar fármacos intravenosos u orales como el Fluconazol , la Anfotericina B, Estibogluconato de sodio y Miltefosina . Estos mismos fármacos se usan para los caso de leishmaniasis mucocutánea.
La leishmaniasis visceral se trata con Anfotericina B Liposomal , en zonas de América Latina, se usan fármacos con Antimonio , y en casos de resistencia a antimonio se trata con Miltefosina .
Pruebas complementarias del tratamiento de la leishmaniasis
Las pruebas complementarias serán la observación del parásito de las zonas donde se encuentre y también la búsqueda de anticuerpos en la sangre de los pacientes.
Factores desencadenantes de la leishmaniasis
El factor desencadenante es la picadura del flebotomo infectado junto con un estado de inmunodepresión del individuo.
Factores de riesgo de la leishmaniasis
Las malas condiciones de vida y las viviendas insalubres aumentan el riesgo de infección por leishmaniasis. También lo hacen el hacinamiento, ya que este atrae a los flebotomo, así como la malnutrición, la deforestación y el ocupar hábitat previamente boscosos.
Complicaciones de la leishmaniasis
Infecciones intercurrentes.
Osteomielitis (inflamación simultánea de la médula ósea y del hueso).
Meningitis.
Septicemia (infección grave y generalizada de todo el organismo).
Úlceras con cicatrices importantes.
Prevención de la leishmaniasis
Uso de mosquiteras con insecticida en las camas.
Mosquiteras en las ventanas para evitar que entren los mosquitos.
Repelentes de insectos en la piel.
Evitar pasear en las zonas de mosquitos en las horas donde se produce el vuelo del mismo (generalmente al final de la tarde).
Especialidades a las que pertenece la leishmaniasis
La leishmaniasis la tratan especialistas de medicina interna con la subespecialidad de medicina infecciosa.
Preguntas frecuentes:
¿Cuál es el parásito de la leishmaniasis?
Hay tres parásitos de la leishmaniasis que son diferentes según la zona del mundo donde se encuentran, así, encontramos la leishmania donovani, da lugar a leishmaniosis visceral y se da principalmente en el continente indio, China, África e Irak, la leishmania infantum, típica de la cuenca mediterránea europea y africana, y la leishmania chagasi causante de la leishmaniasis visceral en América.
¿Es posible la leishmaniasis en personas o solo en perros?
Sí, es posible tener la enfermedad en personas . La leishmaniasis es una zoonosis, esto quiere decir que desde animales donde se encuentran como pueden ser perros, conejos, zarigüeyas y zorros que tienen la enfermedad, puede pasar al humano, tras ser picados por un mosquito.
¿Cómo se transmite la leishmaniasis?
La leishmaniasis se transmite por la picadura de la hembra del mosquito q ue tiene el parásito . Cuando pica al humano u otro animal va a inyectar el parásito por medio de la picadura.
¿Qué son los antimoniales pentavalentes?
Los antimoniales pentavalentes son el Glucantime (se usa más en el primer mundo) y Pentostam (se usa en países en desarrollo) son los fármacos de primera línea en el tratamiento de la leishmaniasis. Aunque no se conoce bien su mecanismo de acción, parece que actúan alterando el funcionamiento de las enzimas de los protozoos. Se administra en dosis inyectable durante 20 días de forma diaria si se trata de leishmaniasis cutánea y el tratamiento se prolonga hasta 28 días en dosis intravenosa si es leishmaniasis mucocutánea. Son fármacos tanto más efectivos cuanto más rápido se usan tras la infección.
 Savia
Savia