Ginecología y Obstetricia
La especialidadArtículos especializados
Enfermedades
Síntomas
Otros contenidos

Artículo especializado
Alimentación complementaria para bebés
Introducción
A partir del sexto mes aproximadamente, bajo la supervisión y aprobación del pediatra, se inicia la alimentación complementaria , independientemente de si la lactancia es materna, artificial o mixta.
Las necesidades de energía en esta etapa son superiores a los que puede aportar la leche materna, por lo que se hace necesaria la introducción de otras fuentes de energía. Si quieres conocer más sobre la alimentación complementaria, continúa leyendo.
Definición
La alimentación complementaria se considera el proceso mediante el cual se le ofrece al lactante alimentos sólidos o líquidos distintos de la leche materna o fórmula infantil, como complemento y no como sustitución de esta, con el fin de cubrir las necesidades de energía y nutrientes que estas no son capaces de proporcionar y que conlleva cambios metabólicos y endocrinos que influyen en la salud futura del niño.
Los objetivos que se persiguen con la alimentación complementaria son:
Promover el adecuado crecimiento y desarrollo neurológico, cognitivo, del tracto digestivo y del sistema neuromuscular.
Proveer nutrientes que son insuficientes en la leche materna como selenio, zinc, hierro.
Favorecer el desarrollo psicosocial.
Conducir a la integración de la dieta familiar.
Promover hábitos de alimentación saludable.
Promover una alimentación complementaria que prevenga factores de riesgo para obesidad, alergias, desnutrición, hipertensión arterial, síndrome metabólico y diabetes, entre otros.
¿Cuánto debe comer un bebé?
No existe una cantidad inicial de alimentación complementaria por ración, es importante irse dirigiendo por el apetito del niño . Al principio, está conociendo los alimentos, por lo cual, solo tomará una cucharada hasta aceptarlo por lo que no hay que obligarle, ya se irá aumentando la cantidad a ingerir.
Se recomienda iniciar la alimentación complementaria con una comida al día ofrecida en un horario conveniente en donde exista un ambiente tranquilo. La cantidad de comida se incrementa de forma gradual a medida que el niño crece, fraccionándola a lo largo del día de acuerdo a su capacidad gástrica y de la densidad energética del alimento ofrecido. Es importante ofrecer comidas nutritivas y no en exceso para no favorecer el abandono precoz de la lactancia.
¿Cuál es la mejor forma de dar de comer al bebé?
Al comienzo, la alimentación es una experiencia sensorial , ya que, el niño, mediante el tacto y el gusto, aprenderá las diferentes texturas y sabores. Con el tiempo, irá comiendo en mayores cantidades y disminuyendo la proporción de leche materna. Los alimentos, al inicio, deben ser de consistencia blanda, no necesariamente triturados, con un aporte calórico promedio de 30 gramos de proteínas diarias y sin necesidad de realizar una comida especial al resto de la familia, solo apartando la del niño antes de colocarle condimentos fuertes.
¿Cómo se deben ir incluyendo alimentos en la dieta del bebé?
La consistencia más apropiada de la comida del lactante va a depender de la edad y del desarrollo neuromuscular.
Al iniciar los 6 meses, el lactante puede comer alimentos sólidos o semisólidos en forma de puré o aplastados, con preferencia de cereales sin gluten, verduras y frutas. La frecuencia es 2 o 3 veces al día para cubrir en conjunto con la leche unos requerimientos de energía diarios de entre 640 a 750 Kcal/día.
A partir del mes 7 , se agregan proteínas como pollo y legumbres, la textura puede ser picado fino o machacado, hasta 3 veces al día para cubrir unos requerimientos de 770 Kcal/día.
Entre los 8 y 12 meses, es el momento de agregar derivados lácteos, como yogur, huevo y pescado. La textura de la comida ha de ser picada fina o en trocitos, con un total de requerimientos diarios de 705 Kcal/día y, por último, posterior a los 12 meses, se introducen los embutidos y la leche entera.
Tipos de alimentos
VERDURAS Y HORTALIZAS: se inician al sexto mes, a excepción de acelgas, remolacha, nabos y espinacas, por su alto contenido en nitrato.
FRUTAS: se introducen a partir del sexto mes. Anteriormente se retrasaban los cítricos, pero, actualmente, no existe evidencia científica que indique que retrasarlo disminuya el riesgo de alergias. Solo se recomienda una fruta por comida para determinar posibles alergias.
CARNE: se puede comer desde los 6 meses de edad, preferiblemente pollo, pavo y conejo, por menor contenido graso.
PESCADO: por su alto contenido de mercurio, evitar el consumo de peces de gran tamaño.
HUEVOS: su retraso en la alimentación del niño no disminuye el riesgo potencial de alergia. Se recomienda dar su contenido por separado.
Ejemplo de un plan diario
En un bebé de 6 meses:
Día 1 al 3: plátano
Día 4 al 6: calabacín en puré
Día 7 al 9: calabacín y patata en puré
Día 10 al 12: brócoli y patata
Preguntas frecuentes
¿Cómo se puede compaginar la lactancia materna con la alimentación complementaria?
Es importante insistir en que la alimentación complementaria , como su nombre indica, complementa a la leche materna o lactancia artificial por lo que no debe ser sustituida por ningún alimento y, un destete a esta edad, puede traer como consecuencias riesgos en la salud del bebé a largo plazo.
¿Cuántas veces al día se debe recurrir a la alimentación complementa?
Se debe iniciar una vez al día a los 6 meses e ir aumentando paulatinamente a partir de los 9 meses, para culminar a los 12 meses con 4 tomas de comida.

Artículo especializado
Alimentación en la lactancia
Introducción
La lactancia materna es la alimentación ideal para el recién nacido, ya que contiene todos los elementos nutritivos que necesita para su crecimiento y desarrollo, así como sustancias que le protegen contra infecciones.
Es importante, durante este tiempo, comer de forma sana para obtener los nutrientes necesarios que necesitas y producir leche de excelente calidad. Si quieres saber más sobre la alimentación durante la lactancia materna , te invitamos a que continúes leyendo este artículo.
¿Cómo debe ser mi alimentación durante la lactancia?
Existen algunos consejos generales para planificar la dieta en madres lactantes . A continuación, señalamos algunos:
Se deben tomar proteínas 2 o 3 veces al día como carne, pollo, pescado, huevos, productos lácteos y nueces.
Consumir tres porciones de verduras, incluyendo verduras de color verde y amarillas cada día.
Tomar tres porciones de fruta diaria.
Incluir granos integrales como pan, pasta, cereales y avena diariamente.
Los alimentos ricos en calcio como leche, queso y yogur, son importantes consumirlos diariamente.
Tomar solo de forma esporádica alimentos ricos en contenido graso y azúcares, ya que tienen muchas calorías y bajo valor nutricional.
Beber unos dos litros de agua al día, es indispensable para la fabricación de la leche. El zumo de frutos y la leche también son una alternativa para mantenernos hidratados.
Se debe evitar el consumo de cafeína.
Si se desea beber alcohol, se aconseja esperar 3 horas después de amamantar, aunque lo más aconsejable es no ingerir alcohol.
Evitar los alimentos muy especiados o picantes, ya que, pueden producir molestias estomacales al bebé.
La importancia de la vitamina D en la lactancia
La leche materna , como sabemos, es el mejor alimento para los lactantes, pero posee una limitación al no poseer la suficiente cantidad de vitamina D para un metabolismo fosfocálcico adecuado, por esto, desde hace tiempo, se recomienda la suplementación de la madre con dosis altas de vitamina D o al lactante. Si la madre no puede ingerirla o metabolizarla, se debe complementar con 400 unidades diarias de vitamina D para favorecer la absorción de calcio en los huesos y evitar enfermedades como el raquitismo.
Alimentos recomendados durante la lactancia
Los lácteos y sus derivados son recomendados por ser un elemento fundamental para la mineralización ósea del bebé, se deben incluir 4 raciones diarias bajo en grasas.
Las carnes magras, se deben evitar los embutidos.
Pescado al menos 4 veces a la semana, tanto blanco como azul.
Tomar tres o cuatro huevos a la semana si no existe contraindicación.
Cereales, preferiblemente integrales, y legumbres con su aporte proteico y baja cantidad de grasa.
Frutas, verduras y hortalizas deben estar presentes en la dieta cinco veces al día, incluyendo una fruta cítrica.
Aceite de oliva virgen extra en cantidad moderada.
En relación a la bollería, su consumo debe estar indicado puntualmente, ya que aporta calorías vacías sin energía nutricional.
Alimentos a evitar durante la lactancia
Se debe evitar el consumo de pez espada, atún rojo y lucio porque eleva el riesgo de superar la ingesta máxima de mercurio permitida.
Limitar las bebidas con cafeína, ya que, pueden producir irritabilidad, insomnio y temblores en el bebé; su consumo debe estar restringido a menos de tres tazas diarias justo después de la toma de pecho.
Aunque la cantidad de alcohol que traspasa la leche materna es baja, si se ingiere es recomendable hacerlo en cantidades pequeñas de forma esporádica justo después de las tomas.
Alimentos como el ajo, espárragos, cítricos, picantes y cebolla, pueden alterar el sabor de la leche materna, lo cual, no quiere decir que sea desagradable para el bebé como cita el “mito”, sino que se tenga que consumir más cantidad del producto de lo que se hace en circunstancias normales.
En familias con antecedentes alérgicos, se ha encontrado beneficioso que la madre suspenda de la dieta alimentos potencialmente alergénicos como el huevo; esto varía de un individuo a otro, por lo cual, hay que consultar previamente al médico.
Ejemplo de dieta
DESAYUNO: tortilla de espinacas + 2 tostadas de pan integral + leche
A MEDIA MAÑANA: 1 plátano
COMIDA: 200 g de pavo + arroz integral + lentejas + ensalada cruda + manzana
MERIENDA: macedonia de fruta
CENA: salmón a la plancha + zanahoria cocida + arroz + mandarina
Preguntas frecuentes
¿ Es recomendable seguir una dieta durante el periodo de lactancia ?
Durante el periodo de lactancia solamente vamos a seguir las pautas nutricionales que iniciamos durante nuestro embarazo, si nos fijamos en los alimentos recomendado y sus porciones es una dieta equilibrada para cualquier persona.
¿Puedo ingerir alimentos con cafeína o alcohol durante la lactancia?
Con respecto a la cafeína, debería limitarse el consumo a menos de tres tazas diarias y después de las tomas del bebé, aunque se debe suspender si lo notamos irritable. En relación al alcohol , aunque traspasa en escasa cantidad a la leche materna, no es recomendable su uso continuo en grandes cantidades. Si se va a ingerir, debe ser después de las tomas de leche y en pequeña cantidad.
¿Ser vegetariano o vegano puede afectar a la leche materna?
Las dietas vegetarianas bien planificadas son saludables y nutricionalmente adecuadas , y pueden proporcionar beneficios para la prevención y tratamiento de enfermedades crónicas, incluyendo embarazo y lactancia. Las mujeres vegetarianas necesitan durante el embarazo y lactancia fuentes regulares de vitamina B12 y de ácido docosahexaenoico. Es importante una buena proporción de vitaminas, minerales y algas dejadas en remojo previamente y bien cocidas, asegurarnos un buen aporte de calcio con sésamo, brócoli, tofu, col verde, perejil, almendras, judías blancas, col china, espinacas y, de aminoácidos, a través de legumbres y frutos secos.
Artículo especializado
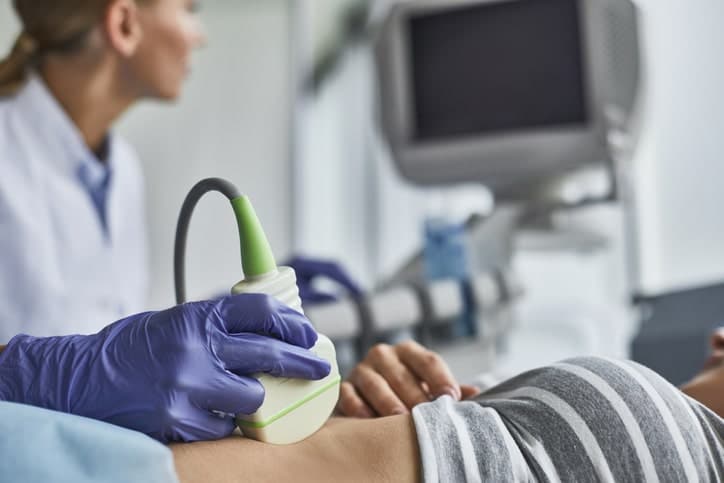
Qué es y Cómo se hace una Ecografía Transvaginal
El término ecografía se refiere a un “gráfico” dibujado gracias a los ultrasonidos, es decir, usando ultrasonidos podremos confeccionar una imagen de la persona explorada. Los ultrasonidos son unas ondas sonoras de alta frecuencia, que se difunden por los órganos blandos. En cambio, no se transmiten por el aire ni por los órganos que no contienen agua, como los huesos.
Hazte una ecografía transvaginal sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
Cómo funciona
El ultrasonido atraviesa el tejido del territorio que abarca y se va encontrando con diferentes órganos de distinta consistencia, en función de su densidad las ondas de ultrasonidos rebotarán sobre ellos en una frecuencia u otra. El mismo transductor recoge las ondas que le vienen devueltas y con esa información el software del ecógrafo confecciona una imagen que se representa en una pantalla. La imagen obtenida será un plano anatómico en dos dimensiones a modo de sección del espacio explorado.
Es el mismo principio que usan los murciélagos para orientarse, o los radares de los aviones. El dispositivo que emite y recibe los ultrasonidos se llama transductor , que se apoya sobre el paciente en la zona próxima al órgano a estudiar, a la que se la ha aplicado previamente un gel acuoso que permitirá que se transmita por ella la onda, pues como hemos comentado no habría una buena difusión de esa energía sobre una zona seca, pues el ultrasonido requiere la presencia de agua para propagarse.
Cómo es esta prueba
Se trata de una prueba inocua, indolora, que no tiene ningún efecto sobre los tejidos a estudiar, que se interpreta “en directo” mientras el ecografista va explorando los distintos planos anatómicos de los órganos objeto de diagnóstico.
Según el tejido que interese estudiar se han diseñado distintos transductores con formas diversas y que usan longitudes de onda distintas según la profundidad que deseemos explorar.
Por ejemplo, los estudios abdominales clásicos usan unos transductores convexos, de cierta amplitud, para poder abarcar el máximo de órganos posibles, pero para explorar zonas más cercanas a la piel podemos usar un transductor más pequeño y de superficie plana que no profundice pero que nos ofrezca imágenes más detalladas de la zona cercana al transductor, por ejemplo, para realizar una ecografía del tiroides o de la mama.
Del mismo modo se han desarrollado transductores de forma alargada y estrecha, para poder introducirse en espacios anatómicos estrechos y acercarnos lo más posible al órgano a explorar. Este es el caso de los transductores transvaginales o transrectales, para explorar los genitales internos de la mujer o la musculatura del esfínter rectal o la próstata.
La ecografía transvaginal se realiza con un transductor alargado de poco grosor con bordes anatómicos y extremo convexo que se introduce unos 10 cm en el interior de la vagina hasta entrar en contacto con el fondo de la misma y por tanto en contacto directo con el útero. Las imágenes que así obtenemos del útero y los ovarios tienen muchísima más resolución que cuando las exploramos por encima de la piel del abdomen.
Hazte una ecografía transvaginal sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
Qué se requiere para realizarla
Este tipo de exploración el único requisito que requiere es que la vagina sea explorable, es decir, que la paciente haya iniciado relaciones sexuales o que el himen no ofrezca resistencia y permita la entrada del transductor. En ese caso la exploración se realiza cómodamente provocando mínima o ninguna molestia a la paciente. El transductor lo podemos mover lateralmente haciendo un barrido derecha-izquierda y anterior-posterior, explorando todo el espacio que ocupan el útero y ambos ovarios y trompas permitiendo diagnosticar patologías de esos órganos con mucha precisión y embarazos desde etapas muy tempranas.
Es obvio que para poder realizar esta exploración de forma segura hay que cubrir el transductor con un preservativo desechable con cada paciente para evitar el riesgo de transmisión de enfermedades.
La alternativa ecografía ginecológica desde la superficie de la pared abdominal de la paciente para obviar la introducción del transductor en la vagina requiere que la vejiga urinaria esté completamente llena de orina pues sin ella el aire que contienen los intestinos interfiere en la difusión de los ultrasonidos impidiendo su difusión y por tanto la obtención de buenas imágenes. Si por el contrario l a vejiga está llena ocupa todo el espacio a explorar desplazando más arriba los intestinos y actuando a modo de pantalla sobre el útero y los ovarios permitiendo que sean explorados con precisión.
Este requerimiento de vejiga completamente llena no está exento de molestias para la paciente, que tiene que beber aproximadamente un litro de líquido una hora antes de la exploración lo cual hace que la paciente misma prefiera la vía transvaginal.
El abordaje vaginal nos permite ser mucho más precisos y explorar con mayor fidelidad órganos profundos acercándonos a ellos sin ocasionar graves molestias a la paciente. Es una exploración ampliamente difundida y usual actualmente en cualquier consulta ginecológica.
Hazte una ecografía transvaginal sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
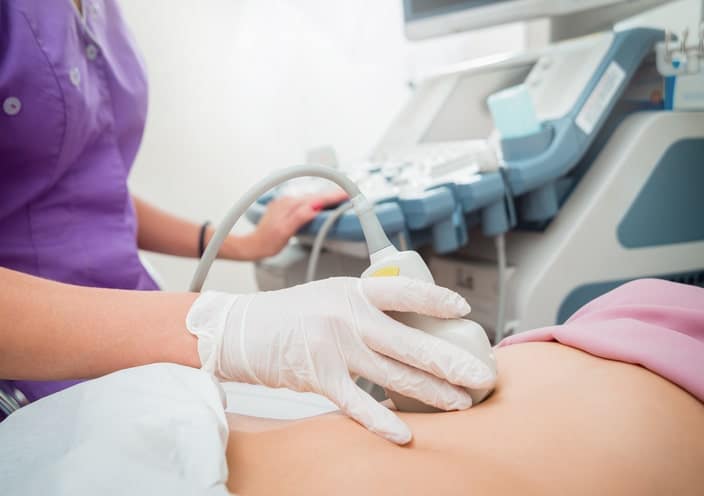
Artículo especializado
Qué se Puede Ver en una Ecografía 4D
La ecografía es un método de diagnóstico por la imagen muy útil en medicina y veterinaria. Está basado en la emisión y recepción de ondas de baja frecuencia que se llaman ultrasonidos, por eso también se le llama ultrasonografía.
Hazte una ecografía 4D sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí
Cómo funciona
Estas ondas son emitidas por un dispositivo llamado transductor que se apoya sobre el paciente, atraviesa sus tejidos, y según la densidad de los órganos que va encontrando en su avance rebotan y vuelven al punto de partida con información que el ordenador del ecógrafo compondrá para emitir una imagen en una pantalla, que será el gráfico anatómico del espacio estudiado.
El ultrasonido se propaga por medios acuosos, no obtiene imágenes de calidad si atraviesa aire o hueso. Por ello es necesario cubrir la piel del paciente con un gel acuoso que hará de medio para la propagación de las ondas. Y por este motivo es un método más adecuado para ciertos órganos que otros. Nos ofrece buenas imágenes de músculos, vísceras sólidas, y el ejemplo más claro, el feto, que al estar sumergido en la bolsa de las aguas es el sujeto ideal para ser explorado.
De la 2D a la 4D
Este es el principio de la ecografía clásica, que podemos llamar 2D, es decir, que la imagen obtenida es un plano de 2 dimensiones. Desde los primeros ecógrafos se ha evolucionado infinitamente, obteniendo de los aparatos de última generación imágenes de altísima resolución. A partir de este mismo principio físico y modificando la fuente emisora de los ultrasonidos, para enviar en lugar de un plano de ultrasonidos un bloque de los mismos y también modificando el software que lo convierte en imagen podemos obtener imágenes en 3 dimensiones, 3D, dando sensación de profundidad. Un paso más allá fue poder explorar en movimiento esas imágenes 3D que inicialmente eran fijas, con lo que añadiendo la dimensión temporal se pudo empezar a hablar de imágenes 4D, que actualmente ya se han sustituido por las 5D, con ecógrafos de última generación que construyen una imagen en profundidad, movimiento y textura que da la impresión de ser real.
Cualquiera de las exploraciones 2D, 3D, 4D o 5D usan el mismo principio físico, que no tiene ningún efecto sobre los tejidos que explora, así pues, es una prueba segura e inocua tanto para el ecografista como para los/las pacientes y fetos.
Hazte una ecografía 4D sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí
Qué se obtiene
Esta posibilidad de componer las imágenes con efecto tridimensional y su inocuidad la han hecho ideal para explorar la anatomía fetal. Con la ecografía 4D-5D se obtienen imágenes de gran resolución de la superficie anatómica del feto, de su cara, manos, pies, genitales… en movimiento, permitiendo al público no entrenado identificar claramente sus rasgos y gestos, si abre la boca, bosteza, sonríe, etc. Esto la ha popularizado para hacer ecografía de carácter “lúdico” durante el tercer trimestre de embarazo simplemente para disfrutar de la visión del feto. Actualmente con el perfeccionamiento del procesamiento de las imágenes es impresionante la verosimilitud y el aspecto real que nos ofrece del feto. Pero para ello hace falta una mínima “colaboración” del bebé… es sumamente sensible a factores externos: una mala posición fetal mostrándonos la espalda, la escasez de líquido amniótico en la zona que queremos mirar o su proximidad a la placenta, o simplemente que coloque sus extremidades por delante pueden arruinarnos la experiencia. Por este motivo no siempre se consigue a la primera, y son frecuentes los casos en que se recita a la paciente para otra ocasión esperando tener mejor suerte.
Posibilidades médicas
Pero dejando de lado este aspecto festivo de la ecografía 4/5D existe otro mundo de infinitas posibilidades desde el punto de vista médico. Obviamente la convierte en la exploración ideal para comprobar malformaciones de la superficie de la anatomía como pueda ser un labio leporino (malformación facial del feto en que el labio superior, y en ocasiones también el paladar está partido). Actualmente el rastreo anatómico se realiza en 2D, pero el apoyo del 4D en estas ocasiones puede ser de ayuda, y sin duda ilustrativo para mostrar a los futuros padres el alcance de la lesión.
La ecografía 4D también permite el almacenaje de volúmenes, es decir grabar esos datos para una vez finalizado el estudio y en ausencia ya de la paciente volver a ellos y poderlos reproducir desde otros ángulos de visión y perspectivas diferentes que nos permitan aumentar las posibilidades diagnósticas, tanto en la exploración de un feto como de un órgano concreto.
Es decir que la aplicación de la ecografía 4/5D para disfrutar de imágenes muy reales del feto está en auge, pero en realidad constituye la punta del iceberg de las posibilidades que nos ofrece tanto en obstetricia como en muchas otras especialidades.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Hazte una ecografía 4D sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí

Artículo especializado
Cómo Funciona el Método Ropa
El método ROPA es el acrónimo de Receptora de Óvulos de la Pareja. Se refiere a las parejas de mujeres homosexuales que desean un embarazo en común y una de ellas actúa como donante de óvulos para su pareja (madre genética) y la otra gesta el embarazo en su útero (madre biológica).
Tiene un requisito legal: según la legislación española, para poder realizar esta técnica la pareja debe estar casada legalmente, no sirve ser pareja de hecho. Este detalle es importante y puede llamar la atención, pero simplemente es una formalidad pues en nuestro país hay una norma muy estricta según la cual cualquier donación de órganos, semen u óvulos, ha de ser anónima, y la única excepción es esta técnica, que lo permite. Asimismo, legalmente al hacer este tipo de tratamientos ambos miembros de la pareja se hacen responsables del hijo/a y así deberán inscribirlo como común en el libro de familia.
Cuándo se indica este método
Las indicaciones son múltiples, simplemente para implicarse ambos miembros de la pareja y compartir los roles por elección personal . O por motivos médicos, en caso de que la receptora presente baja reserva ovárica o alteraciones en la calidad ovárica o cualquier tipo de enfermedad hereditaria o alteración genética o cromosómica o que sea portadora de alguna mutación que pueda ser heredada a la descendencia. O simplemente cuando han fallado previamente otros ciclos de tratamiento de fertilidad. O porque la donante presente alguna patología médica u obstétrica que contraindique embarazo o que condicione que el embarazo sea de riesgo.
Debe cumplirse, simplemente por sentido común, que la que dona sus óvulos tenga un buen perfil de donante, es decir, a nivel genético no tenga problemas y a nivel ginecológico tenga buena edad y buena reserva ovárica. Y que la receptora no tenga problemas de salud que puedan verse comprometidos con un embarazo y que su útero no presente patología que contraindique la gestación.
Fases del método
Desde el punto de vista técnico hay que recurrir a una fertilización in vitro en varias fases:
La paciente que actúa como donante de óvulos se ha de someter a un tratamiento de estimulación ovárica con una medicación que lo que pretende es que en el ovario durante la primera parte de un ciclo se desarrollen cuantos más óvulos mejor. Se realiza un control ecográfico regularmente, cada 48-72 horas de los ovarios para ir haciendo seguimiento de su evolución. En el momento óptimo de madurez de los óvulos se administra otra medicación que nos asegura que estén aptos para ser extraídos en el momento en que se programe su extracción. Esta se realiza en un quirófano, habitualmente bajo sedación y mediante la punción de los ovarios por vía vaginal guiándonos por ecografía, puncionando cada uno de los folículos, que son las bolsitas de líquido del ovario en el interior de las cuales flota el óvulo. Se aspira su contenido, con el óvulo incluido y se le entrega al laboratorio, donde se conservarán para su fecundación.
En el laboratorio se incorpora a los óvulos una muestra de semen de donante anónimo para que un espermatozoide fertilice cada uno de ellos, a partir de ese momento se conservaran los embriones en medios de cultivo y bajo unas estrictas condiciones de humedad y temperatura. Se va supervisando su evolución durante los primeros días. Los embriones sanos se van dividiendo de forma uniforme y a una velocidad concreta, y a los tres o cinco días podremos escoger los que han tenido mejor evolución y aspecto para transferir el o los mejores. Cada vez es más común transferir un solo embrión porque cada vez los resultados de los tratamientos son mejores, sobre todo en este tipo de pacientes, las cuales no tienen por qué tener ninguna dificultad en gestar y en general tienen mejores resultados que las parejas heterosexuales que cuando recurren a tratamientos de fertilidad es cuando sí que han presentado problemas. De esta manera se ha reducido mucho la tasa de embarazos múltiples que eran tan frecuentes hace unos años motivados por la transferencia de múltiples embriones para aumentar la tasa de éxitos.
Paralelamente, el otro miembro de la pareja, la receptora, tiene que recibir un tratamiento con estrógenos orales o transdérmicos (parche cutáneo) para madurar el endometrio y que esté condiciones idóneas en el momento de la transferencia. Seguramente será necesario hacer algún control ecográfico para asegurarnos de que evoluciona correctamente. En el momento en que el embrión esté listo para ser transferido se introducirá suavemente mediante una cánula en el interior del útero de la receptora en un procedimiento ambulatorio que no requiere de anestesia. Las primeras semanas se deberá administrar una medicación para mejorar la implantación y mantenimiento del embarazo.
Si todo funciona habremos obtenido un embarazo en el cual ambos miembros de la pareja tienen un importante papel.

Artículo especializado
Cuándo se Recomienda el Diagnóstico Genético Preimplantacional
El diagnóstico genético preimplantacional o DGP es una técnica diagnóstica que permite detectar alteraciones en la estructura o número de cromosomas o enfermedades genéticas en células embrionarias de embriones que se han conseguido mediante un ciclo de fecundación in vitro.
En qué consiste
Necesariamente, para poder realizar esta técnica diagnóstica debemos recurrir a un ciclo de fecundación in vitro. A grandes rasgos, este tratamiento consiste en someter a la mujer a un tratamiento para inducir el desarrollo del máximo de óvulos en su ovario y, cuando estén en el momento óptimo de maduración, extraerlos y conservarlos en el laboratorio. El proceso de extracción es una punción guiada por ecografía de los ovarios por vía vaginal, aspirando el contenido de las distintas bolsitas de líquido que habrán crecido y en el interior de las cuales flota un óvulo. Este procedimiento se realiza habitualmente en el quirófano y con la paciente sedada. Una vez nos hemos hecho con los óvulos los pondremos en contacto con una muestra de semen de la pareja, o de banco si es el caso, para fertilizarlos. A partir de este momento consideramos que ya se trata de un embrión que va dividiéndose y multiplicando su número de células mientras se mantiene en cultivo en el laboratorio hasta el quinto o sexto día en que es ya un buen amasijo de células, todas iguales de momento, llamado blastocisto.
Si es necesario un DGP, se toman unas cuantas células representativas del embrión para realizar la biopsia, y el blastocisto se congela (vitrifica) para dar tiempo a obtener el resultado y transferirlo diferidamente si se comprueba que es sano. El hecho de extraer cierto número de células del embrión no lo daña ni compromete su evolución, pues en este estadio de crecimiento todas las células todavía son iguales. Eventualmente se puede realizar la biopsia de una parte muy concreta del óvulo (corpúsculo polar) en lugar de células embrionarias si el caso lo requiere, pero con peores resultados.
Las células extraídas son sometidas a distintas técnicas de laboratorio según lo que necesitemos detectar y una vez obtenido el resultado se descartan los embriones que no eran sanos y se seleccionan los que no presentan anomalías para una vez preparado el endometrio de la paciente en un ciclo posterior transferirlo al interior del útero para t ener las máximas posibilidades de embarazo y llegar a término de un recién nacido sano.
La fiabilidad de la técnica es prácticamente del 100%.
Cuándo se indica
Hay unos contextos muy concretos en los que puede estar indicado realizar un DGP:
Por un lado, cuando tenemos motivos para pensar que el embrión pueda presentar alteraciones genéticas:
En casos en que conocemos que uno de los progenitores es portador de una alteración en su fórmula cromosómica , o en casos de que uno o ambos progenitores son portadores de una mutación responsable de una enfermedad genética en el feto, como la hemofilia, la fibrosis quística o cualquier enfermedad genética diagnosticada en la familia que planifica el embarazo.
En pacientes a las que se han realizado ciclos previos de fertilización in vitro aparentemente con buenas expectativas y que han sufrido abortos de repetición o fallos de implantación de los que se desconoce la causa.
En pacientes de edad avanzada, pues a mayor edad más riesgo de alteraciones numéricas en los cromosomas de los óvulos.
En casos de esterilidad masculina de origen genético.
En parejas que en gestación anterior han presentado una anomalía genética.
Existe otro supuesto en que legalmente se puede realizar un DGP más delicado: en casos de familias con un hijo con una enfermedad grave que pueda beneficiarse del tratamiento con células madre de cordón umb ilical de un hermano histocompatible. Se puede realizar un DGP y seleccionar los embriones que presentan compatibilidad de tejidos con el hermano enfermo, con la finalidad terapéutica de que en el momento del parto se pueda recoger sangre del cordón umbilical rica en células madre que en este caso servirán para hacerle tratamiento al hermano mayor.
El poder realizar un DGP es un procedimiento que está regulado por ley. En España existen unos requisitos que se han de cumplir de forma indispensable para autorizar un DGP y son:
Que el embrión tenga probabilidades de tener una enfermedad de aparición temprana.
Que esta enfermedad no sea curable en la actualidad.
Que esta enfermedad sea potencialmente mortal.
Fuera de estos tres supuestos el caso ha de ser presentado ante un Comité de Bioética y ser estudiado y aprobado por éste antes de ser autorizado el DGP.
El DGP no corrige ningún problema ni tiene ninguna capacidad de modificar el resultado, se trata simplemente de seleccionar los embriones que no presentan anomalías para evitar el nacimiento de niños con enfermedades que se pueden diagnosticar a priori, nada más alejado de tener hijos a la carta.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.

Artículo especializado
En qué Consiste el Tratamiento con Embriones Congelados
En el marco de los tratamientos de reproducción asistida, hay ocasiones en que es necesario conservar embriones en el laboratorio. El proceso que se usa para ello es la vitrificación, que ha supuesto un avance respecto al método clásico de congelación lenta que se empezó a emplear en los años 80 y que ofrecía peores resultados.
Actualmente, para la criopreservación tanto de óvulos como de embriones se utiliza la congelación ultrarrápida. Para ello, después de la obtención de la muestra a congelar, se trata con una sustancia para evitar la formación de cristales durante la congelación, que dañarían al óvulo o embrión, y se introducen en los recipientes donde permanecerán congelados en un tanque de nitrógeno líquido a -196º. Este proceso se llama vitrificación, y permite mantener en buenas condiciones embriones y óvulos durante tiempo indefinido con una altísima tasa de viabilidad cuando se descongelan.
Los buenos resultados de esta técnica han hecho cambiar algunos de los planteamientos de la reproducción asistida, pues los resultados con estos embriones son prácticamente equiparables a cuando se transfieren los embriones en fresco.
¿Qué ventajas nos aporta la posibilidad de criopreservar los embriones?
Cuando se realiza una fertilización in vitro la paciente es sometida a un tratamiento en el que pretendemos forzar al ovario a producir cuantos más óvulos mejor para “rentabilizar” ese ciclo al máximo. Después de que adquieran su ideal estado de madurez se procederá a su extracción mediante una punción guiada por ecografía de los ovarios, bajo sedación, aspirando cada uno de los óvulos producidos, que pueden ser según la edad y perfil de la mujer desde unos pocos hasta ¡algunas decenas! Estos ovarios que han sido estimulados en algunos casos pueden darnos complicaciones si la mujer queda gestante en este mismo ciclo. En algunos casos es más prudente esperar a que los ovarios vuelvan a la normalidad y transferir los embriones en un ciclo posterior. Esto es posible gracias a la criopreservación.
Hay veces en las que hay que realizar un estudio a los embriones antes de transferirlos, por ejemplo, cuando haya que descartar anomalías cromosómicas o enfermedades genéticas. Estos estudios necesitan tiempo, y en estos casos el poder criopreservar los embriones, y transferirlos cuando ya tenemos resultados, lo hace posible.
En un tratamiento de fertilización in vitro se obtienen múltiples embriones, se transferirá el de mejor calidad y el resto se criopreservan. Si no ha habido éxito y la mujer no queda gestante se prepara un nuevo ciclo en el que no hay que estimular los ovarios de nuevo, sino que se prepara simplemente el endometrio y se transfiere uno de estos embriones criopreservados. Este segundo tratamiento es mucho menos complejo y de esta manera se reduce en gran medida la tasa de embarazos múltiples que era tan común en tratamientos de fertilización in vitro pues sin la criopreservación de los embriones restantes se forzaba más la transferencia de varios embriones para aumentar las probabilidades de embarazo.
De igual manera, la pareja que ya se sometió a un tratamiento con éxito y se plantea un nuevo embarazo puede rescatar uno de estos embriones sin necesidad de volver a empezar.
En ocasiones, el tratamiento ha dado buenos embriones, pero las condiciones del endometrio no parecen las óptimas para tener éxito. En este caso podemos criopreservar y transferir en otro ciclo con una mejor preparación.
Qué hacer con los embriones sobrantes
Cuando se realiza un tratamiento de fertilización in vitro los embriones sobrantes se criopreservan. La pareja en ese caso decide si los conserva para sí, y se hacen responsables de los gastos del mantenimiento de los mismos o, alternativamente, si no desean utilizarlos en el futuro para su proyecto reproductivo común, pueden escoger entre tres opciones:
Donación a otras parejas o mujer que lo requieran: parejas que tienen problemas de fertilidad de causa tanto femenina como masculina requieren de una donante de óvulos y un donante de semen, o bien han de adoptar un embrión. O una mujer que decida gestación en solitario y que con óvulos propios no sea posible. Esta opción sólo es viable si la mujer que dona los óvulos es menor de 35 años en el momento de la criopreservación. Estas receptoras de embriones simplemente tendrán que preparar su endometrio sin que tengan que estimular sus ovarios, por lo que el tratamiento se simplifica, y como se trata de óvulos jóvenes los resultados son muy buenos.
Donación con finalidad científica para investigación.
Cesar su conservación sin que se utilicen para ninguna otra finalidad en el momento en que la receptora ya no reúna los requisitos clínicos para un nuevo embarazo.
Como siempre, los avances tecnológicos nos abren opciones que previamente no se podían plantear ampliando el abanico de posibilidades y permitiendo tratamientos más seguros y exitosos.

Artículo especializado
Para qué Sirve una Ecografía Obstétrica
Una ecografía es una prueba de imagen que utiliza ultrasonidos, no lleva radiación y, por tanto, no es perjudicial para el feto. En la ecografía se emiten sonidos con una frecuencia mayor a la que es capaz de captar el oído humano y por ello se llaman ultrasonidos. La diferencia entre la forma en que se refleja en cada tejido emite ecos diferentes y todo ello procesado en el ordenador que llevan incorporados los aparatos nos da una imagen en la pantalla.
La ecografía se utiliza en radiología para el estudio de diferentes órganos y aparatos del cuerpo humano y es muy utilizada en el control de embarazo, se llama ecografía obstétrica.
Hazte una ecografía obstétrica sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
Dependiendo del tamaño del útero y del órgano o tejido que queramos estudiar utilizaremos dos vías distintas para la exploración:
Transvaginal: se utiliza un transductor que se introduce en la vagina y puede observar mejor las estructuras cercanas a la vagina. Se utiliza en el estudio del primer trimestre de embarazo, para valorar el cuello del útero o bien para valorar las estructuras fetales colocadas en la parte más inferior del útero.
Abdominal: se utiliza un transductor convexo. Se suele realizar a partir del segundo trimestre ya que hasta entonces es más útil la vía transvaginal.
El número de ecografías a realizar depende de cada gestación y de los factores de riesgo, pero s e establece generalmente que el mínimo de ecografías por gestación es de tres, una por trimestre y cada una tiene una función específica.
Ecografía del primer trimestre
Se suele realizar entre las 11 y 13 semanas y es muy importante definir varios parámetros. Ante todo, si se trata de una gestación viable, es decir, con un embrión que está vivo, con un corazón que late correctamente . Se deben definir el número de embriones presentes, y en caso de gestaciones múltiples (gemelares o de trillizos) la corionicidad, es decir, cuántas placentas hay, y si tiene cada embrión su bolsa amniótica o bien la comparte, ya que estos datos indicarán el factor de riesgo del embarazo.
Se debe medir el tamaño del feto desde el cráneo hasta el coxis, el llamado CRL, y con esta medición se define el tiempo de gestación, si coincide o no con la fecha de última regla o bien si debe modificarse este dato.
En esta ecografía se realiza un repaso morfológico del embrión en que debemos observar unas estructuras básicas con aspecto de normalidad, como son la cabeza con todo el cráneo íntegro y así descartar defectos del cráneo como anencefalias. Debemos visualizar un tórax y un abdomen de aspecto normal y con paredes íntegras y descartar defectos de la pared abdominal que hagan que las estructuras del abdomen se encuentren fuera de la cavidad abdominal fetal como son la gastrosquisis o bien onfalocele, y solemos observar el estómago y la vejiga de la orina. Debemos visualizar las cuatro extremidades de aspecto correcto y con todos los huesos largos. Posteriormente, se realiza un examen a consciencia de los marcadores fetales de cromosomopatía, es decir las alteraciones ecográficas que indican un aumento del riesgo de feto afecto de síndrome de Down. El marcador más importante es el pliegue nucal, que se mide con el feto de perfil, intentando visualizar el hueso nasal en el corte y se mide un espacio que se observa en la nuca del feto. Se pueden estudiar otros marcadores de alteración cromosómica como son el Doppler del ductus venoso o el paso de sangre a través de la válvula tricúspide del corazón.
Hazte una ecografía obstétrica sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
Ecografía del segundo trimestre
Se realiza entre las 19 y las 22 semanas de embarazo y se suele realizar de forma abdominal. En esta ecografía lo primero a realizar es confirmar la viabilidad fetal, la posición del feto, es decir si está situado de forma transversal en el abdomen de la gestante o bien longitudinal (que puede estar de nalgas o bien con la cabeza hacia abajo, en cefálica). Se observa la localización de la placenta y su inserción y la cantidad del líquido amniótico. Se realizan medidas del feto que, como mínimo, son: la cabeza, el abdomen y el fémur, y con ello se confirma que el crecimiento sea correcto . Además, se realiza un estudio más detallado de la morfología fetal, sobre todo de estructuras cerebrales, de estructuras del corazón y otros órganos como los riñones, intestinos… En algunos centros se mide además la longitud del cuello del útero para valorar el riesgo de prematuridad y las arterias uterinas para saber el riesgo de hipertensión del embarazo.
Ecografía del tercer trimestre
Se realiza sobre las 34 semanas aproximadamente y suele ser abdominal. En esta exploración se determina la viabilidad y la posición fetal como en el segundo trimestre. Además, se estudia la inserción de la placenta y la cantidad de líquido amniótico. Se realizan también mediciones del feto para estudiar su crecimiento y un repaso a la morfología ya que algunas malformaciones pueden ser de aparición tardía.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Hazte una ecografía obstétrica sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí

Artículo especializado
Cuándo Debe Practicarse un Legrado Uterino
El legrado uterino también se puede llamar raspado uterino y es una intervención quirúrgica ginecológica que se realiza para estudiar la parte más interna del útero el endometrio o bien evacuar tejidos de dentro del útero.
Podemos dividir los legrados en dos tipos básicos: el ginecológico y el obstétrico . El ginecológico suele ser para estudiar tejido del interior del útero en casos de menstruaciones irregulares o sangrados después de la menopausia, y el obstétrico se realiza en casos de abortos diferidos o incompletos o bien después de un parto.
Indicaciones de un legrado uterino ginecológico
Reglas abundantes o sangrado menstrual anormal entre reglas. Con el legrado se consigue tejido endometrial para su estudio y posterior tratamiento de las irregularidades.
Sospecha de pólipo endometrial. En la ecografía puede haberse observado una imagen compatible con un pólipo endometrial que se extirpa con un legrado y se remite para su estudio.
Sangrados después de la menopausia que requieren estudio del endometrio para descartar procesos malignos en este tejido.
Indicaciones de un legrado obstétrico
Aborto diferido: es decir, la embarazada no tiene sangrado o bien es escaso y en la ecografía se constata una gestación no evolutiva, es decir que el embrión ha dejado de latir o bien no ha crecido embrión dentro del saco gestacional (huevo huero)
Aborto en curso: la gestante acude por sangrado abundante y en la exploración se constata que el tejido gestacional está siendo expulsado, puede ser que esté ya en el cuello del útero a punto de ser expulsado.
Aborto incompleto: la gestante ha tenido sangrado abundante y ha expulsado el saco gestacional y el embrión si lo había, pero no todo el tejido gestacional de la placenta… y el riesgo de sangrado y de infección es alto.
Aborto voluntario: la gestante decide interrumpir una gestación de curso normal antes de las 12 semanas.
Sangrado postparto o postcesárea: en algunos casos después de un parto o una cesárea el sangrado del útero es superior al deseado y la paciente corre peligro de perder un volumen demasiado alto de sangre por lo que se realiza un legrado, se extrae todo el tejido que quede en el interior y el útero suele contraerse mejor y dejar de sangrar.
Retención total o parcial de la placenta: en algunas ocasiones en el momento del parto o bien en la visita del postparto se observa una parte de la placenta que no ha sido expulsada del todo y produce sangrados intermitentes que no cesan por lo que se realiza un legrado y se extraen los restos de dentro del útero.
¿Cómo se realiza un legrado?
Es una intervención que generalmente se realiza bajo anestesia general por lo que la paciente debe estar en ayunas de al menos ocho horas. El primer paso es la dilatación del cuello uterino y para ello en ocasiones se administra una medicación vía vaginal que favorece este paso. Se coloca una pinza en el cuello de la matriz para traccionar y se introducen unos dilatadores (que son como unas varillas) por el cuello, al principio más delgados y progresivamente más gruesos. Una vez conseguida la dilatación deseada se introduce una cureta que es un instrumento quirúrgico en forma de cuchara hueca que rasca por su borde de forma que se rasca contra las paredes uterinas y se consigue el material deseado para el estudio.
Una vez finalizada la intervención la paciente pasa a una sala de control postquirúrgico en que se monitorizarán sus constantes vitales, las pérdidas de sangre y el dolor que se pueda tener. Se administra medicación para las molestias si son necesarias y una vez está controlada y se considera que está en condiciones de volver a su domicilio se le da el alta.
Posibles complicaciones de un legrado
Reacciones alérgicas a la medicación.
Infecciones por la intervención en una cavidad estéril.
Hemorragia o sangrado excesivo.
Perforación uterina: el proceso de dilatación del cuello uterino se realiza forzando el orificio interno del cuello de la matriz y cuando está muy rígido y cerrado puede producirse daño en el tejido adyacente o bien perforación del fondo del útero por la fuerza empleada. El tratamiento de esta complicación generalmente es médico y precisa sólo de la administración de medicación que ayuda a contraer el útero.
Síndrome de Asherman: cicatrices dentro de la cavidad uterina que producirán adherencias entre la cara anterior y posterior de la cavidad.
Cuidados a domicilio tras un legrado
Puede ser que tenga algo de malestar abdominal y dolor como de regla. No debería ser un dolor mayor que el de una regla. Si produce un dolor a nivel de todo el abdomen debería acudir a su médico o bien a urgencias.
Si han indicado tratamiento antibiótico se debe completar toda la duración indicada. En caso de fiebre deberíamos contactar con el médico o acudir a urgencias.
No se debe introducir nada en la vagina durante al menos dos semanas, como tampones, realizar duchas vaginales ni tener relaciones sexuales. Se deben evitar también los baños (que no duchas) estas dos semanas, ni bañera, ni piscina ni mar.

Artículo especializado
Estudios de Fertilidad
Los estudios de fertilidad son una batería de pruebas que permiten valorar las dificultades de una mujer o una pareja para lograr descendencia. Primero de todo conviene diferenciar entre dos términos que se confunden con frecuencia y que, pese a que en el día a día se utilizan como sinónimos, definen situaciones médicas distintas: la esterilidad y la infertilidad.
¿Esterilidad o infertilidad?
La esterilidad es la incapacidad para concebir tras mantener relaciones sexuales de manera habitual y sin utilizar métodos anticonceptivos. No se consigue fecundar el óvulo. La esterilidad requerirá un estudio de fertilidad de ambos miembros de la pareja.
La infertilidad, sin embargo, es la imposibilidad para lograr finalizar un embarazo satisfactoriamente con el alumbramiento de un bebé sano porque se produce un aborto espontáneo. Se logra que un espermatozoide fecunde un óvulo y se produzca el embarazo, pero este embarazo no llega a término. Esta situación requerirá un estudio de infertilidad de la mujer para valorar las posibles causas de los abortos de repetición.
Los problemas de fertilidad son más habituales de lo que pueda parecer, dado que afectan a un 15% de las parejas. Una tercera parte son debidos a problemas de la mujer, una tercera parte por problemas del hombre y la otra tercera parte es de causa mixta. Para cada caso se realizarán unas pruebas u otras.
Cuándo se realizan
Estas pruebas se realizan en los siguientes casos:
Parejas que llevan más de un año (o medio año si la mujer tiene más de 35 años) buscando el embarazo sin lograrlo.
Mujeres que hayan tenido más de un aborto espontáneo previo.
Mujeres que deseen tener un hijo a través de las técnicas de reproducción asistida.
Mujeres con antecedentes familiares de problemas de fertilidad, que padezcan enfermedades crónicas que alteren la capacidad reproductiva, o que estén sometidas a tratamientos de radioterapia o quimioterapia.
Hombres con antecedentes de problemas de fertilidad.
En qué consiste
En el estudio de fertilidad de la mujer inicialmente se realizará una visita con el ginecólogo para realizar un interrogatorio completo sobre sus antecedentes personales y médicos , así como una exploración ginecológica en consulta. A continuación, el médico solicitará:
Una analítica de sangre en unos días concretos del ciclo menstrual para poder determinar los niveles de varias de las hormonas sexuales que regulan el correcto funcionamiento de los ovarios, como son hormona foliculoestimulante (FSH), la hormona luteinizante (LH), el estradiol, la hormona antimülleriana (AMH) y la hormona tirotropina (TSH).
Una ecografía ginecológica para valorar la presencia de posibles enfermedades del sistema reproductor, como pueden ser malformaciones, pólipos, miomas, quistes u otras lesiones y, asimismo, realizar un recuento de los folículos antrales donde se hallan los óvulos inmaduros para conocer cuál es la reserva ovárica, es decir, el número de óvulos que potencialmente podrían ser fecundados.
Si fuese necesario y los primeros estudios no fuesen conclusivos, el ginecólogo puede valorar llevar a cabo otra serie de estudios:
Una citología, a menos que la paciente se haya realizado una en su revisión ginecológica anual hace menos de un año.
Una histerosalpingografía o una histerosalpingosonografía para poder valorar si existe una alteración en el útero y determinar si las trompas de Falopio son permeables.
Una histeroscopia para examinar con una cámara el interior de la cavidad uterina.
En el caso del hombre…
Se realizaría inicialmente una visita con el andrólogo, el especialista en fertilidad masculina, para investigar los antecedentes personales y médicos del paciente y realizar una exploración física completa (pene, testículos, próstata).
Asimismo, se solicitará un seminograma o espermiograma que permitirá valorar diferentes parámetros del esperma, como volumen, número de espermatozoides y su vialidad para poder llevar a cabo la fecundación del óvulo.
Si el andrólogo lo considerase necesario podría solicitar otras pruebas como un segundo seminograma, un cultivo del esperma, una prueba de capacitación espermática, una analítica para valorar posibles alteraciones hormonales, especialmente de los niveles de testosterona, una ecografía testicular y prostática o un estudio cromosómico y/o genético de los espermatozoides.
Con toda esta información el equipo de especialistas en reproducción podrá determinar cuál es la causa de las dificultades para la fecundación y valorar las posibles opciones terapéuticas, como la inseminación artificial, la fecundación in vitro, la microinyección espermática o la transferencia de embriones congelados.

Artículo especializado
Cuánto Tiempo Dura el Proceso de Fecundación In Vitro
Determinadas circunstancias como la edad a la que accedemos a la gestación, el tipo de vida que llevamos en cuanto a estrés, hábitos tóxicos, sobrepeso… inciden negativamente en la fertilidad de las parejas, que cada vez c on más frecuencia deben consultar a un especialista en técnicas de reproducción asistida porque necesitan tratamiento.
Cuándo acudir a consultar
Una pareja que, tras un periodo prudencial, que según la edad puede ser de seis a 12 meses, busca activamente el embarazo y no lo consigue espontáneamente, debe plantearse una consulta para hacer algún estudio de ambos con la intención de diagnosticar si existe alguna causa que lo impida.
En ocasiones se identifica el eslabón que falla en la cadena, y en otras ocasiones no se encuentra causa alguna, y tanto en un caso como en el otro el médico puede aconsejar una técnica de reproducción asistida para facilitar las cosas. De entre las distintas técnicas, la fecundación in vitro es una de las más usuales.
Duración del tratamiento
Una de las preguntas habituales de una pareja que se interesa por el tema es: ¿cuánto tiempo dura el proceso de fecundación in vitro? Pues es relativamente rápido, ya que simplemente se trata de hacer “in vitro”, que significa en el laboratorio (en vidrio, en una probeta en el laboratorio), el proceso de fecundación de un óvulo por un espermatozoide . Se empieza por la preparación de los ovarios para obtener óvulos de calidad, cuantos más mejor, y que puedan ser fertilizados en el laboratorio. Una vez fecundado el embrión, se deposita con sumo cuidado en el interior del útero de la mujer… y ¡a esperar! Por tanto, dura lo que dura un ciclo menstrual, aproximadamente un mes.
Pero vamos a detallarlo un poco mejor:
Daremos a la mujer una medicación, desde el inicio de su ciclo. En la raza humana al iniciarse un ciclo menstrual se ponen en marcha cierto número de óvulos, variables según la edad, desde un par de decenas en mujeres jóvenes a unos pocos en mujeres de edad más avanzada. De forma natural hay un proceso que hace que de esos óvulos que hay en oferta cada mes sólo evolucione hasta su estadio de máxima madurez uno solo. Por este motivo los embarazos humanos mayoritarios son de una sola cría. Pues esta medicación tiene la finalidad de inhibir ese fenómeno y conducir hasta el final el mayor número de óvulos posibles, para tener el máximo de oportunidades.
Ecográficamente iremos monitorizando la evolución de todos esos óvulos que hemos reclutado, observando su crecimiento cada 48-72 horas.
Alrededor del día 14 del ciclo de la mujer seguramente ya estarán maduros y aptos para ser extraídos. Esto es variable de una mujer a otra. Pero más o menos en este momento se añade alguna otra medicación para asegurarnos que estarán disponibles en el momento en que vayamos a extraerlos.
En un procedimiento sencillo, de cirugía ambulatoria y bajo sedación habitualmente. Se realiza la punción de los ovarios para obtener los óvulos y se hace aspirando con una aguja que, por vía vaginal y guiada por ecografía, llega hasta los ovarios.
A partir de este momento es responsabilidad de los biólogos del laboratorio manipular los óvulos obtenidos que se mantienen en un medio de cultivo para que estén en buenas condiciones y se unen a la muestra de semen de la pareja, o de donante si es el caso, y los óvulos son fertilizados y se empiezan a dividir lentamente. Se van supervisando para asegurarnos que son de buena calidad y que progresan adecuadamente durante tres a cinco días, periodo al final del cual consideramos que si el embrión presenta buen aspecto tiene opciones de implantarse en el útero de la mujer.
Al tercer-quinto día se cita de nuevo a la mujer y mediante una cánula muy delgadita, sin requerir en este caso ningún tipo de anestesia, se deposita delicadamente el embrión o embriones (si se decide transferir más de uno para aumentar las opciones, siempre con el consentimiento de la paciente o pareja). Siempre se escoge el mejor o mejores y se congela el resto para una ocasión posterior.
La mujer en poco tiempo podrá hacer vida normal, tendrá que administrarse alguna medicación para contribuir a la buena implantación del embrión, y dos semanas más tarde se podrá hacer una prueba de embarazo, y si hemos tenido suerte saldrá positiva.
Este es el procedimiento estándar, puede tener variaciones, puede no ser posible transferir en ese mismo ciclo por seguridad o si es necesario biopsiar los embriones para descartar patologías. En ese caso nos vamos al siguiente ciclo, pero si todo es fácil, el tratamiento durará un mes , y si todo ha funcionado, nueve meses más tarde asistiremos al parto.

Artículo especializado
Clamidia
La clamidia es un tipo de bacteria especial que tiene un comportamiento a caballo entre una bacteria y un virus. Existen tres tipos de clamidia que pueden afectar a las personas, pero en este caso hablaremos de la Chlamydia Trachomatis , que es causante de una infección ginecológica. Las otras dos especies son causantes de infecciones respiratorias.
Cómo se transmite y qué síntomas provoca
La transmisión de la infección por clamidia es por vía sexual, afecta tanto a hombres como a mujeres y puede ser completamente asintomática. Cuando causa síntomas son muy variados:
Uretritis, es decir, síntomas de inflamación de la uretra que pueden confundirse con una infección de orina. En varones puede acompañarse de secreción purulenta por el meato uretral y de dolor testicular.
En mujeres también se puede observar esa secreción a través del orificio del cuello uterino, pus que proviene del interior del útero y por tanto estar afectando los genitales internos en una entidad que se llama enfermedad inflamatoria pélvica, que se define como una infección de gravedad moderada-severa, que afecta útero y trompas, con potencial de afectar toda la cavidad abdominal y lesionar las trompas permanentemente, hecho que conllevaría problemas para la fertilidad femenina.
Si se transmite por sexo anal puede ocasionar inflamación del recto con dolor rectal y secreción anormal mucosa o hemática por el ano.
En personas con un determinado grupo genético puede ocasionar un síndrome general que afecta los ojos, las articulaciones y la piel llamado Síndrome de Reiter.
Otras consecuencias de la clamidia
En los casos de gestantes afectadas por clamidia podemos encontrarnos con recién nacidos contagiados por este germen durante el parto al que pueden causar conjuntivitis, motivo por el cual es norma aplicar una pomada antibiótica ocular a todos los bebés que nacen en centros sanitarios. Si no se trata, una infección ocular neonatal por clamidia puede ocasionar problemas graves o incluso ceguera.
No en nuestro medio, pero en algunos países de Asia, África y América, existen unas cepas concretas de clamidia que ocasionan una pequeña úlcera genital que pasa desapercibida y cura en pocos días, pero posteriormente puede ocasionar una grave inflamación de los ganglios de la zona que pueden formar grandes colecciones de pus y una severa afectación general.
Otras cepas de clamidia pueden causar una conjuntivitis que se transmite de persona a persona favorecida por las malas condiciones higiénicas. Es una de las principales causas de ceguera en países subdesarrollados.
A quién afecta
La incidencia es difícil de calcular, pues el 70% de las infecciones son asintomáticas y, al ser una infección de transmisión sexual, es mucho más frecuente en determinados grupos de población de riesgo.
Tratamiento efectivo
Una vez planteado este contexto apocalíptico hemos de dar un mensaje tranquilizador ya que a pesar de que la infección tiene una alta prevalencia, en la mayoría de los casos las infecciones son leves y además el tratamiento antibiótico es altamente efectivo, así que el reto es saberla diagnosticar y tratar. Hay que tratar también a las parejas sexuales del sujeto infectado.
El diagnóstico es fácil con unas pruebas de laboratorio sencillas pero específicas, así que hay que sospecharla, porque los medios de cultivo que se usan habitualmente no son buenos para detectarla.
Prevención
Como la transmisión es mediante relaciones sexuales no protegidas, tanto orales, vaginales como anales, con la persona infectada, la manera de prevenir la infección es mediante el uso del preservativo en todas las prácticas sexuales y durante todo el contacto. La persona infectada puede perfectamente no ser consciente de ello pues un alto porcentaje son asintomáticas. Y la infección no deja inmunidad, así que tras haber recibido tratamiento y solventado la infección conviene mantener las mismas medidas de precaución pues el recontagio es posible.
Artículo especializado
Puerperio, Recuperación del Aparato Reproductor tras el Parto
Después del parto es importante respetar los tempos y tener una serie de precauciones y realizar las acciones necesarias para que todo vuelva “más o menos” a quedar como estaba antes del embarazo.
Qué pasa en el embarazo
El embarazo es un proceso fisiológico, pero que supone una importante sobrecarga física para la mujer:
Durante la gestación es normal un incremento de peso de 10-12 Kg, en los mejores casos, pero no es infrecuente un aumento mucho mayor. Este peso de más lo carga la espalda, las rodillas y los tobillos de la embarazada causando frecuentes dolores de espalda.
La distensión abdominal y el volumen que carga la embarazada en su abdomen hace que la musculatura abdominal se distienda y muchas veces los músculos abdominales se separan de la línea media, además el centro de gravedad del cuerpo se adelanta con lo que la columna vertebral debe arquearse para mantener la estabilidad.
El útero que contiene el feto aumenta de tamaño a medida que avanza el embarazo llegando hasta debajo de las costillas al final de la gestación
Los ligamentos entre los huesos de la pelvis adquieren cierta laxitud para permitir un mínimo juego entre ellos que facilite el paso del feto a través suyo en el momento del parto.
La vagina se engrosa para permitir su estiramiento durante el parto y todos los órganos pélvicos se congestionan por la presión que ejerce el útero gestante
Todos estos cambios culminan en el momento del parto en el que la presión ejercida por las contracciones uterinas empujará el feto hacia el exterior por la vagina. Esto puede comportar, en ocasiones, el descenso de los órganos pélvicos o lesiones ocasionadas por el feto en su expulsión. Y en caso de cesárea, también los músculos abdominales se verán afectados por la intervención.
La recuperación tras el parto
El primer paso de la recuperación postparto es buscar la manera de que la madre descanse tanto como sea posible, se alimente bien, y duerma el número suficiente de horas, aunque sea de forma interrumpida por la lactancia y los cuidados del bebé.
Se aconsejan suplementos vitamínicos, una buena dieta y hidratación y antiinflamatorios en los primeros días del puerperio.
Y una vez terminado el puerperio inmediato, después de los primeros días-semana empezar un plan de recuperación para que la musculatura abdominal y pélvica recupere su anatomía y fuerza.
Este plan lo dividiremos en las medidas a tomar durante el puerperio inmediato y el tardío:
En el puerperio inmediato, durante la primera semana postparto:
Las recomendaciones empiezan por los cuidados necesarios para una correcta cicatrización de la episiotomía o cesárea siguiendo los consejos del médico
Evitar actividad física innecesaria pues el cuidado del recién nacido ya constituye suficiente carga, evitando cargar peso, estar mucho tiempo de pie o andar demasiado, aunque a la vez es conveniente una mínima movilización de las piernas para evitar problemas vasculares y no estar demasiado en cama.
La lactancia materna es muy beneficiosa para madre e hijo, pero hay que procurar tener una buena postura pues favorece los dolores de espalda que ya son frecuentes por el simple hecho de la readaptación de la columna a que nuevamente se ha desplazado el centro de gravedad del cuerpo. También favorece el restreñimiento , que hay que evitar para no hacer descender más los órganos pélvicos el soporte de los cuales ya está debilitado por el parto. Hay que recomendar un abundante aporte de líquido.
Después de los primeros días del parto ya podemos empezar a hacer ejercicios de Kegel para tonificar el suelo pélvico y aplicar el mismo concepto de este ejercicio al hacer cualquier contracción abdominal: cargar un peso, toser, estornudar…
Y no realizar ningún ejercicio abdominal tradicional ni mantener relaciones sexuales durante los primeros 40 días
Los ejercicios de Kegel consisten en contraer voluntariamente la musculatura del suelo pélvico como si quisiéramos interrumpir el chorro de orina durante la micción. Mantener esa contracció n unos segundos y aflojar, repetir 10-15 veces, y intentar realizar esta maniobra de forma rápida contraer-aflojar-contraer-aflojar sin mantener la tensión también 10-15 veces, realizando estas series dos o tres veces al día
En el puerperio tardío, desde la semana hasta el final de la cuarentena:
Seguir las recomendaciones anteriores incrementando nuestra actividad física y los ejercicios de Kegel, y a partir de la cuarentena ya se pueden iniciar los ejercicios abdominales hipopresivos, que consisten en contraer los músculos abdominales hacia el interior del abdomen, trabajando mucho la respiración y el diafragma, sin que haya movimiento. En esta fase un fisioterapeuta especializado podrá valorar el estado de la musculatura abdominal y pélvica y dirigir estos ejercicios, y en ocasiones añadir algún tratamiento adicional específico como electroterapia, terapias manuales o técnicas de biofeedback .
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.

Artículo especializado
Pólipos Endometriales
Estamos ante una de las patologías ginecológicas más frecuentes. Se trata de formaciones redondeadas u ovaladas que crecen en el interior del útero y que son más frecuentes a medida que la edad avanza . Son mayoritariamente benignos.
Contexto…
El útero está recubierto por dentro por un tejido llamado endometrio que tiene la finalidad de acoger y alimentar el embarazo durante las primeras semanas. Durante la edad fértil de la mujer, con una periodicidad de aproximadamente 4 semanas, este tejido madura, y si no se ha producido la gestación, caduca y se desprende en forma de sangrado menstrual para construir uno nuevo. A partir de la menopausia, este tejido queda latente sin actividad. Pues bien, los pólipos endometriales serían estas formaciones redondeadas u ovaladas que crecen en el interior del útero.
Cómo se producen
Los pólipos endometriales crecen en este tejido, su causa es desconocida, aunque en su fisiopatología están implicados factores hormonales, inflamatorios y genéticos. Son más frecuentes al aumentar la edad, muy raros antes de los 20 años, más frecuentes entre los 40 y los 60. Son una patología eminentemente benigna, aunque pueden malignizar un 1%.
El tejido del que están formados contiene glándulas y abundancia de vasos, motivo por el cual su sintomatología más frecuente son los sangrados, tanto aumento del sangrado menstrual, como sangrados entre reglas o sangrado después de la menopausia. Muy a menudo no ocasionan síntomas y se diagnostican casualmente durante una ecografía rutinaria . Otros síntomas no tan frecuentes son dolor o esterilidad.
Cómo se diagnostican
El diagnóstico es bastante sencillo mediante una ecografía transvaginal . En mujeres postmenopáusicas y en determinados momentos del ciclo menstrual su imagen es característica, se identifican como una formación nodular sólida en el interior de la cavidad uterina, que puede medir desde pocos milímetros a 1-2 cm. No son habituales los pólipos mayores a 2 cm. Fácilmente se puede identificar el pedículo arterial que lo alimenta.
Cómo se tratan
Cuando se diagnostican, normalmente, se aconseja su exéresis quirúrgica por varios motivos. En primer lugar, a pesar de que se trata de una patología benigna, tiene un potencial de malignización muy bajo, pero no cero, s obre todo en pacientes menopáusicas . Y, en segundo lugar, porque es muy raro que desaparezcan solos, y lo único que pueden hacer es seguir creciendo. Y finalmente porque el tratamiento quirúrgico es muy sencillo y con baja tasa de recidiva y complicaciones.
El tratamiento es una histeroscopia quirúrgica : consiste en introducir un dispositivo dotado de cámara de endoscopia a través de la vagina y del orificio del cuello uterino hasta el interior del útero. Esta imagen, como en cualquier endoscopia, se ve proyectada en una pantalla. El mismo dispositivo lleva incorporado una herramienta que facilita el corte, y con ella se puede seccionar y extraer el pólipo endometrial de una pieza o fragmentado para remitirlo al laboratorio de análisis de anatomía patológica.
Este procedimiento se practica habitualmente de forma ambulatoria sin anestesia o con una anestesia regional o sedación, pudiendo dar de alta a la paciente al poco rato. La tasa de complicaciones del procedimiento es baja, y el postoperatorio no suele comportar dolor y permite la reincorporación a las tareas habituales prácticamente enseguida .
SI SE BUSCA UN EMBARAZO…
En mujeres que desean embarazo, además, está añadido el hecho de que el pólipo menoscaba sus posibilidades de gestación, pues por un lado está ocupando el espacio en el que deberá implantarse el embrión, y en función de la localización del pólipo puede suponer un impedimento para el normal ascenso de los espermatozoides pues puede obstruir la trompa.
Así que, aunque es una patología mayoritariamente benigna, cuando se diagnostican se suelen extirpar, y constituye una de las intervenciones quirúrgicas más frecuente en ginecología.

Artículo especializado
Por qué No me quedo Embarazada
Lograr un embarazo a la primera no es lo más habitual. Quedarse embarazada no es tan sencillo ni tan fácil como parece . En cada intento tenemos, aproximadamente, un 17% de probabilidades de concebir.
Desde que una pareja decide tener hijos, hasta que consiguen un embarazo, lo habitual es que pasen varios meses. La media son unos seis. Este tiempo suele estar lleno de impaciencia y, si el embarazo no llega, es inevitable preguntarse las causas de por qué no logramos el embarazo .
Fertilidad en cifras
1 de cada 6 intentos (17%) logra un embarazo en una pareja sana y supuestamente fértil.
La edad va en nuestra contra. La fertilidad decrece naturalmente con la edad, de manera más acusada, a partir de los 40.
En Europa, 1 de cada 6 mujeres tienen algún tipo de dificultad para lograr un embarazo.
En España, entre 10 y 15 de cada cien parejas que se plantean tener un hijo tienen problemas para quedar embarazadas.
Unos 100.000 bebés cada año nacen gracias a las técnicas de reproducción asistida.
Conocer tu ciclo y tus días fértiles
Uno de los motivos por los cuales una mujer no se queda embarazada es por el desconocimiento de su propio cuerpo. Reconocer los días fértiles, si no hay ningún problema añadido, es una buena herramienta para concebir un bebé.
La concepción no es fácil, ya que influyen múltiples factores y las condiciones deben ser las óptimas: la mujer ovule, el espermatozoide fertilice al óvulo maduro, éste se desarrolle, anide en el útero y avance el embarazo.
Las probabilidades aumentan si las relaciones sexuales se mantienen durante los días fértiles de la mujer .
La ovulación se produce en los días centrales del ciclo menstrual , que dependiendo de cada mujer, tiene una duración normal de 23 a 35 días. En la mayoría de las mujeres la ovulación se produce entre el día 12 y el día 16 del ciclo.
Métodos como el sintotérmico de fertilidad o el método Billings, pueden ayudar a identificar esos días. El primero consiste en tomar la temperatura basal de la mujer y, el segundo, se identifica la ovulación a través de la observación de las secreciones vaginales. También disponemos de test de ovulación que detectan en la orina la subida de la hormona LH (Hormona Luteinizante) que se produce 24-36 horas antes de la ovulación.
La edad es uno de los factores más frecuentes
Cada vez posponemos más la maternidad: el trabajo, los estudios, la estabilidad económica y las escasas políticas de estimulación de la natalidad , hacen que las mamás y los papás sean cada vez más mayores. El reloj biológico juega en nuestra contra, a medida que la edad de la mujer y el hombre avanzan, las probabilidades de concebir disminuyen. Con 20 años, una mujer tiene un 25% de probabilidades de conseguir el embarazo manteniendo relaciones sexuales en sus días fértiles, a los 30 años, un 15%, a partir de los 35 años, un 8% y a partir de los 38 años, un 3%.
Causas físicas más frecuentes de infertilidad
Aproximadamente, un 35% de las causas de infertilidad son femeninas, otro 35% masculinas. En un 20% de las parejas con problemas para tener hijos, la esterilidad procede de ambos . Y finalmente, en otro 10% de los casos no se encuentra el origen.
Causas femeninas más frecuentes
Problemas ovulatorios
Baja respuesta o reserva ovárica
Problemas en la permeabilidad de las trompas de Falopio
Endometriosis
Ovario poliquístico
Causas masculinas más frecuentes
Menor producción de esperma
Obstrucción de los conductos de esperma
Baja movilidad de los espermatozoides
Malformaciones en los espermatozoides
Recuento bajo de espermatozoides
Trastornos de la erección y eyaculación
La exposición a tóxicos (tabaco, alcohol, drogas u sustancias nocivas en el entorno…) son otra de las causas que causan problemas de fertilidad en hombres y mujeres .
¿Cuándo se debe acudir al especialista?
En parejas menores de 35 años, si tras 12 meses de relaciones sexuales sin protección no se consigue el embarazo, deben acudir a un centro de fertilidad. En parejas mayores de 35, el tiempo es menor: si a los seis meses no hay embarazo, se deben estudiar las causas.
Por otro lado, no debemos retrasar la visita al especialista cuando presentemos estas circunstancias que se enumeran a continuación, porque pueden causar infertilidad y, detectarlas a tiempo y tratarlas, es muy importante para intentar lograr el deseado embarazo :
Endometriosis.
Síndrome de ovario poliquístico (SOP).
Inicio de ciclos irregulares: pueden ser sospecha de menopausia precoz o baja reserva ovárica.
Antecedente de infecciones pélvicas o cirugía pélvica.
Problemas endocrinológicos: obesidad, problemas tiroidales, ovario poliquístico o peso insuficiente.
La consanguiniedad: este tipo de parejas siempre debe de contar con consejo genético.
Si se padece una enfermedad genética: es importante el consejo genético y tener toda la información disponible para saber los riesgos o la transmisibilidad de la enfermedad.
Enfermedades de transmisión sexual: pueden repercutir en los órganos reproductivos.
En el caso del varón, se debe acudir a un especialista en fertilidad cuando éste presente :
Paperas en la infancia del futuro papá: es una causa de esterilidad masculina.
Antecedentes de patología urológica como infecciones de transmisión sexuales, cirugía, traumatismos o varicocele.
Recomendaciones para ayudar a lograr un embarazo
Tener relaciones frecuentes : no sólo porque, por sí mismas, aumentan la probabilidad de un embarazo, sino porque tener relaciones sexuales a diario mejora la calidad del semen. Según la OMS, para elevar las posibilidades de tener un hijo, el tiempo óptimo de abstinencia es entre dos y siete días.
Visitar al ginecólogo antes de buscar un embarazo : el ginecólogo hará un examen y evaluará el estado de salud de la mujer y de su pareja, recetará un suplemento de ácido fólico, preguntará sobre los antecedentes familiares, explorará a la mujer y le realizará pruebas como analítica y ecografía para valorar posibles condiciones que puedan dificultar un embarazo.
Unos buenos hábitos : el estilo de vida de la futura madre es fundamental para lograr la concepción y el buen desarrollo del embarazo. Dejar los malos hábitos y evitar los tóxicos como el alcohol y el tabaco. Realizar ejercicio físico para bajar de peso si se padece sobrepeso u obesidad y llevar una alimentación equilibrada.
Bienestar emocional : el estrés no es bueno para nada. Asimismo, el cansancio y la ansiedad pueden interferir en los deseos genésicos de la pareja.
¿Y si no me quedo embarazada?
Una visita al especialista es definitiva para confirmar si hay, o no, problemas de fertilidad en la pareja . En algunas ocasiones, el problema se resuelve (si es hormonal, por ejemplo) y puede lograrse un embarazo con éxito. Si no se debe recurrir a un centro especializado en medicina reproductiva para valorar las diferentes opciones para obtener un embarazo, en función de las condiciones de la pareja.
¿Qué pruebas se realizan en una unidad de medicina reproductiva?
En la mujer y en el varón se realizan, de manera rutinaria, una serie de exámenes para determinar la causa de la posible infertilidad. En un 10% no se encuentra la causa.
En la mujer se realiza :
Ecografía transvaginal: para valorar la forma del útero y los ovarios. Se pueden detectar tanto malformaciones uterinas, miomas o pólipos endometriales y descartar, como también, quistes o tumoraciones ováricas.
Analíticas hormonales: para valorar la función ovárica y del tiroides.
Serologías: para descartar infecciones como la rubeola, hepatitis B y C, sífilis o VIH.
Histerosalpingografía: es una prueba de imagen con contraste que permite estudiar la cavidad uterina y comprobar que las trompas -que es el lugar donde se produce la fecundación – sean permeables.
En el caso del varón :
Analítica: general y hormonal
Seminograma con REM (recuento de espermatozoides móviles).
Artículo especializado
Como Evitar la Preeclampsia
La preeclampsia es una de las complicaciones graves más frecuentes del embarazo. Afecta al 2-5% de los embarazos, y puede revestir gravedad tanto para la madre como para el feto.
Está ocasionada por factores diversos, pero tiene un componente autoinmune importante, como si el organismo materno no reconociera como propio el al feto y reaccionara ante él como los receptores de órganos que rechazan el tejido exógeno. Con lo cual, cuando se inicia el proceso la única manera de “curarlo” es finalizando el embarazo, así que será tanto más grave cuanto antes se presente, pues al riesgo fetal y materno de esta patología añadimos la prematuridad en caso de que sea necesario finalizar el embarazo precozmente.
Quiénes son más proclives a sufrirla
Parece ser que la reacción autoinmune se manifiesta más en pacientes que no han tenido una historia larga de exposición a los antígenos de su pareja (presentes en el esperma), como si la inmunidad materna se hiciese más tolerante a los antígenos masculinos al irse exponiendo a ellos a lo largo del tiempo. Este es el motivo por el que es más frecuente en primeros embarazos, en parejas que han utilizado habitualmente como método anticonceptivo el preservativo, en inseminaciones artificiales con semen de banco, o en mujeres con hijos previos de otra de pareja.
La parte masculina puede influir
También es muy curioso que este componente autoinmune también venga condicionado por parte masculina, como si ciertos varones desencadenaran una reacción inmunológica más intensa que otros: los varones que han engendrado un embarazo complicado con preeclampsia constituyen factores de riesgo para que una nueva pareja desarrolle preeclampsia en una futura gestación. También hay un factor genético materno, siendo más frecuente en grupos familiares en que la madre/hermanas hayan sufrido este problema.
Cómo se manifiesta la preeclamsia
Se trata de un trastorno multiorgánico de la gestante, se manifiesta a partir de la mitad del embarazo, pero los factores que la provocan ya están presentes antes. Existen cambios en el interior de todos los vasos del cuerpo que, cuando se empieza a manifestar esta afección, están anormalmente contraídos . Si las arterias principales están “tensionadas” o “contraídas” se manifiesta el principal síntoma de la preeclampsia: la hipertensión arterial, los síntomas de la cual son la sensación de mareo y dolor de cabeza. Esta disfunción en los vasos afecta también al riñón, de forma que no cumple exactamente su función, dejando pasar a su través proteínas, cosa que un riñón en condiciones no debe hacer, con lo que nos encontramos con el segundo signo de este trastorno: la presencia de exceso de proteínas en orina. L a principal proteína que se pierde es la albúmina , este es el motivo por el que clásicamente a este proceso se lo conocía como “ataque de albúmina”. Una consecuencia de esta pérdida de proteínas es que se derrama líquido por fuera de los vasos, con lo que se manifiesta el tercer síntoma más frecuente: la hinchazón o edema en tobillos, manos, cara… Si no se diagnostica y se deja evolucionar el cuadro puede seguir afectando al hígado, al cerebro y causar convulsiones, siendo este el nivel de máxima gravedad (la eclampsia), cuando la vida tanto de la madre como del feto se pueden ver comprometidas.
¿No existe tratamiento?
Como no existe tratamiento, el máximo interés lo hemos de tener en la detección precoz , con lo que en cada visita prenatal se determina la presión arterial y ante una elevación de la misma o la presencia de edemas no justificados el ginecólogo solicitará una analítica sanguínea y de orina para valorar las proteínas, signo indicativo de esta patología. No hay que alarmarse ante un aumento puntual de la tensión arterial que, dependiendo del contexto, no tiene por qué significar una preeclampsia, ni los edemas en los tobillos, muy comunes en embarazos absolutamente normales en algunas mujeres al final del embarazo y sobre todo relacionados con el calor y las horas que pase la gestante en pie, y que son debidos a dificultad del retorno circulatorio en las piernas debido al volumen ocupado en la pelvis por el útero grávido.
Detección precoz
Para su detección precoz se han estudiado muchos indicadores. Actualmente se practica de rutina la valoración del flujo sanguíneo en los vasos que llevan la sangre al útero y consecuentemente a la placenta: las arterias uterinas. Ecográficamente se puede determinar la “tensión” que presentan esos vasos, siendo un factor de riesgo el encontrar ese valor elevado durante el primer o más fiablemente durante el segundo trimestre de embarazo. Esto nos permite identificar a pacientes de riesgo y someterlas a una supervisión más estricta o a plantearnos “terapias” preventivas.
Difícil prevenir
Se han valorado distintos tratamientos preventivos, sin haber un consenso firme al respecto. Pero en casos muy concretos de alto riesgo puede valorar el tratamiento preventivo con ácido acetil salicílico (Aspirina®) a dosis bajas.
Pero ya hemos comentado que los cambios microscópicos en la circulación ya se han establecido mucho antes de que se presenten los síntomas, así que la prevención es muy difícil, el reto ha de ser la detección precoz, y el tratamiento a tiempo.
Tratamiento
El tratamiento no es otro que finalizar el embarazo en cuanto sea posible. Si nos encontramos en etapas tempranas del embarazo en el que existe riesgo fetal por prematuridad se recomienda reposo, tratamiento con fármacos antihipertensivos y supervisión estricta mientras podemos estimular al feto para que acelere su maduración pulmonar en caso de tener que extraerlo prematuramente. Con esto reduciríamos el riesgo de complicaciones pulmonares por prematuridad. En casos severos requiere ingreso hospitalario y medicación endovenosa múltiple. En cuanto el bebé está fuera el proceso empezará a revertir, pero puede costar hasta seis semanas en recuperarse la total normalidad, incluso es posible que se manifieste la preeclampsia en el posparto. En este caso nuestra única preocupación es la madre, y es más fácil de gestionar su tratamiento, pues los cambios de presión arterial no nos afectaran al feto.
Hoy en día, a pesar de llevar una vida saludable quizás no podemos evitar la aparición de una preeclampsia, pero con una buena supervisión médica para el diagnóstico precoz y el tratamiento adecuado es muy infrecuente sufrir complicaciones graves de una preeclampsia o una eclampsia. Así pues, un buen consejo si estás embarazada es que contactes con tu ginecólogo o te hagas una simple determinación de tensión arterial en cualquier farmacia ante un dolor de cabeza poco habitual o si se te hinchan exageradamente los tobillos, o ambas cosas. ¡Más vale prevenir!
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.

Artículo especializado
Embarazo de Riesgo
El embarazo es un proceso fisiológico para el que el organismo de la mujer está perfectamente preparado, pero hay que tener en cuenta que le supone una sobrecarga y un estrés , y en determinadas situaciones puede incluso suponer un riesgo para su salud. En estos casos hablamos de embarazo de riesgo desde el punto de vista materno.
En otras ocasiones, es el propio embarazo el que está en riesgo por circunstancias que pueden afectar al pronóstico de la gestación o al estado del feto, es entonces cuando consideramos un embarazo de riesgo desde el punto de vista fetal.
En los embarazos que evolucionan con normalidad la gestante puede hacer vida relativamente normal, pero en los embarazos de riesgo se requiere a veces reposo, o controles más intensivos o pruebas diagnósticas especiales . En estos casos, es importante seguir las pautas indicadas por el ginecólogo.
Cómo actuar
En la primera visita de embarazo, o en una visita preconcepcional en casos de patología materna hay que valorar todos los antecedentes de la paciente y etiquetar el embarazo como embarazo normal, de riesgo medio, alto o muy alto. Las causas de riesgo pueden ser de tres tipos:
Desde el punto de vista social: condiciones de la paciente, su edad, peso, talla, perfil socio-económico, hábitos tóxicos, exposición a tóxicos laborales…
Desde el punto de vista de los antecedentes de la paciente : enfermedades previas al embarazo, abortos o partos anteriores…
Desde el punto de vista del embarazo actual : patologías que se desarrollan en el embarazo en curso, como diabetes gestacional o preeclampsia, malformaciones fetales, embarazos múltiples o rotura prematura de la bolsa amniótica.
Causas de riesgo medio
Las causas de riesgo medio engloban todas las condiciones anatómicas que pueden dificultar un parto vaginal e incrementar el riesgo de cesárea , como son la talla baja, la obesidad no mórbida (la obesidad mórbida se considerará de riesgo alto) y las anomalías de la forma de la pelvis.
Por otro lado, todas las situaciones que puedan comportar un control insuficiente lo que puede comportar situación de riesgo fetal como los embarazos no deseados, las adolescentes, o las pacientes en condiciones socioeconómicas desfavorables.
Otro factor de riesgo medio, que puede ser alto o muy alto en función de la dosis, es la gestante con hábitos tóxicos, fumadoras o consumidoras de drogas o alcohol , por el efecto que puede tener en el feto. Las grandes fumadoras tienen fetos de bajo peso, y el consumo de alcohol incluso puede provocar un síndrome alcohólico fetal con afectaciones de múltiples órganos y retraso mental.
Son consideradas gestantes de riesgo medio las pacientes con alguna patología leve diagnosticada antes del embarazo, como cardiopatías leves, problemas respiratorios crónicos, enfermedades de transmisión sexual. Asimismo, las pacientes de edad avanzada o que han tenido más de 4 hijos previamente, o si el periodo transcurrido desde el último embarazo es inferior a 12 meses (de parto a parto).
También consideramos embarazo de riesgo medio cuando ha existido esterilidad previa y si el embarazo se ha conseguido a través de técnicas de reproducción asistida.
A lo largo del embarazo pueden aparecer circunstancias que conviertan un embarazo normal en uno de riesgo medio como pérdidas de sangre durante el primer trimestre, incremento excesivo o insuficiente de peso, infecciones urinarias…
Riesgo alto
Se considerará riesgo alto la patología materna más grave: cardiopatías, patologías endocrinas, anemia grave, obesidad mórbida por el riesgo que puede suponer el embarazo sobre la patología de la madre. También la diabetes gestacional por el riesgo fetal que comporta si no se controla adecuadamente. O pacientes diagnosticadas de infecciones víricas o bacterianas (hepatitis, toxoplasma, sífilis, VIH) por riesgo de malformaciones congénitas o infección del recién nacido.
También catalogado como riesgo alto los antecedentes obstétricos desfavorables: abortos anteriores, partos prematuros, recién nacidos de bajo peso, o partos previos con complicaciones dado el riesgo de presentar nuevos abortos o complicaciones en el parto. Así como pacientes que hayan sido sometidas a cirugía uterina previa por el riesgo de rotura uterina.
Incluimos en este grupo los embarazos en los que se ha diagnosticado una m alformación fetal, que según su severidad puede ser incluso de riesgo muy alto. También los embarazos de gemelos y la preeclampsia leve (alteración multiorgánica del tercer trimestre de embarazo que cursa con elevación de la tensión arterial, proteínas en la orina, y alteraciones analíticas).
Riesgo muy alto
En el grupo de riesgo muy alto incluimos todas aquellas gestantes con patología muy grave: cardiopatías severas, enfermedades psiquiátricas, diabetes previas al embarazo porque el embarazo puede tener serias consecuencias sobre el estado de la madre.
La drogadicción o alcoholismo habitual por el riesgo fetal de malformaciones, retrasos de crecimiento y prematuridad. Así como la preeclampsia grave. Y las malformaciones fetales graves o retrasos de crecimiento severos
La gestación múltiple (de 3 o más fetos) o de fetos con malformación congénita compleja confirmada y todas aquellas condiciones que pueden favorecer un parto prematuro, como rotura prematura de membranas, malformación uterina o contracciones prematuras sin causa aparente.
Otro concepto que hay que incluir en este grupo es a las mujeres que han sufrido previamente una muerte fetal prenatal o neonatal por el riesgo de repetición y por la ansiedad generada por estos antecedentes.
Y finalmente accidentes obstétricos graves como la placenta previa o el desprendimiento precoz de placenta.
Cómo atender estos embarazos
Según el nivel de riesgo el control de embarazo se podrá realizar en el p rimer nivel asistencial, consultas básicas o centros de asistencia primaria en embarazos sin riesgo o con riesgo medio.
En algunos casos de riesgo medio y los de riesgo alto han de ser controlados en centros especializados o en hospitales de nivel B (comarcales).
Los de riesgo muy alto es necesario su seguimiento y atención al parto en hospitales de nivel C, donde se dispone de equipamiento adecuado para manejar recién nacidos con patología compleja o de gran prematuridad, así como gestantes con patología severa.
Si se te ha diagnosticado un embarazo de riesgo sigue los consejos de tu especialista y confía en que con el control adecuado y los medios a nuestro alcance prácticamente todos los problemas tienen solución.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.

Artículo especializado
Gonorrea, ¿Qué Debes Saber?
Seguro que sabes que la gonorrea es una enfermedad de transmisión sexual , pero poco más. Para empezar, te diremos que afecta sobre todo a personas jóvenes, entre los 15 y los 25 años, y que está provocada por la bacteria Neisseria Gonorrhoeae , un germen que existe en todos los países del mundo. El principal problema para su tratamiento está siendo el desarrollo de resistencias a los antibióticos.
¿Cómo se contrae?
En contagio se produce por relaciones homo o heterosexuales, genitales, orales o anales. Puede afectar a los genitales masculinos y femeninos, y también al ano o la cavidad oral. Una mujer embarazada que la padezca puede transmitírsela a su bebé durante el parto. La única manera de evitar la transmisión es limitar la promiscuidad sexual, y tener sexo protegido con preservativo. Además, para evitar la diseminación de la infección, cada vez que se diagnostica un caso hay que localizar a las parejas sexuales previas (teóricamente, a las personas con las que se han tenido relaciones durante los 60 días previos), explorarlas y tratarlas.
¿Qué síntomas produce?
En el hombre, el síntoma fundamental es el dolor o picor al orinar , que es la traducción de la inflamación de la uretra. Además, es frecuente observar una gota de pus blanco, verde o amarillo al final de la micción. Puede haber otros síntomas más raros, como el dolor en los testículos.
En la mujer, la gonorrea puede pasar inadvertida, o puede simular los síntomas de una irritación vulvar, una vaginitis o una infección de orina . Puede notarse ardor al orinar, aumento del flujo vaginal, o sangrado
Independientemente del sexo, la infección en el ano o el recto puede no causar síntomas, o manifestarse como flujo, picor en el ano o dolor al ir de vientre.
En el caso de afectar la cavidad oral, la enfermedad provoca una faringitis que se manifiesta por dolor de garganta, secreciones, fiebre , aumento de los ganglios linfáticos, o dolor de cabeza.
Se ha de tener en cuenta que existen otras uretritis y vaginitis no gonocócicas, que no están causadas por la bacteria de la gonorrea, sino por otros microbios, fundamentalmente la clamidia. Su diagnóstico se basa en pruebas microbiológicas, de la muestra tomada. Como son difíciles de distinguir de la gonorrea, muchas pautas de tratamiento incluyen antibióticos que sean efectivos para los dos gérmenes.
¿Cómo se diagnostica?
Se puede utilizar una muestra de orina para detectar la gonorrea. Sin embargo, si ha habido relaciones sexuales orales o anales, hay que usar un hisopo (bastoncillo) para obtener muestras de la garganta o del recto. Lo mismo se puede emplear para tomar muestras de la uretra del hombre o la vagina de la mujer.
¿Qué pasa si no se trata?
No tratada, esta infección puede curar por sí sola u ocasionar problemas muy graves. En la mujer puede ser responsable de una enfermedad inflamatoria pélvica , una infección interna de la pelvis que puede causar fiebre, dolor abdominal crónico, o infertilidad. En el hombre, puede ser responsable de infección de los testículos o la próstata , y causar también infertilidad . En casos graves, la infección puede pasar a la sangre y afectar a las articulaciones u otros órganos, y puede ser incluso mortal.
¿Cómo se trata?
Es una infección que se trata con antibióticos como los macrólidos y las cefalosporinas. Las resistencias del germen han ido aumentando a muchos antibióticos, por lo que no puede tratarse con penicilina u otros antibióticos más antiguos. En algunos casos, es necesario practicar una prueba llamada antibiograma para conocer la sensibilidad del germen a los distintos antibióticos y administrar el más adecuado.
¿Y la prevención?
Es evidente que el sexo seguro es la mejor prevención, con la utilización del preservativo para cualquier relación genital, oral o anal. También es importantísimo detectar y tratar a posibles parejas que puedan seguir transmitiendo la enfermedad a otras personas.

Artículo especializado
Ecografía 5D
¿Qué embarazada no está ansiosa por ver la cara de su bebé? ¿Qué futuro papá o mamá no imagina y fantasea sobre cómo será? Para dar respuesta a esta demanda se ha acelerado el desarrollo de tecnología con ultrasonidos que nos permite ver imágenes sorprendentes del feto dentro del vientre materno.
Un poco de historia…
La historia de la ecografía tiene poco más de 100 años. Se inició en el contexto de la ingeniería y la tecnología militar y no fue hasta mediados del siglo XX cuando se aplicó en medicina. Encontró en el campo de la obstetricia uno de las especialidades en la que más se ha utilizado su tecnología, por su inocuidad a la hora de explorar a las gestantes y por el gran nivel de información que nos ofrece al estar el feto sumergido en agua, que es el medio óptimo por el que se transmiten los ultrasonidos .
La tecnología 2D
La tecnología en la que se basa el diagnóstico actualmente es la “2D” , imágenes en blanco y negro que nos ofrecen cortes de los tejidos. Es como exploramos habitualmente los fetos para rastrear su anatomía y descartar malformaciones. Los aparatos actuales ofrecen imágenes cada vez más nítidas y precisas. Para ello se usan ultrasonidos, ondas de alta frecuencia que se aplican mediante un transductor sobre la piel de la paciente lo más cerca posible del órgano a explorar. Para favorecer su difusión se aplica sobre la piel un gel acuoso y estas ondas, al llegar a los distintos tejidos, rebotan en una frecuencia u otra según su densidad y profundidad, y el rebote es recogido por el mismo transductor (emisor-receptor). Un software interpreta los datos recogidos y los plasma en una imagen en la pantalla del ecógrafo en diferentes tonalidades de gris.
La tecnología 3D y 4D
Hace poco más de una década se desarrolló la tecnología 3D , con la que un “barrido” en dos dimensiones sobre un tejido a explorar, procesado por un ordenador, componía una imagen fija con aspecto de tres dimensiones. Con el tiempo se sofisticó y se podían ver estas imágenes 3D en movimiento en tiempo real. Aplicado a la obstetricia nos permite ver al feto moviéndose, gesticulando, bostezando, parpadeando… A esta nueva tecnología se la llamó 4D.
Hasta llegar a la tecnología 5D
Recientemente se ha mejorado el software que permite la composición y el tratamiento de la imagen, cambiando el tono sepia de las 3 y 4D por un tono rosado con más tonos de sombra y textura, como si se tratara de una imagen real del feto iluminado, dándole el nombre de 5D . En realidad, no hay mucha diferencia entre la 4 y 5D pues es la misma tecnología mejorada, lo ofrece resultados mucho más vistosos en cuanto a realismo .
No tiene finalidad diagnóstica
Tal y como está planteado en el mercado actualmente la ecografía 4-5D es más bien una exploración “festiva” cuya pretensión es obtener bonitas imágenes del feto en movimiento, de sus rasgos y evolución y no una prueba médica con finalidad diagnóstica. Existen infinidad de centros que realizan este tipo de ecografías:
Algunos en el contexto de un centro médico en el que además se puede hacer el control gestacional y las ecografías con finalidad diagnóstica.
En otro tipo de centros el único propósito es disfrutar de la imagen del feto. Para ello, disponen de aparatos de alta tecnología y personal altamente cualificado para hacer este tipo de ecografías, que no son fáciles de hacer.
PARA QUE QUEDEN BIEN…
Este tipo de ecografía es una exploración que depende mucho de la “colaboración” fetal. Se requiere de una buena posición del feto para obtener buenas imágenes, líquido abundante, cuanto más delgada esté la gestante mejor, si la placenta no obstaculiza la visión también mejor… No siempre se consigue un buen resultado a pesar de la cualificación del técnico o médico y de su mejor intención. En esto la tecnología 5D también ha supuesto un avance pues solventa mejor el problema de las interferencias de órganos o tejidos que se interponen en la imagen.
¿Qué nos llevamos a casa?
Actualmente se pueden contratar exploraciones a precios razonables que además de los 20-30 minutos de exploración en directo nos darán las imágenes registradas en soportes digitales como CD/DVD o lápices de almacenamiento, fotos, incluso proyecciones sobre el vientre materno a la vez que se realiza la ecografía. Se comercializan bonos de dos, tres o más ecografías para poder disfrutar de esas imágenes en distintas etapas del embarazo y así observar la impactante evolución del feto… Infinitas posibilidades para lo que es un negocio con un nicho de mercado interesado.
Más allá de la parte lúdica: una tecnología para el futuro
A parte de esta vertiente más lúdica y conocida de las ecografías 4-5D también hay que saber que existe una indicación médica muy importante de esta tecnología que está en sus inicios pero que tiene un gran futuro, pues nos permite visualizar mejor las posibles alteraciones anatómicas del “exterior” del feto (labio leporino, malformaciones genitales, hernias, malformaciones de las extremidades). Y la adquisición de volúmenes de imágenes que una vez terminada la exploración, cuando la paciente ya está en su casa, permite al médico examinarla desde ángulos distintos a los que la miró en directo y tomar diferentes medidas. Esto es una concepción diferente de lo que se conocía hasta ahora de una ecografía, que era una prueba que se interpretaba a medida que se realizaba.
Pruebas inocuas
Tanto la ecografía clásica como la 4-5D son absolutamente inocuas tanto para la madre como para el feto, indoloras y que se pueden realizar con la asiduidad que las condiciones requieran o permitan. No hace falta preparación alguna, en etapas precoces de embarazo se pueden realizar por vía vaginal y, si no, por el abdomen. En este caso se requerirá que la vejiga urinaria esté llena para que el líquido que contiene permita el paso de los ultrasonidos al útero que está detrás.
¿Cuándo es mejor realizarla?
De escoger una única fecha para realizar una ecografía 5D lo ideal es que sea entre la semana 26-30 , aunque se puede realizar en cualquier momento del embarazo. Se recomienda no ponerse cremas hidratantes o antiestrías el día de la exploración porque determinados componentes pueden interferir con la transmisión de los ultrasonidos y restar nitidez. Si el feto está colocado en una posición que dificulta la visión puede que el técnico/médico te estimule suavemente el abdomen para favorecer que el feto cambie de posición, igual que si está dormido, para conseguir imágenes en actividad que son más sorprendentes. Si no lo conseguimos, a veces se aconseja comer algo dulce , que también tiene la capacidad de activar al feto o volver en otro momento si realmente no se han conseguido imágenes de calidad por la posición fetal.
De todas maneras, no te sientas decepcionada, lo importante es que el resto de pruebas salgan bien y pronto tendrás a tu bebé en tus brazos y ¡podrás verlo tanto como quieras!
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Artículo especializado
Densitometría Osea, ¿Cómo Están Tus Huesos?
La densitometría ósea es la prueba principal para valorar la densidad mineral ósea , es decir, el calcio en los huesos y, por tanto, la presencia de una patología que afecta a un elevado sector de la población, la osteoporosis. A nivel mundial, la sufren 200 millones de personas, y en España, concretamente, afecta al 35% de mujeres de más de 50 años y al 72% mayores de 70 años.
Es una patología que afecta sobre todo a la calidad de vida debido al deterioro que sufre la calidad de los huesos y el elevado riesgo de fracturas asociado a ello. El impacto de esta enfermedad sobre la población es tan elevada que algunos expertos hablan de que “las fracturas por osteoporosis superan el total de casos de infarto agudo al miocardio, paro cardiaco y cáncer de mama juntos”, con el agravante de que las fracturas, en la mayoría de ocasiones, pasan desapercibidas y pueden ocasionar muchos problemas a posteriori.
Para reducir el riesgo de osteoporosis , las sociedades médicas recomiendan la realización de pruebas de valoración de la densidad mineral ósea, y la prueba que mejores resultados da es la absorciometría dual de rayos x (DXA o DEXA ) o también conocida como densitometría ósea.
¿En qué consiste?
Es una técnica de diagnóstico por la imagen en la que existe radiación de rayos X, pero la radiación total es muy baja si se compara con la que recibe el paciente que se somete a una radiografía convencional de tórax (20 veces inferior a ésta), por lo que el riesgo-beneficio es evidente. A diferencia de otras pruebas en los que se emiten rayos X, en este caso no es necesario usar protectores de plomo al estar muy concentrada la zona a valorar.
Es necesario informar al profesional que realiza la prueba si hay posibilidad de estar embarazada, así como si en las dos semanas previas nos hemos realizado algún estudio de radiodiagnóstico en el que se haya recibido contraste. Si este fuera el caso sería necesario esperar unas dos semanas para poder someterse a la DEXA. Tanto el embarazo como el contraste son contraindicaciones para su realización, en el primer caso absoluta y en el segundo caso temporal.
El paciente se tumbará en una camilla durante 10 a 20 minutos. Si se quiere estudiar la columna la posición será con las piernas elevadas y flexionadas encima de una especie de almohada cuadrada o triangular, mientras que si la valoración es de la cadera las piernas estarán estiradas, pero con una abrazadera que mantiene la posición idónea para realizar el estudio. Es importante mantenerse inmóvil durante el momento en que se realiza la prueba para evitar que la imagen quede distorsionada y pueda interferir en la posterior valoración.
¿CÓMO ME PREPARO PARA LA PRUEBA?
Para la realización del examen no se requiere de ninguna preparación específica, y se puede seguir una dieta normal . En cuanto la ropa, se recomienda llevar ropa cómoda y holgada que no comprima, evitando aquellas que tengan material metálico ya que en este caso será necesario sacársela. En ocasiones se solicita al paciente que se ponga una bata en lugar de su ropa pare evitar inconvenientes. Será necesario quitarse joyas, relojes y otros accesorios.
Los resultados
Las imágenes y los resultados que se derivan de la prueba los valorará el profesional. Estos situarán al paciente en un estrato diagnóstico en función de dos valores mundialmente aceptados como referentes:
T-Score: este valor muestra la cantidad ósea que presenta el paciente, comparado con un adulto joven del mismo género con masa ósea máxima.
Una puntuación superior a -1 se considera normal. Una puntuación entre -1 y -2,5 se clasifica como osteopenia (masa ósea baja). Una puntuación inferior a -2,5 se define como osteoporosis. La puntuación T se utiliza para calcular el riesgo que tiene de desarrollar una fractura.
Z-Score: este valor muestra la cantidad ósea que presenta el paciente en comparación con otras personas de su grupo étnico, edad y género. La valoración de la Z-score puede ser de utilidad en mujeres premenopáusicas y en varones en quienes la validez de la clasificación de la OMS (Organización Mundial de la Salud) no se encuentra establecida, así como en la monitorización de pacientes sometidos a intervenciones terapéuticas.
Pueden existir diferencias entre los resultados de una localización u otra y ello queda reflejado en la gráfica que suele acompañar el informe final que entrega el especialista al paciente. Los colores de las distintas zonas sitúan al paciente en zona de mayor o menor riesgo en función de su densidad mineral ósea.
Debido a su relativa baja inocuidad y los buenos resultados que ofrecen se han establecido unas indicaciones para su realización siendo estas las siguientes:
Mujeres ≥ 65 años
Personas que sufran enfermedades en las que exista pérdida de masa mineral ósea
Mujeres posmenopáusicas (< 5 años):
Uno o más factores de riesgo.
Historia personal o familiar de fractura (una historia materna de factura dobla el riesgo para el paciente).
Si los resultados pueden influir sobre intervenciones terapéuticas.
Hábito tabáquico activo.
Utilización de esteroides por vía oral durante más de tres meses.
Contenidos sobre enfermedades
Somos conscientes de que los conceptos médicos pueden resultar confusos si no te los explican con claridad. Para evitar esto, le hemos pedido a nuestros profesionales que preparen estas fichas en donde podrás acceder a información relevante sobre enfermedades que te ayudará a entender de una manera sencilla por qué se producen y por qué es necesario su tratamiento.
Ver todas las enfemedades 
Enfermedad
Ovarios Poliquísticos
Actualizado el día 15/09/2021
El síndrome del ovario poliquístico es la patología endocrina más frecuente en mujeres en edad fértil, aunque permanece infradiagnosticado. Se trata de un síndrome complejo y heterogéneo en cuanto a su presentación, evolución y consecuencias a corto y largo plazo.
¿Qué es el síndrome de ovarios poliquísticos?
El síndrome de ovarios poliquísticos determina la aparición de quistes (pequeñas cavidades llenas de líquido) en los ovarios, debido a una producción excesiva de hormonas masculinas.
El síndrome de ovarios poliquísticos agrupa una colección de signos y síntomas que incluye, además de la producción de hormonas masculinas por encima de lo normal, disfunción ovulatoria con prolongación, disminución de la frecuencia o ausencia de los períodos menstruales con escasa liberación de óvulos y aparición de quistes en los ovarios .
El signo clínico más característico determinado por el hiperandrogenismo es el hirsutismo o exceso de vello siguiendo un patrón masculino. También puede aparecer acné y alopecia.
Esta alteración endocrina afecta aproximadamente a 1 de cada 10 mujeres en edad reproductiva y está relacionado directamente con la disminución de la fertilidad.
Causas del síndrome de ovarios poliquísticos
Como en la mayoría de los síndromes, no existe una única causa para los ovarios poliquísticos. Sí existe una disfunción neuroendocrina con un exceso de hormona luteinizante, que es la encargada de regular la secreción de testosterona, impidiendo a los óvulos madurar lo suficiente y que, en lugar de ser expulsados de los ovarios durante la ovulación, permanezcan en el interior formando los quistes.
También existe un trastorno metabólico con resistencia a la insulina e hiperinsulinemia, lo que también estimula la producción de andrógenos.
Otros factores que se relacionan con la enfermedad y que pueden influir en el desarreglo hormonal son la obesidad , una alimentación deficiente y una vida sedentaria, entre otros.
Finalmente, el síndrome de ovario poliquístico puede tener causas genéticas, por alteración o mutación de genes, lo que determina que sea una patología altamente hereditaria.
Síntomas
Los síntomas del síndrome de ovarios poliquísticos pueden incluir:
Menstruaciones irregulares . Es común la oligomenorrea (disminución hasta 6-8 reglas anuales) o amenorrea (ausencia de regla durante varios periodos menstruales seguidos). Estos ciclos menstruales irregulares se asocian con una disminución en la ovulación y mayores tasas de infertilidad.
Hirsutismo y síntomas virilizantes . El exceso de hormonas masculinas (hiperandrogenismo) determina la aparición de síntomas virilizantes, como el aumento de vello en diferentes zonas como la cara, muslos, abdomen, espalda y antebrazos. Otros síntomas incluyen clitoromegalia, alopecia, voz grave, hipotrofia mamaria y aumento de la masa muscular.
Acné y piel grasa.
La resistencia a la insulina puede conducir a la aparición de diabetes, hipertensión arterial, aumento del colesterol y obesidad, entre otros.
Aumento de peso .
Dolor pélvico .
Manchas de color marrón oscuro en la piel.
Pruebas y exámenes para el diagnóstico del síndrome de ovarios poliquísticos
En un tercio de las mujeres pasan más de 2 años hasta que se les diagnostica la enfermedad. De ahí que se deba poner el foco en dos cuestiones específicas para identificar a los pacientes con mayor riesgo: mujeres con exceso de vello corporal o facial con un patrón masculino y mujeres con un historial de irregularidad menstrual u oligoamenorrea.
Las pruebas complementarias y exámenes para el diagnóstico del síndrome de ovarios poliquísticos deben incluir:
Examen físico.
Examen pélvico.
Análisis de sangre completo que incluya determinaciones hormonales, en especial, las hormonas masculinas.
Ecografía ginecológica de alta resolución.
Tratamiento del síndrome de ovario poliquístico
El síndrome de ovario poliquístico no tiene cura, pero sí se pueden establecer metas terapéuticas para diferentes aspectos de la enfermedad.
Tratamiento no farmacológico
Los cambios en el estilo de vida pueden suponer una mejora considerable de los diferentes parámetros alterados por la enfermedad. La pérdida de peso, una alimentación sana y realizar ejercicio físico de manera regular puede favorecer la regulación hormonal, mejorar la sensibilidad a la insulina, aumentar la fertilidad y hacer que mejoren todos los síntomas.
Tratamiento farmacológico
Los anticonceptivos hormonales pueden ser adecuados para regular la producción de hormonas y de esta manera normalizar el ciclo menstrual. También pueden incidir positivamente sobre el acné y el crecimiento del vello corporal.
El tratamiento hormonal como los antiandrógenos que regulan el nivel de las hormonas masculinas mejoran el acné y el vello corporal.
Por otro lado, el uso de antidiabéticos orales como la metformina puede ayudar a regular los niveles de insulina y, por tanto, a regular los ciclos menstruales.
Por último, se pueden utilizar inductores de la ovulación en el caso de pacientes que deseen quedarse embarazadas.
Factores desencadenantes del síndrome del ovario poliquístico
Como en la mayoría de síndromes, no existe un único desencadenante del síndrome del ovario poliquístico.
Por el contrario, existen diversos factores que pueden determinar un mayor riesgo de que aparezca la patología.
Factores de riesgo de los ovarios poliquísticos
Los factores de riesgo del síndrome de ovarios poliquísticos pueden incluir una alimentación deficiente, el exceso de peso y la obesidad y una vida sedentaria. También puede haber factores genéticos que hacen que la enfermedad sea hereditaria en base a determinados cambios o mutaciones genéticas.
Complicaciones
Las mujeres que padecen el síndrome de ovario poliquístico pueden presentar una serie de complicaciones asociadas, entre ellas:
Síndrome metabólico.
Diabetes tipo 2 y obesidad.
Hipertensión arterial.
Enfermedades cardiovasculares.
Trastornos menstruales, infertilidad y abortos.
Crecimiento excesivo de vello.
Apnea obstructiva del sueño.
Cáncer de endometrio.
Depresión y ansiedad.
Prevención
Existe una serie de recomendaciones que pueden ayudar a reducir el riesgo de padecer la enfermedad y, en todo caso, atenuar los síntomas y regular los ciclos menstruales. Además del tratamiento médico, es importante conseguir una buena calidad de vida eliminando el estrés, realizar ejercicio físico de manera regular, mantener una dieta saludable y evitar el exceso de peso y la obesidad.
Especialidades para el síndrome del ovario poliquístico
El síndrome de ovarios poliquísticos es tratado por los médicos especialistas en Endocrinología y en Ginecología.
¿Necesitas atención presencial con un especialista en ginecología? En Savia reserva una consulta con los mejores profesionales sin esperas.
Preguntas frecuentes
¿Cuáles son los síntomas de quistes en los ovarios?
Los síntomas de quistes en los ovarios son dolor en la parte baja del abdomen, hinchazón y sensación de plenitud abdominal, dolor durante las relaciones sexuales o dolor durante la defecación, entre otros.
¿Qué riesgos implica el ovario poliquístico?
El síndrome de ovario poliquístico aumenta el riesgo de infertilidad, cáncer de endometrio, metabolismo anormal de la glucosa y dislipidemia.
¿Qué produce quistes en los ovarios?
Los quistes de ovarios suelen tener un componente genético, pero también se producen por una alteración hormonal, endometriosis, embarazo, infecciones pélvicas o el síndrome de ovarios poliquísticos.
¿Cuál es el tamaño normal de un quiste de ovario?
Un quiste de ovario suele medir menos de 5 cm. En el síndrome de ovarios poliquísticos suelen aparecer al menos 12 folículos que suelen medir de 2 a 10 mm.
¿Qué son los folículos de los ovarios?
Los folículos son estructuras anatómico-funcionales que forman parte del ovario y que albergan en sus paredes internas al ovocito y a otras células productoras de estrógenos.
¿Qué es un quiste funcional?
En los ovarios se producen folículos que son estructuras funcionales que producen hormonas y liberan el óvulo durante la ovulación. Cuando un folículo normal continúa creciendo, se denomina quiste funcional. No suelen causar síntomas y desaparecen por sí solos.
¿Cuánto tiempo tarda en quitarse un quiste de ovario?
Por norma general, un quiste de ovario se rompe en el momento de la ovulación, pero algunos resisten y pueden tardar hasta 3 meses en desaparecer.
Bibliografía
Sociedad Española de Ginecología y Obstetricia. Estudio y tratamiento de la anovulación en el síndrome de ovarios poliquísticos. Prog Obstet Ginecol 2017; 60(5): 505-516 .
Azziz R. Polycystic Ovary Syndrome. Obstet Gynecol 2018; 132(2): 321-336. doi: 10.1097/AOG.0000000000002698 .
McCartney CR, Marshall JC. Polycystic Ovary Syndrome. N Engl J Med. 2016 Jul 7;375(1):54-64. doi: 10.1056/NEJMcp1514916 .

Enfermedad
Síndrome premenstrual
¿Qué es el síndrome premenstrual?
El síndrome premenstrual (SPM) es un conjunto de síntomas y cambios físicos y psíquicos, bien definidos, que experimentan las mujeres días antes de la menstruación (entre el día 14 y 28). Esto sucede mes tras mes y puede afectar al 90 % de las mujeres, y con mayor frecuencia entre los 20 y 30 años de edad.
La intensidad de los síntomas puede variar de unas mujeres a otras y pueden ser simples molestias o ser tan agudos que el malestar que ocasionan pueden interferir e incluso incapacitar en las actividades diarias o laborales.
El síndrome premenstrual termina cuando empieza la regla .
Tipos de síndrome premenstrual
No existen tipos de síndrome premenstrual.
Causas de un síndrome premenstrual
No se sabe con exactitud cuales son las causas del síndrome premenstrual , pero podría estar relacionado con un desequilibrio hormonal de estrógenos y progesterona. Esto produce una retención de líquidos y sodio que provocaría un aumento de peso y edema generalizado dando lugar a los síntomas premenstruales.
También se desconocen las causas por las que unas mujeres son más sensibles que otras a estos cambios hormonales.
Síntomas de un síndrome premenstrual
Los síntomas del síndrome premenstrual pueden ser:
Síntomas físicos:
Hinchazón de abdomen
Edemas generalizados por retención de líquidos
Tensión e inflamación de las mamas
Diarrea o estreñimiento
Calambres
Dolor de cabeza y espalda
Intolerancia a la luz y al ruido
Acné
Síntomas psicológicos o emocionales:
Cambios repentinos del estado de ánimo
Irritabilidad
Cansancio
Ansiedad
Tristeza o depresión
Cambios de apetito como la necesidad de comer dulce
Trastornos del sueño
Pérdida de interés en el sexo
Pérdida de concentración
Tratamiento de un síndrome premenstrual
El tratamiento del síndrome premenstrual puede ser:
Tratamiento médico: para aliviar los síntomas como los antiinflamatorios, analgésicos, diuréticos, antidepresivos o anticonceptivos hormonales, entre otros.
Remedios caseros: ayudan a paliar los síntomas como la actividad física diaria, evitar la sal, cafeína, alcohol y azúcar los días previos al ciclo, no fumar, controlar el estrés, descansar y dormir más horas, o llevar una dieta saludable con más vitaminas y minerales durante esos días previos.
Pruebas complementarias de un síndrome premenstrual
No hay pruebas específicas para diagnosticar el síndrome premenstrual , basta con la descripción de los síntomas, en qué momento aparecen y si se repiten durante al menos tres ciclos menstruales para poder diagnosticar el síndrome premenstrual.
Factores desencadenantes de un síndrome premenstrual
El factor desencadenante se debe a la disminución de los niveles de estrógeno y progesterona después de la ovulación. Cuando comienza la menstruación, los niveles de estas hormonas comienzan a subir de nuevo. S e desconoce porqué unas mujeres son más sensibles que a otras .
Factores de riesgo de un síndrome premenstrual
No hay factores de riesgo.
Complicaciones de un síndrome premenstrual
Las posibles complicaciones de un síndrome premenstrual pueden ser la incapacidad del desarrollo de las actividades diarias y laborales, pensamientos suicidas e incluso suicidio en las mujeres con depresión, por eso es importante ajustar el tratamiento esos días puntuales .
Prevención de un síndrome premenstrual
No existe prevención para evitar el síndrome premenstrual.
Especialidades a las que pertenece
El síndrome premenstrual es tratado por el médico de Atención Primaria , que trata los síntomas y recomienda pautas para aliviarlos, pero cuando el síndrome premenstrual afecta de manera más intensa o incapacita el ritmo de vida diario es el Ginecólogo (médico del aparato reproductor femenino) quien hace un seguimiento y tratamiento del síndrome premenstrual.
Preguntas frecuentes
¿Cuándo aparecen los primeros síntomas del embarazo?
Los primeros síntomas de embarazo es la ausencia de regla, senos hinchados, cansancio y somnolencia, orinar más a menudo, náuseas y vómitos, hinchazón abdominal y dolor pélvico, entre otros.
¿Cuándo se presenta el síndrome premenstrual?
El síndrome premenstrual se presenta cuando aparecen una serie de síntomas concretos días antes de la regla, durante al menos 3 meses.
¿Cuánto es lo máximo que dura el periodo menstrual?
El periodo menstrual puede durar entre 25 y 30 días, incluso alargarse a 35 días.
¿Cuáles son los trastornos menstruales?
Los trastornos menstruales pueden ser náuseas, vómitos, dolor abdominal tipo retortijón, dismenorrea (dolor menstrual), dolor de espalda, diarrea o dolor de cabeza, entre otros.
¿Cuánto tiempo pueden durar los síntomas premenstruales?
Los síntomas pre menstruales duran unos días antes de la aparición de la regla. Suelen estar presentes en los años entre la adolescencia y la vida adulta, es decir, entre los 20 y 30 años.

Enfermedad
Mioma Uterino
¿Qué es el mioma uterino?
El mioma o fibroma uterino, es un tipo de tumoración benigna en las paredes del útero y está formado por un incremento en forma de nódulo de las fibras musculares del útero .
Los miomas varían en número, tamaño y localización. Afecta a mujeres en edad fértil y su origen es desconocido , pero su crecimiento está muy influenciado por las hormonas femeninas.
Tipos de mioma uterino
Los miomas uterinos pueden ser:
Mioma subseroso: tiene una afectación en mujeres del 40% de miomas. No produce síntomas, pero si alcanza un tamaño grande puede producir molestias y dolor por compresión en órganos próximos.
Miomas intramusculares: debido a que pueden alcanzar gran tamaño, puede aumentar, también, el tamaño del útero. Constituye el 55% de los miomas y se suelen localizar en la porción central del miometrio (capa muscular intermedia).
Mioma submucoso: son menos frecuentes, dan más sintomatología al producir mucho sangrado menstrual provocando, en muchos casos, que la mujer padezca anemia ferropénica (falta de hierro). Tiene una elevada probabilidad de malignizar.
Causas de un mioma uterino
No se conocen las causas del mioma de útero, pero se ha detectado una relación directa con las hormonas femeninas , condicionando el desarrollo y crecimiento de los miomas, por eso se da en mujeres en edad fértil (desde la pubertad hasta la menopausia). Transcurrido este tiempo, el tamaño disminuye debido a que los niveles de hormonas en sangre son menores.
Síntomas de un mioma uterino
Aproximadamente el 30% de las mujeres no tienen ningún síntoma y solo se descubre su presencia de un mioma uterino en las revisiones rutinarias con el ginecólogo .
La aparición de los síntomas depende de su tamaño, número de miomas y localización, siendo los más sintomáticos los que se localizan en la cavidad interna del útero.
Los síntomas pueden ser:
Cambios menstruales en su duración, frecuencia y cantidad de sangrado.
Dolor.
Anemia ferropénica debido al exceso de sangrado.
Aumento del perímetro del abdomen en caso de miomas grandes.
Aumento de peso.
Complicaciones en embarazo y parto.
Compresión de vejiga y recto en el caso de miomas de gran tamaño.
Necesidad de orinar con mayor frecuencia.
Lumbalgia y dolor en pelvis.
Infertilidad.
Aumento de probabilidades de aborto o parto prematuro.
Molestias en las relaciones sexuales.
Tratamiento de un mioma uterino
La mayoría de los miomas no requieren tratamiento por ser asintomáticos, y se tiende a tener una actitud conservadora.
En caso de presentar sintomatología, el tratamiento puede ser:
Tratamiento médico:
Fármacos (agonistas de la GnRH) que disminuyen el nivel de estrógenos en sangre y, con ello, el tamaño de los miomas, pero tiene efectos secundarios con sintomatología similar a una menopausia (sofocos, sudoración, sequedad vaginal, etc.) y, además, cuando se termina el tratamiento, el mioma vuelve a crecer.
Analgésicos para paliar el dolor.
Anticonceptivos, progestágenos y dispositivos uterinos para disminuir la hemorragia.
Hierro para tratar la anemia.
Tratamiento quirúrgico:
Se emplea dependiendo de tamaño y localización del mioma.
Se puede realizar por vía vaginal o laparoscópica (tubo flexible con una cámara e instrumentos quirúrgicos, que se introduce por unas incisiones realizadas en el abdomen). Pueden ser:
Miomectomía, en la que se extirpa sólo el mioma, se conserva el útero y se preserva la fertilidad.
Histerectomía, en la que se extirpa una parte o la totalidad del útero, dependiendo de la localización y tamaño del mioma. Se preserva la función hormonal por conservar los ovarios, pero no hay posibilidad de embarazo.
Radiología intervencionista: técnica guiada por rayos usada para embolizar los miomas, es decir, suspender el riego sanguíneo del mioma.
Pruebas complementarias de un mioma uterino
Algunas pruebas complementarias para el diagnóstico de un mioma uterino son:
Exploración física: para detectar el tamaño del útero, presencia de miomas y dolor a la palpación.
Ecografía: para localizar, medir y determinar cuántos miomas hay. Es la prueba diagnóstica más efectiva y fiable.
Histeroscopia: se introduce un tubo por la vagina para ver el interior del útero.
TAC pélvico: para observar la repercusión de los órganos vecinos.
Resonancia magnética: para visualizar posibles tumores.
Factores desencadenantes de un mioma uterino
Los factores desencadenantes de los miomas uterinos están causados por el aumento de estrógenos en sangre .
Factores de riesgo de un mioma uterino
Los factores de riesgo de un mioma pueden ser:
Mujeres de entre 35 y 45 años.
Mayor incidencia en la raza afroamericana.
Obesidad, hipertensión o diabetes.
Mujeres nulíparas (no han dado a luz).
Desarreglo hormonal (aumento de estrógenos).
Factor hereditario.
Complicaciones de un mioma uterino
Las complicaciones del mioma uterino pueden ser:
Compresión de vejiga y retención urinaria.
Edemas, varices y trombosis en las piernas, por compresión de venas pélvicas dificultando la circulación de retorno de las piernas.
Hemorragias abundantes.
Malignización del mioma, suele ocurrir en un 0,5 % de los miomas.
Prevención de los miomas
Los miomas no se pueden prevenir debido a que no se sabe con exactitud la causa .
Se pueden hacer unas recomendaciones como son las revisiones ordinarias con el ginecólogo, controlar el peso y llevar una dieta saludable junto con la práctica regular de ejercicio físico.
Especialidades a las que pertenece
La especialidad médica que trata los miomas es Ginecología y Obstetricia.
Preguntas frecuentes
¿Cuál es el tamaño de un mioma uterino?
Los miomas varían en tamaño, siendo los más pequeños de hasta 2 cm. y los grandes a partir de 6 cm .
¿Cuál es la diferencia entre un mioma y un fibroma?
Es lo mismo un mioma que un fibroma. También se pueden llamar leiomiomas .
¿Qué son miomas tipo 4?
Los miomas tipo 4 son miomas que ocupan un 50% del volumen del interior del útero .
¿Qué es un mioma en el endometrio?
Un mioma en el endometrio es aquel que crece hacia la cavidad uterina, es decir, hacia la mucosa que recubre la pared del útero .
¿Cuándo una mujer tiene miomas puede quedar embarazada?
Los miomas son compatibles con el embarazo, pero, en ocasiones, pueden aparecer complicaciones durante la gestación (abortos, partos prematuros o alteración en el desarrollo fetal), en el parto (hemorragias, mala presentación del feto o dificultad en las contracciones), y en el postparto (hemorragias).

Enfermedad
Vaginosis Bacteriana
¿Qué es la vaginosis bacteriana?
La vaginosis bacteriana es una infección vaginal por una bacteria , se produce por el desequilibrio entre la diferente flora bacteriana de la vagina, en la cual se produce un descenso de los lactobacilos y un aumento de la gardnerella (bacilo de la región genital). Es la infección bacteriana más frecuente entre los 14 y 40 años, y es una enfermedad leve.
Tipos de vaginosis
Los tipos de vaginosis serán diferentes según el germen que lo produce, así tenemos:
Vaginosis bacteriana : se produce por el germen conocido como Gardnerella vaginalis.
Vaginitis candidiasica o candidiasis vaginal : se debe a la infección por hongo Candida albicans , produce un flujo blanco y espeso.
Vaginitis tricomoniasis : se produce por el protozoo Trichomona vaginalis.
Vaginitis por clamidia : producida por la Chlamydia trachomatis
Causas de la vaginosis bacteriana
La causa de la vaginosis bacteriana es la infección por parte de la Gardnerella vaginalis.
Síntomas de vaginosis bacteriana
La vaginosis bacteriana en la mayoría de los casos es asintomática , o presenta síntomas muy leves. Cuando aparecen síntomas, estos son, la presencia de flujo delgado y abundante con olor a pescado , de un color que puede ser blancuzco, gris apagado o incluso verdoso, las pacientes también pueden presentar ciertas molestias como ardor al orinar o ligero picor, en algunos casos poco frecuentes puede dar dolor suprapúbico.
Tratamiento para la vaginosis bacteriana
El tratamiento de la vaginosis bacteriana va a ser tratamiento antibiótico , que puede ser de uso oral, en forma de óvulos vaginales, o geles. Los antibióticos que se suelen usar son el Metronidazol o Clindamicina .
Pruebas complementarias del tratamiento de vaginosis bacteriana
La prueba complementaria será un exudado vaginal , aunque también se puede encontrar mediante citología en aquellas personas que no presentan sintomatología y por tanto no consultan por este problema.
Factores desencadenantes de la vaginosis bacteriana
No se conocen las causas que desencadenan las vaginosis bacterianas, si bien se conoce que las personas con relaciones sexuales con múltiples parejas pueden sufrir esta infección. No se encuentran casos de vaginosis bacteriana en personas que no tienen relaciones sexuales.
Factores de riesgo de la vaginosis bacteriana
Son factores de riesgo las duchas vaginales, el uso de productos de higiene femenina muy perfumados o que puedan ser irritantes, y el uso de ropa ajustada y que no transpire.
Complicaciones de la vaginosis bacteriana
La vaginosis bacteriana es una infección local que no presenta complicaciones.
Prevención de la vaginosis bacteriana
Evitar las duchas vaginales.
Evitar el uso de jabones abrasivos.
Usar preservativo para evitar contagios.
Ropa interior de algodón.
Especialidades a las que pertenece la vaginosis bacteriana
La vaginosis bacteriana será tratada en primer lugar por el médico de familia, solo en casos que sean recidivantes puede ser necesario el tratamiento por parte del ginecólogo.
Preguntas frecuentes
¿Qué es la candidiasis bacteriana?
No existe la candidiasis bacteriana. La candidiasis es un infección producida por un hongo conocido como Cándida albicans , que, al reproducirse por alteraciones locales en mayor cuantía de lo normal, da lugar a una infección que se caracteriza por picor intenso , asociado a producción de flujo blanquecino y espeso. Las bacterias son un tipo de células diferentes que producen otras infecciones como la vaginosis bacteriana.
¿Qué es la vulvovaginitis?
La vulvovaginitis es la inflamación tanto de la vulva como de la vagina, la paciente presenta síntomas internos de molestias vaginales, asociados a picor externo y, en muchos casos, ardor al orinar, ya que el paso de la orina da lugar a un irritación local de la vulva. Precisará tratamiento interno de la vagina y externo de la vulva para mejorar los síntomas. Puede ser producida por bacterias y hongos.
¿Hay algún remedio casero para aligerar los síntomas de la vaginosis bacteriana?
Para tratar la vaginosis bacteriana son necesarias medidas que cambien el PH vaginal, haciéndolo más ácido. Así, al añadir vinagre de manzana al agua de lavarse puede ser eficaz, el consumo y aplicación de yogur natural puede ser otro tratamiento, añadir al agua de lavarse el aceite del árbol de té puede ser también cambiar el PH vaginal, impidiendo las infecciones de repetición. Evitar el uso exagerado de productos de higiene femenina que pueden ser irritantes y cambiar el PH por sí mismo.
¿Qué es la enfermedad Gardnerella?
La Gardnerella es una bacteria conocida como Gardnerella vaginalis , que produce una infección en la vagina conocida como vaginosis bacteriana, que se debe a una alteración de la flora vaginal donde disminuyen los Lactobacillus y prolifera la Gardnerella , es la principal causa de alteración vaginal aunque hasta el 50 de las personas que la presentan no tiene síntomas.
¿Qué es una célula clave?
La célula clave es una célula pavimentosa de la vagina, que se encuentra rodeada de bacterias, en general Gardenella vaginaleis , las baterias se hayan pegadas a la pared celular y son típicas de la infección por esta bacteria.
Artículos por especialidad
CertificadosAlergologíaAnatomía PatológicaAnestesiología y ReanimaciónAngiología y Cirugía VascularAnálisis ClínicosAparato DigestivoCardiologíaChequeosCirugía General y del Aparato DigestivoCirugía General y del Aparato Digestivo PediátricaCirugía Oral y MaxilofacialCirugía Ortopédica y TraumatologíaCirugía Ortopédica y Traumatología PediátricaCirugía PediátricaCirugía Plástica y ReparadoraCirugía TorácicaClínica u HospitalDermatología Médico-Quirúrgica y VenereologíaEndocrinología y NutriciónEnfermeríaFisioterapiaGenética HumanaGinecología y ObstetriciaInmunologíaLogopedia y FoniatríaMedicina Estética y Unidad LaserMedicina Física y RehabilitaciónMedicina GeneralMedicina InternaMedicina NuclearMedicina del DeporteNefrologíaNeumologíaNeurocirugíaNeurofisiología ClínicaNeurologíaNutrición y DietéticaOdontología y EstomatologíaOftalmologíaOncología MédicaOncología RadioterápicaOsteopatíaOtorrinolaringologíaPediatríaPodologíaPoliclínicasPreparación al PartoPsicologíaPsiquiatríaRadiodiagnóstico-Diagnóstico Por ImagenReumatologíaTricologíaUnidad del DolorUrgencias HospitalariasUrología
Todas las especialidades  Savia
Savia