Análisis Clínicos
La especialidadArtículos especializados
Enfermedades
Síntomas
Otros contenidos
Artículo especializado
¿Qué Detecta un Hemograma y Cómo Interpretarlo?
Detectar precozmente enfermedades, algunas de ellas graves, puede ser tan sencillo como realizarse hemogramas de control con frecuencia. Descubre la importancia de estos análisis.
La sangre es un tejido corporal que aparenta ser un líquido homogéneo, pero está compuesta por varios tipos celulares diferenciados, que flotan en una mezcla de agua y sustancias químicas denominada suero o plasma sanguíneo. Sirve para el transporte del oxígeno y los nutrientes a todas las células del organismo, así como otros elementos como hormonas, minerales, vitaminas…
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
¿En qué consiste?
El hemograma o hematimetría es una prueba que consiste en un recuento completo de las células sanguíneas, así como una valoración de la estructura y forma normales de éstas, a partir de una pequeña muestra de sangre. En el pasado era un proceso arduo debido a que se realizaba el recuento de forma manual, observando al microscopio, pero hoy en día los hemogramas automatizados permiten conocer con comodidad, rapidez y precisión los resultados. Una cantidad anormal de cualquiera de las células puede ser indicativo de enfermedad.
¿Cómo se realiza?
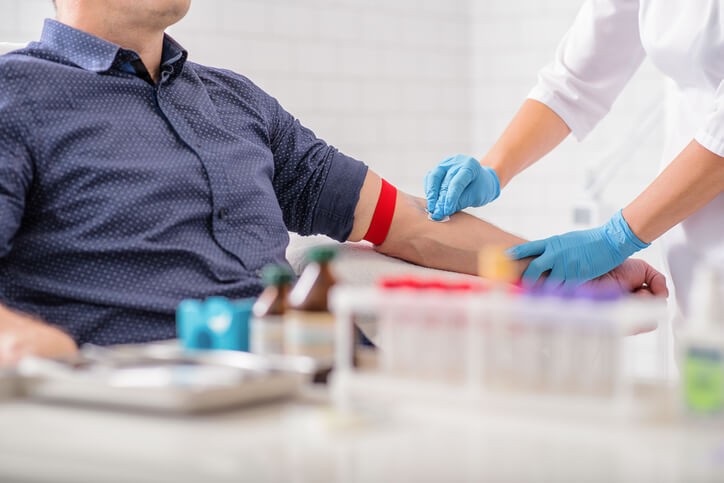
Se extrae una pequeña cantidad de sangre venosa para proceder a determinar su composición a través de un análisis de laboratorio. Generalmente, se realiza manteniendo el ayuno de al menos seis horas, puesto que la ingesta de alimentos/líquidos puede alterar mucho los resultados. Al margen de este requisito, no requiere de ninguna otra preparación especial más.
Las muestras se extraen con una jeringa o dispositivo similar (de baja presión), generalmente de venas cercanas a la flexura del codo. Primero se coloca una goma elástica atada alrededor del brazo del paciente para resaltar la vena a puncionar y así, facilitar la tarea. Cuando se ha extraído la cantidad de sangre necesaria, se retira la aguja y se ejerce un poco de presión en la zona de puntura con un algodón durante unos minutos, para evitar el manchado de sangre y la aparición de hematomas. Todo el procedimiento dura unos cinco minutos. Si sólo son necesarias unas gotitas de sangre, basta con hacer una pequeña punción con aguja en una de las yemas de los dedos y aplicar una presión suave sobre el mismo para que fluya la sangre necesaria.
Una vez obtenida la muestra, se etiqueta el recipiente en el mismo lugar con un código de barras, que contiene la información necesaria para asociarla al paciente en cuestión. Después es enviada al laboratorio en unos contenedores. El personal del área de recepción del laboratorio las clasifica dependiendo de los parámetros solicitados. A partir de ahí, los recipientes pasan a los aparatos de análisis del laboratorio para las pruebas que se requieran en cada caso.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
NO TE ALARMES SI…
Los valores no coinciden. Dependiendo del laboratorio hay ligeras variaciones en los “valores de referencia”. También pueden ser valores distintos porque se usen unidades de medición diferentes.
Hay tres tipos principales de células en la sangre:
Hematíes o eritrocitos o glóbulos rojos: son los corpúsculos celulares que transportan el oxígeno que necesitan las células de todo el organismo para respirar. En su interior contienen la hemoglobina, que lleva hierro y es lo que le otorga el color rojo a la sangre. (Valores normales (VN): 4,5-6,5 mill/mm3 en varones; 3,8-5,8 mill/mm3 en mujeres).
Cuando la concentración de hemoglobina disminuye (valores bajos en la analítica) aparecen las anemias; las más frecuentes en la población se llaman ferropénicas, porque se deben al déficit de hierro. Los valores de ferritina nos indican cuánto hierro se encuentra depositado en el organismo.
Leucocitos o glóbulos blancos : son las células de defensa frente a agentes patógenos (VN: 5000-10.000/mm3). Pueden ser:
Granulocitos o polimorfonucleares: a su vez se subdividen en neutrófilos, encargados de la defensa frente a microorganismos, eosinófilos, que combaten los parásitos y basófilos, que intervienen en las reacciones de hipersensibilidad.
Linfocitos: se encargan de fabricar anticuerpos y de la defensa contra virus y células tumorales.
Plaquetas: son las encargadas de taponar las heridas, iniciar la formación del coágulo sanguíneo e impedir la pérdida de sangre por hemorragia. (VN: 150.000-350.000/mm 3 ). Las células de nuestra sangre se generan en la médula ósea de algunos huesos, donde unas células precursoras denominadas ‘hematopoyéticas’ las van fabricando y liberando al torrente sanguíneo una vez maduradas.
Otros parámetros posibles de ser analizados en un hemograma son los siguientes:
Hematocrito: es el tanto por ciento de hematíes en el volumen total de la sangre. Es un buen indicador para valorar las anemias. Valores normales (VN): 40-54% en varones; 37-47% en mujeres).
Hemoglobina: (VN: 14-18 g/dL en varones; 12-16 g/dL en mujeres).
VCM (Volumen corpuscular medio) y H.C.M ((Hemoglobina corpuscular media): el primero es un valor que refleja el tamaño de los hematíes (VN: 83-97 fl) y el segundo refleja el promedio de la cantidad de hemoglobina que contiene cada hematíe (V.N. 27-31 pg). Ambos sirven para poner unos “apellidos” cuando se diagnostica una anemia y diferenciar así los tipos (por ejemplo, anemia microcítica hipocroma o anemia normocítica normocroma…).
CHCM (Concentración de Hemoglobina Corpuscular Media): es el índice que relaciona la cantidad de hemoglobina que lleva cada hematíe con su volumen. (VN: 32-36 g/dL).
IDH (Índice de Dispersión de los Hematíes): indica la variación en el volumen de los glóbulos rojos. Si está elevado, refleja que los hematíes no son todos del mismo tamaño (fenómeno denominado anisocitosis). (VN: 11,5-14,5 (%)).
VSG (Velocidad de Sedimentación globular): es un indicador de la velocidad con que los hematíes se agregan y sedimentan. Es un valor muy inespecífico y no significa forzosamente enfermedad, ya que aumenta con la edad, la menstruación, el embarazo, la toma de anticonceptivos…También se encuentra alterado (elevado) en patologías como infecciones, tumores, anemias, enfermedades autoinmunes, etc. (VN: 1-13 mm/h en varones; 1-20 mm/h en mujeres).
VPM (Volumen Plaquetario Medio): es un término que en medicina se utiliza como medida para conocer el tamaño medio de las plaquetas sanguíneas. (VN: 5-15 fl).
TEN EN CUENTA QUE…
La presencia en los resultados de una analítica de una o varias anomalías sanguíneas no significa necesariamente que se padezca alguna enfermedad. Un análisis de sangre es una prueba complementaria en el diagnóstico y deben realizarse otras muchas, teniendo siempre como marco de referencia la historia clínica del paciente (síntomas, circunstancias personales, antecedentes familiares y personales, etc.), para poder obtener un diagnóstico final.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Artículo especializado
Fosfatasa Alcalina: ¿Hígado o Hueso?
Como has supuesto bien, si hablamos de fosfatasa alcalina es porque también existe la fosfatasa ácida. Tan sólo una pincelada para diferenciar ambas.
La fosfatasa ácida es una enzima repartida por todo el organismo que tiene cinco isoenzimas. Las isoenzimas son moléculas o proteínas muy parecidas entre ellas (tan sólo difieren en alguna pequeña secuencia) que participan en el mismo proceso metabólico. La isoenzima de la fosfatasa ácida más relevante en nuestra práctica clínica es la específica de la próstata o isoenzima 2. Sus valores están muy elevados en pacientes con cáncer de próstata. Por tanto, se solicita tanto para el diagnóstico como para el estudio de extensión del tumor. Nos ayudará en la monitorización de la respuesta al tratamiento.
La fosfatasa alcalina es un grupo de enzimas presentes en numerosos tejidos (hígado, hueso, riñón, intestino, placenta) y en células sanguíneas. Sus concentraciones más elevadas se observan en células óseas y hepáticas, por ello, concentraciones elevadas de fosfatasa alcalina en sangre suelen asociarse a trastornos hepáticos u óseos. Igual que en el caso de la fosfatasa ácida, posee diferentes isoenzimas en el organismo que identifican el origen.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
En adelante abordaremos la fosfatasa alcalina
Algunos tipos de cáncer producen isoenzimas de la fosfatasa alcalina que se detectan en sangre. Es el caso de pulmón, testículo (seminoma), próstata, laringe, páncreas, estómago, y colon.
En condiciones normales los niveles sanguíneos de fosfatasa alcalina proceden, a partes iguales, del hígado y el hueso . Puede haber oscilaciones durante el embarazo y en las edades extremas de la vida así como durante el crecimiento (en niños y adolescentes es característico hallar concentraciones de fosfatasa alcalina aumentadas, debido a su crecimiento óseo).
Por tanto, los resultados de la determinación de la fosfatasa alcalina deben interpretarse de manera diferente en niños y adultos.
¿En qué situaciones podemos encontrar unas fosfatasas alcalinas elevadas?
En primer lugar, sospecharemos una alteración hepática u ósea , aunque pueden existir otras causas. Podemos diferenciar los distintos tipos de isoenzimas de fosfatasa alcalina producidos por el organismo para identificar su procedencia. Los síntomas y signos acompañantes pueden orientarnos sobre el origen óseo o hepático de un aumento de la fosfatasa alcalina. Así mismo, al determinar la isoenzima especifica elevada podemos corroborar nuestra sospecha clínica.
Voy a mencionarte las principales causas de origen hepático que pueden ocasionar un aumento de fosfatasa alcalina: coledocolitiasis (presencia de cálculos en la vía biliar), tumor, pancreatitis crónica, quistes, divertículo duodenal, infección, colestasis (alteración en la excreción de la bilis), enfermedades metabólicas, cirrosis, hepatitis vírica, hepatitis alcohólica, etc.
De entre las principales causas de origen óseo podríamos mencionar cualquier situación que suponga una formación ósea excesiva : fracturas, tumores primarios y metastásicos, osteomielitis, enfermedad de Paget, osteomalacia, problemas hormonales, etc.
Otras causas no hepáticas ni óseas podrían ser: el li nfoma de Hodgkin, el infarto agudo de miocardio, la insuficiencia cardíaca congestiva, el infarto pulmonar , la colitis ulcerosa, la ingesta de algunos medicamentos (antigotosos, antidepresivos, antiepilépticos), etc.
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.
Si se detecta una elevación de fosfatasa alcalina…
Ante el hallazgo de una elevación de fosfatasa alcalina normalmente se descarta en primer lugar un origen hepático por lo que se solicita una analítica completa y una ecografía hepática . Si estas pruebas no nos permiten conocer si la causa es hepática u ósea, resulta de utilidad solicitar la determinación de las isoenzimas específicas de la fosfatasa alcalina.
El aumento de fosfatasa alcalina puede acompañarse de un aumento de los niveles de otras pruebas hepáticas como bilirrubina, aspartato aminotransferasa (AST) y alanina aminotransferasa (ALT). Si además la GGT también está aumentada, las probabilidades de que la causa sea hepática aumentan.
Los niveles de fosfatasa alcalina suelen interpretarse conjuntamente con los otros parámetros específicos del hígado. Por ejemplo, en caso de una hepatitis encontraremos la fosfatasa alcalina aumentada pero las transaminasas (AST y ALT) mucho más elevadas. Sin embargo, cuando existen obstrucciones de la vía biliar (por litiasis o piedras, por ejemplo) los aumentos de fosfatasa alcalina y de bilirrubina son muy superiores a los de las transaminasas. Ya sabes que existen otras muchas causas de elevación de fosfatasa alcalina como puede ser un cáncer de hígado.
Contrariamente, es posible que el aumento de fosfatasa alcalina sea de causa ósea en cuyo caso, muy probablemente, encontraremos el calcio y/o el fósforo alterados.
Enfermedad de Paget
Como hemos mencionado, una posible causa ósea sería la enfermedad de Paget que consiste en un trastorno metabólico que afecta a uno o varios huesos , fundamentalmente pelvis, vértebras, cráneo, fémur y tibia. Se caracteriza por un aumento inicial de destrucción ósea , seguido de un aumento de formación ósea compensatoria, dando lugar a un hueso aumentado de grosor y desorganizado, por tanto, más frágil que el sano. A pesar de que es una enfermedad asintomática en la mayoría de casos puede acompañarse de dolor óseo. Aparece generalmente a partir de los 50 años y es algo más frecuente en varones que en mujeres. Un porcentaje importante de pacientes son diagnosticados de forma casual al realizar una radiografía por otro motivo (donde se evidencia una calidad ósea alterada) o una analítica rutinaria donde se detecta la fosfatasa alcalina elevada (en este punto te quiero enfatizar, una vez más, la importancia de seguir los controles médicos rutinarios). Es interesante que sepas que una vez confirmado el diagnóstico seguimos haciendo determinaciones periódicas de fosfatasa alcalina para monitorizar la actividad de la enfermedad dado que la correlación es directa.
Como seguro habrás imaginado el tratamiento a realizar para normalizar el aumento de la fosfatasa alcalina debe ser el de la causa que origine dicho aumento (sea ósea, hepática u otra).
Por curiosidad, no lo hemos comentado antes, pero tienes que saber que también pueden observarse niveles disminuidos de fosfatasa alcalina en la analítica. En este caso pueden aparecer, por ejemplo, después de una transfusión sanguínea o de un by-pass cardíaco o por un déficit proteico. ¡Ahora ya sabemos interpretar una parte de la analítica sanguínea!
¿Tienes dudas? Regístrate ahora en Savia y habla gratis con nuestros especialistas médicos por chat o videoconsulta.

Artículo especializado
Utilidad de los Test Genéticos
El test genético es una prueba médica que ayuda a conocer si hay una mutación determinada en el ADN (organizado en forma de genes) de un individuo, la identifica y determina si ésta se asocia a una enfermedad concreta.
Cada individuo tiene un conjunto de genes, con una función determinada. La alteración de algunos de estos genes (mutación) puede aumentar la susceptibilidad de padecer una enfermedad, de presentarla o de que ésta sea de mayor o menor gravedad.
El estudio genético indica si la persona, una vez identificada la mutación, es portadora o no. Esto significa si ha heredado la alteración que le hace tener un mayor riesgo de sufrir una enfermedad. El hecho de ser portador no quiere decir que vaya a desarrollarla necesariamente sino que existe una mayor predisposición que en el resto de la población.
El procedimiento para el paciente es muy sencillo ya que se hace generalmente con una simple analítica en sangre, otras veces con muestras de células de piel o saliva. Lo que se estudia en el laboratorio es el ADN del individuo y si existen las alteraciones genéticas (genes específicos) descritas y asociadas con enfermedades hereditarias.
¿Cómo se interpreta?
Aunque la realización de la prueba es sencilla, su interpretación, por el contrario, es complicada y precisa ser hecha por un especialista, quien además debe tener otros datos como la historia médica y familiar del paciente.
El objetivo del test genético es establecer un plan preventivo para disminuir el riesgo de que el paciente desarrolle la enfermedad, por ejemplo, un cáncer de ovario. Para ello es fundamental tener otros datos que nos ofrezcan una imagen global de la situación de la persona estudiada. Es decir, por sí sola la información genética puede no ser concluyente. Entre otros factores, hay enfermedades de causa multifactorial (además de la genética intervienen otros actores) y de herencia poligénica (intervienen varios genes) lo cual hace que sea necesaria la valoración cuidadosa de cada caso y del riesgo del paciente antes de tomar medidas específicas de tratamiento.
Aclarando conceptos
Existe gran confusión en este campo, y por ello proliferan empresas en Internet que hacen de forma económica un test genético, con el problema de que la interpretación no la realiza un especialista y pueden crear situaciones erróneas y confusas al solicitante. En Europa están prohibidos los diagnósticos genéticos directos al consumidor. Según la Ley de Investigación Biomédica “el diagnóstico genético requiere un proceso de consejo genético previo y posterior”. En otras palabras , es el médico quien recomienda o indica el test genético tras el estudio en consulta del paciente con el asesoramiento pertinente.
Actualmente, los hospitales universitarios de un gran número de ciudades españolas disponen de las llamadas Unidades de Consejo Genético , cuya función es el asesoramiento, la valoración y la indicación de pruebas genéticas en aquellos casos que lo consideren pertinente.
¿En qué áreas se aplica?
Los tests genéticos se indica sobre todo en:
Estudio diagnóstico de enfermedades de clara causa genética y hereditarias como la fibrosis quística.
Prevención y detección precoz en oncología, para descartar cánceres con un componente genético claro como el cáncer de ovario o el de mama.
En recién nacidos, para la determinación precoz de un panel de enfermedades genéticas.
En familiares de pacientes diagnosticadas de enfermedades hereditarias, por ejemplo, la miocardiopatía hipertrófica o la paraparesia espástica familiar.
Test genéticos y oncología
Uno de los avances más interesantes en los últimos años en el área de la oncología ha sido el estudio de la genética y su asociación con determinados tipos de tumores.
El conocimiento de los paneles genéticos (genes mutuados y el cáncer con el que se asocia) permite desarrollar diferentes estrategias, especialmente para la prevención y desarrollo de este tipo de tumor en los pacientes que sean portadores de esa mutación determinada.
Por ejemplo, en mujeres con una mutación determinada que se ha demostrado que aumenta el riesgo de cáncer de ovario, la realización de una ooforectomía (quitar los ovarios) lo elimina completamente.
Por tanto, la realización de test genéticos en cánceres hereditarios se ha ido incorporando a la práctica médica habitual.
¿Cuándo se realiza?
Se sospecha que puede haber un cáncer hereditario en aquellas con antecedentes médicos personales o familiares especiales. Entre ellos se incluyen: la presencia de varios casos de cáncer en la familia y/o si han aparecido a edades tempranas; haber presentado varios tipos de cáncer el mismo paciente, ser de un determinado grupo étnico que tienen mayor susceptibilidad, etc.
¿Qué tipos de cáncer son los más frecuentemente hereditarios?
Cáncer de mama hereditario: implicados los genes BRCA1 y BRCA2.
Cáncer de colon: gen APC.
Cáncer de piel (melanoma maligno).
Cáncer de ovario: genes BRCA1, BRCA2.
Cáncer medular de tiroides: gen RET.
Otros tipos de cáncer más raros: feocromocitoma-paraganglioma (genes, SDHC, SDHB, SDHA y SDHAF2), neoplasia endocrina múltiple (Gen MEN1), retinoblastoma (gen RB1).
Las acciones que se pueden llevar a cabo de carácter preventivo se han de individualizar en cada caso, pero en líneas generales incluirán cirugía (mastectomía profiláctica, por ejemplo), quimioterapia (fármacos para reducir el riesgo) y diagnóstico precoz (pruebas de detección tempranas, por ejemplo colonoscopia en cáncer de colon).

Artículo especializado
Funciones y Deficiencia de la Vitamina B12
La vitamina B 12 (cobalamina) es una vitamina hidrosoluble del grupo B, que r esulta básica para el funcionamiento normal del cerebro, del sistema nervioso, y también para la formación de la sangre y de varias proteínas . Además, contribuye a la elaboración del ADN, el material genético presente en todas las células; y también en la metabolización de los aminoácidos, de los ácidos grasos y de los glúcidos. También previene un tipo de anemia, denominada anemia megaloblástica, que provoca cansancio y debilidad en las personas.
Propensa a la deficiencia
No es infrecuente que se produzca deficiencia de vitamina B12 pues su fisiología humana es compleja . Esta vitamina debe ser liberada de la unión a las proteínas por la acción de las peptidasas digestivas (enzimas), tanto en el estómago como en el intestino delgado. El ácido gástrico libera la vitamina de las partículas de alimentos; por lo tanto, los antiácidos y los medicamentos que bloquean los ácidos, pueden inhibir la absorción esta vitamina. La posibilidad de sufrir de hipovitaminosis B 12 aumenta con la edad, ya que algunas personas producen menos ácidos estomacales a medida que envejecen.
¿Qué funciones cumple la vitamina B 12 ?
La vitamina B 12 es imprescindible para la salud por varios motivos :
Aumenta la energía y reduce la fatiga y el cansancio.
Favorece la digestión, la asimilación del hierro y de los hidratos de carbono consumidos con la alimentación y la metabolización correcta de las grasas.
Asegura un buen funcionamiento del sistema nervioso.
Ayuda a la producción de los glóbulos rojos en la sangre.
Regula la división celular y favorece la longevidad.
Protege el corazón y el sistema circulatorio de la homocisteína.
Está implicada en la producción de la hormona suprarrenal.
Favorece un sistema inmunológico saludable.
Favorece la reproducción femenina y un embarazo saludable.
Favorece la serenidad mental y regula el estado de ánimo.
Fomenta la claridad mental, la concentración y la memoria.
Aumenta la energía física, emocional y mental.
¿Qué causa el déficit de vitamina B 12 ?
No suele tener un origen dietético (salvo en personas veganas/vegetarianas), es decir, rara vez se debe a una ingesta deficiente por parte de la persona. Las causas más comunes son:
Problemas de absorción : para su correcta asimilación por el organismo la vitamina B 12 necesita una proteína que se segrega en el estómago llamada factor intrínseco. Cuando por algún motivo no se produce, o su secreción es deficiente, la vitamina B 12 no se asimila. Esta falta de factor intrínseco puede deberse a anomalías puntuales, a un defecto congénito o a una cirugía donde se ha reseccionado una parte del estómago. También hay otras patologías (donde no interviene el factor intrínseco) que dificultan la correcta absorción de vitamina B 12 , como la celiaquía, la enfermedad de Crohn, problemas pancreáticos, parásitos intestinales, etc.
Interacciones : diversos fármacos pueden dificultar la acción de la vitamina B 12 , así como también algunos tratamientos como la quimioterapia, y el crecimiento de bacterias anormales en la flora intestinal.
Otras patologías : hipotiroidismo y otros trastornos endocrinos, alcoholismo, enfermedades hepáticas, cáncer, etc.
¿Qué ocurre si no consumo o absorbo suficiente vitamina B 12 ?
Algunos de los síntomas de la deficiencia de vitamina B 12 son cansancio, debilidad, constipación, pérdida del apetito, pérdida de peso y anemia megaloblástica . También es posible que se manifiesten problemas neurológicos , como entumecimiento y hormigueo en las manos y los pies. Otros síntomas de la deficiencia de vitamina B 12 incluyen problemas de equilibrio, depresión, confusión, demencia y pérdida de memoria. La deficiencia de vitamina B 12 puede causar daños en el sistema nervioso, incluso en personas que no padecen anemia. Por este motivo, es importante tratar una deficiencia lo antes posible.
En el caso de los bebés, si hay deficiencia de vitamina B 12 se manifiesta con retraso del crecimiento, problemas del movimiento, retrasos en alcanzar los hitos típicos del desarrollo, y anemia megaloblástica.
Altas concentraciones de ácido fólico (vitamina B 9 ) pueden ocultar una deficiencia de vitamina B 12 al corregir la anemia megaloblástica, un signo característico de la deficiencia de vitamina B 12 . Sin embargo, el ácido fólico no corrige el daño progresivo al sistema nervioso que también causa la deficiencia de vitamina B 12 . Por esta razón, los adultos sanos no deben consumir más de 1,000 mcg de ácido fólico por día.
¿Qué alimentos son fuente de vitamina B 12 ?
La vitamina B12 la encontramos de forma natural en muchos alimentos de origen animal y en algunos que la añaden (alimentos fortificados con vitamina B 12) . Se pueden obtener las cantidades recomendadas (entre 2-3 mcg/día), con una dieta que incluye alimentos variados como :
Hígado vacuno, almejas, ostras y mejillones son las mejores fuentes de vitamina B 12 .
Pescado, carne, carne de ave, huevos, leche y otros productos lácteos.
Ciertos cereales para el desayuno, levaduras nutricionales y otros productos alimenticios fortificados con vitamina B 12 . Es mejor leer la etiqueta del producto para saber si a un alimento se le ha añadido dicha vitamina.
Las pocas verduras que son fuentes de esta vitamina, en realidad son análogos, es decir, bloquean la absorción de la vitamina B 12 , aumentando, incluso, la necesidad del cuerpo de este nutriente.
¿Qué suplemento dietético de vitamina B 12 se recomienda?
Si no se consume suficiente vitamina B 12 a través de los alimentos o se sospecha que el organismo no es capaz de absorberla, se recomienda empezar de inmediato a tomar un suplemento dietético de esta vitamina.
Existen suplementos diarios de 25-100 mcg al día, suplementos de 1000 mcg que se pueden tomar dos veces por semana o suplementos de 2000 mcg que se toman uno por semana. La forma química de suplementación de vitamina B 12 se aconseja que sea a través de cianocobalamina, porque es la forma más estudiada, la presentación a mejor precio y que resulta más fácil de encontrar y la forma química más estable y resistente tanto a la temperatura, como a la luz y los cambios de pH.

Artículo especializado
Funciones y Deficiencias de la Vitamina D
La vitamina D, también denominada calciferol, es un nutriente que encontramos en la porción grasa de ciertos alimentos y juega un papel fundamental en la salud ósea. Sólo obtenemos un 10% de esta vitamina a través de los alimentos que ingerimos y la mayor parte, el 90%, se sintetiza en la piel, a través del contacto con los rayos ultravioletas del sol, por este motivo se la conoce como vitamina solar .
Resulta paradójico que el 50% de la población española tenga déficit de esta vitamina siendo un país con buen clima y soleado. Más adelante, detallamos los motivos que pueden conducir a este déficit y las medidas o precauciones para evitarlo.
Una vitamina especial
La vitamina D es especial y diferente a las demás vitaminas porque tanto cumple con una función reguladora como hormonal . Existen dos formas:
Vitamina D3 , también conocida como colecalciferol, aparece en productos animales, se encuentra en el tejido adiposo o graso y es difícil de incorporar a través de la dieta porque hay pocos alimentos que la contengan de forma natural (pescados grasos, como atún, caballa, salmón; lácteos enteros, como leche, yogur, queso, mantequilla, crema de leche, nata; yema de huevo y el hígado). Esta vitamina también la obtenemos a través de la piel mediante la exposición a la radiación solar y es la forma más habitual de incorporarla al organismo.
Vitamina D2 , también conocida como ergocalciferol, se obtiene de forma artificial en los vegetales y se utiliza para enriquecer alimentos y así asegurar la ingesta adecuada diaria.
Funciones de esta vitamina
Estas dos formas de vitaminas (D3, D2), que pasan por el hígado y finalmente en el riñón se transforman en una molécula biológicamente activa con acción hormonal. Estas formas activas favorecen la absorción de calcio en el intestino y en el riñón estimulan su reabsorción, por lo que participan y son indispensables para la formación y mineralización ósea . Sin embargo, a la vitamina D se le atribuyen más funciones porque se han descubierto receptores de esta vitamina en otros tejidos y células (músculo, corazón, cerebro, vasos sanguíneos, mama, colón, próstata, páncreas, sistema inmune y piel). Se sabe que interviene en el sistema nervioso favoreciendo que el impulso eléctrico llegue a los músculos, fortalece el sistema inmune ayudando a prevenir la aparición de infecciones y enfermedades, favorece el control de la presión arterial y también interviene en la secreción de la hormona insulina estimulando su producción en el páncreas y ayudando a las células a no desarrollar una intolerancia, disminuyendo así la posibilidad de crear resistencia y padecer diabetes con el paso de los años. También se ha descubierto que existe una relación directa entre la vitamina D y la producción de serotonina favoreciendo el sentirse de mejor humor y disminuyendo la sensación de cansancio.
Incluso en los últimos años existen estudios que le otorgan un papel protector frente a algunas enfermedades como artritis reumatoide, esclerosis múltiple y cáncer de colon.
Por qué tenemos falta o déficit de vitamina D
El déficit puede aparecer porque no hay un consumo suficiente de vitamina D a través de la dieta, no se absorbe suficiente vitamina D de los alimentos por un problema de malabsorción, existe alguna enfermedad renal o hepática que impide convertir la vitamina D en su forma activa o por la toma de medicamentos que limita la absorción de esta vitamina. También hay que tener en cuenta que, con la edad, de forma natural, la piel pierde su capacidad para producir esta vitamina y las personas con piel de coloración oscura tienen menos capacidad de síntesis de vitamina D. También se sabe que la obesidad obstaculiza el paso de la vitamina D a la sangre ya que cierta cantidad de esta vitamina se adhiere a la grasa por ser una vitamina liposoluble (soluble en grasa)
Aun así, la causa más común que provoca el déficit de esta vitamina es por la falta de exposición solar asociado al uso de cremas solares de alta protección que actúan como pantalla solar, para prevenir la aparición del cáncer de piel. Nos hemos habituado a vivir y trabajar en espacios interiores donde, aunque haya luz, no filtra los rayos solares.
Recomendaciones específicas para evitar la deficiencia
Es importante tener en cuenta los alimentos ricos en vitamina D, ya que son pocos y deberemos escoger adecuadamente
Se encuentra en: aceite de hígado de pescado, pescado azul, huevos, mantequilla, nata, queso, leche enriquecida y, curiosamente, champiñones expuestos a radiación ultravioleta.
También están en alimentos enriquecidos con vitamina D como bebidas de soja o de arroz, zumos o cereales.
El aceite de hígado de pescado y los pescados grasos o azules que se alimentan de plancton que absorben mucha luz solar (arenque, salmón, sardina, caballa, atún…) son las fuentes alimentarias más ricas en vitamina D.
La leche humana y la leche de vaca no enriquecida tienden a ser fuentes pobres de vitamina D. Sin embargo, la leche continúa siendo el alimento de elección para el enriquecimiento de la vitamina D debido a su contenido en calcio.
La vitamina D es muy estable y no se deteriora cuando los alimentos se calientan o se almacenan durante períodos prolongados.
La vitamina D también la sintetiza el organismo a través del contacto de la piel con los rayos solares, por ello se recomienda pasear entre 10-15 minutos al día en horas de sol para sintetizar dicha vitamina. Es suficiente con exponer la cara y los brazos, lógicamente evitando horas de máxima radiación solar en verano (de 11-16h)
Cuando no se expone la piel al sol y no se logra consumir suficientes alimentos enriquecidos o fuentes naturales de vitamina D, otra opción es tomar suplementos de vitamina D. Esta elección siempre debe estar supervisada por un médico y llevar un control.
¿Qué signos o síntomas aparecen cuando hay una deficiencia de vitamina D?
Si la deficiencia es leve no suele producir síntomas o signos. Si la carencia es más grave se produce una pérdida de la densidad ósea favoreciendo el riesgo de sufrir osteoporosis y fracturas. En niños esta situación puede causar raquitismo haciendo que los huesos sean más blandos y se doblen. En adultos, los casos de deficiencia severa pueden conducir a la osteomalacia, que cursa con huesos débiles, dolor y debilidad muscular.
¿Existe la toxicidad por hipervitaminosis?
Debemos tener la precaución de no excedernos con la ingesta de vitamina D ya que se almacena en el organismo y si las concentraciones en sangre son demasiado elevadas puede dar signos de toxicidad como náuseas, vómitos, pérdida de apetito, debilidad y pérdida de peso. Además, la hipervitaminosis D también conlleva unos niveles elevados de calcio en sangre que puede causar confusión, desorientación, problemas en el ritmo cardíaco e incluso provocar daños en los riñones. Sin embargo, llegar a una concentración de vitamina D que se considere perjudicial sólo se puede lograr tomando suplementos, nunca con una exposición excesiva al sol, ya que en caso de haber demasiada vitamina D en sangre, el cuerpo limita su producción.

Artículo especializado
Qué Debes Saber sobre el Sida
Hoy en día, gracias a los avances en la medicación, la mayoría de personas infectadas por el VIH (virus de inmunodeficiencia humana) no llegan a desarrollar el sida. El sida no es sinónimo de infección por el VIH sin más, sino que solamente hace referencia al estadio final de la infección por este virus.
Cómo se contrae
El VIH o virus de la inmunodeficiencia humana es un virus de la familia de los retrovirus. Se conocen solamente dos variedades de este virus, el VIH-I, que es el más habitual, y el VIH-II, que solamente se ha descrito en África. El VIH se puede contraer por diversas vías:
Transmisión sexual: es actualmente la principal vía de transmisión actual y se puede dar tanto en Relaciones heterosexuales como homosexuales.
Transmisión sanguínea : por el uso de jeringuillas compartidas en personas adictas a drogas intravenosas, pinchazos con material quirúrgico o médico con sangre de una persona portadora del VIH.
Transmisión materno-fetal o vertical : el VIH se puede trasmitir de la mujer infectada al feto durante el embarazo o en el momento del parto; asimismo, también se puede transmitir mediante la lactancia.
Cómo actúa
El VIH ataca a un tipo concreto de células de defensa , los linfocitos CD4, y es esta afectación del sistema inmunitario lo que conlleva las infecciones secundarias graves y potencialmente mortales o los tumores malignos que pueden desarrollarse cuando el sistema inmunitario es muy deficitario.
Cómo se desarrolla
La infección por el VIH se desarrolla en general a lo largo de tres fases:
Infección aguda o primoinfección.
Fase asintomática.
Enfermedad avanzada o sida.
Habitualmente la infección aguda no mata a la persona que se infecta, sino que el virus permanece aletargado en el organismo y se convierte en una infección crónica que puede permanecer en este estado, sin causar síntomas, durante años hasta que, sin un tratamiento adecuado, el sistema inmunitario comienza a fallar y surgen las complicaciones de la fase de sida.
En la infección aguda no se dan apenas síntomas, a lo sumo los propios de cualquier infección viral inespecífica como pueden ser fiebre, malestar general, cansancio, inflamación de los ganglios o una leve afectación hepática.
En la fase avanzada de la enfermedad, la llamada propiamente sida , la persona tiene los síntomas propios de infecciones oportunistas (infecciones poco frecuentes que solamente se dan en personas con un sistema inmunitario comprometido) o bien de otras enfermedades causadas directamente por el virus. Los síntomas que causan estas infecciones varían mucho en función de los microorganismos que las causan y de los órganos que se ven afectados. Algunas de estas infecciones oportunistas y enfermedades que definen la fase de sida son:
Tuberculosis pulmonar o diseminada.
Candidiasis en las mucosas —oral, esofágica, genital— o diseminada.
Meningitis por parásitos, como el criptococo.
Diarreas por infección del tubo digestivo por Cryptosporidium.
Infecciones oculares como la queratitis por citomegalovirus.
Infecciones cerebrales como la toxoplasmosis cerebral.
Tumores característicos del sida, como son el sarcoma de Kaposi o los linfomas cerebrales.
Cómo se diagnostica
El diagnóstico de la infección por el VIH se realiza de manera rápida y fiable mediante un análisis de sangre . Se realiza una serología, es decir, se busca la presencia de anticuerpos contras el VIH. Si el resultado es positivo implica que la persona presenta una infección por el VIH, que no es lo mismo, insistimos, que padecer la fase de sida. El diagnóstico de sida se establece cuando existe una serología positiva confirmada y alguna de las infecciones oportunistas o de los tumores que definen esta fase. Toda serología positiva se confirma siempre mediante un segundo análisis. Hoy en día existen kits de detección rápida de los anticuerpos del VIH que permiten, con una gota de sangre obtenida mediante un pinchazo en el dedo, detectar la presencia de anticuerpos del VIH en unos 20 minutos.
Las serologías pueden ser negativas y, sin embargo, haber infección, sobre todo si el contagio puede haber sido reciente. Existe un periodo de latencia, llamado periodo ventana, que dura de tres a 12 semanas y durante el cual no se detectan anticuerpos del VIH. En casos de una sospecha de infección se puede intentar determinar la presencia de un antígeno —una molécula específica del virus a la que se unen los anticuerpos— del VIH llamado p24, que en caso de infección será positivo, aunque todavía no haya suficientes anticuerpos como para detectarlos en la serología.
Tratamiento
Una vez se ha diagnosticado la infección por VIH es esencial evaluar con un análisis completo de sangre el estado inmunitario de la persona , así como la carga viral, es decir, la cantidad de virus que se detectan en sangre. Estos valores son los que tomaremos como referencia para valorar el éxito de los tratamientos antirretrovirales.
Los grupos de fármacos para el tratamiento del VIH han evolucionado enormemente . Mientras que los primeros fármacos causaban muchos efectos secundarios bastante intolerables y se precisaba tomar un gran número de pastillas diarias, hoy en día el tratamiento ha mejorado sustancialmente, con una menor cantidad de medicamentos diarios y una mejor seguridad de estos fármacos. Uno de los principales avances en el tratamiento han sido los resultados del estudio START, que demostró que cuanto antes se dé tratamiento antirretroviral a los pacientes mayor tiempo se mantienen estos sanos y ganan una mayor esperanza de vida.
¿Vacuna?
Asimismo, se e stá pendiente de los resultados de una vacuna terapéutica que se ha comenzado a probar en 2016. No se trata de una vacuna preventiva en sentido estricto, ya que se aplica a personas ya infectadas y no busca prevenir la enfermedad, sino que el sistema inmune reproduzca la respuesta al virus que tienen personas que controlan la enfermedad por sí mismas sin necesidad de medicación, personas cuyo propio sistema inmune mantiene a raya la infección por el VIH.
Medidas de prevención
La prevención del contagio por el VIH pasa por tomar medidas de protección al mantener relaciones sexuales. El preservativo sigue siendo el método más eficaz de prevención tanto para hombres como mujeres. En caso de ser adicto a drogas intravenosas no se deben compartir nunca las jeringuillas. La transmisión vertical se puede prevenir con el tratamiento con antirretrovirales durante el embarazo, el parto y la lactancia.
Conviene mencionar la aparición de la PrEP o profilaxis preexposición como herramienta de prevención del VIH. En 2012 se aprobó en Estados Unidos el uso de la toma de fármacos antirretrovirales como mecanismo preventivo del contagio del VIH después de que algunos estudios demostraran su seguridad y eficacia. Desde entonces, este uso de los fármacos antirretrovirales como medida preventiva se ha aprobado en otros países, permitiendo el acceso a dicha medicación a las personas con más riesgo de infectarse. En España el uso de esta medicación todavía no está aprobado.
Ante la sospecha de un posible contagio es esencial hacerse la prueba de detección del VIH y en caso de ser positiva ponernos en contacto con un servicio de enfermedades infecciosas.

Artículo especializado
Control del Ácido Úrico
¿En una analítica te ha salido el ácido úrico elevado y te han aconsejado controlar tu alimentación? Te explicamos cuáles pueden ser los motivos y cuáles son los alimentos cuyo consumo sería aconsejable moderar .
¿Qué es el ácido úrico?
El ácido úrico es una sustancia química orgánica que se produce en el organismo humano como producto metabólico final de la degradación de las purinas, eliminándose por la orina (70% del total) y a través del intestino (30% restante). Las purinas son unas moléculas que forman parte de la estructura del material genético (ADN/ARN) presente en las células de nuestro cuerpo y en los alimentos que ingerimos.
Por tanto, el ácido úrico puede estar alto debido a factores endógenos (el propio cuerpo lo fabrica a nivel de hígado, músculos, intestinos, riñones…) o factores exógenos (a través de la alimentación).
La hiperuricemia
De una forma general, el rango de valor normal en sangre es 1-7g/dL. La hiperuricemia es el aumento de ácido úrico o urato en sangre por encima de este valor, y puede producirse por:
Aumento de la producción de ácido úrico : por enfermedades genéticas, por causa desconocida o idiopática, por dieta rica en alimentos que contienen abundantes purinas, por casos de leucemia, mieloma múltiple, psoriasis extensas, anemias hemolíticas o tratamiento quimioterápico de tumores malignos, así como, también, por consumo excesivo de alcohol…
Disminución de su excreción (eliminación) renal: más frecuente, por existencia de enfermedades tipo insuficiencia renal, diabetes insípida, hipotiroidismo…
ALIMENTOS RICOS EN PURINAS
Contenido muy alto : vísceras, patés, embutidos, pescado azul, marisco…
Contenido alto: carnes rojas y de caza, habas, lentejas.
Contenido moderado contenido : carnes blancas, legumbres no nombradas anteriormente (garbanzos, judías blancas…), coliflor, espárragos, espinacas y setas.
Contenido bajo: lácteos, el resto de verduras no nombradas anteriormente, tubérculos, raíces, fruta…
¿SABÍAS QUE…?
El consumo excesivo de alcohol produce , de hecho, un aumento de ácido úrico en sangre por ambos mecanismos, ya que por su culpa no sólo aumenta la producción del mismo, sino que disminuye también su eliminación por el riñón.
Síntomas, diagnóstico y tratamiento de la hiperuricemia
La hiperuricemia generalmente es asintomática , pero cuando el ácido úrico se deposita en los tejidos aparece la gota.
En caso de hallar niveles elevados de ácido úrico en sangre, hay que intentar descubrir su causa y para ello es necesario determinar el ácido úrico en orina para saber si es por sobreproducción o por defecto de excreción.
Comprend e tres vías de actuación :
Modificación de la dieta: cabe destacar que este apartado no tiene un papel fundamental porque es necesaria una dieta muy pobre en purinas para conseguir descensos moderados de los niveles de ácido úrico. La restricción estricta de las purinas de la dieta puede descender tan sólo unos pocos milígramos los niveles de ácido úrico. No obstante, el control de la dieta, el consejo de reducción de peso en pacientes obesos, el consejo de ingerir abundantes líquidos a lo largo del día y el consejo de no ingerir bebidas alcohólicas formarán parte del tratamiento siempre.
Práctica de ejercicio físico regular.
Fármacos: bien mediante medicamentos que inhiben la producción de ácido úrico endógeno (por ejemplo, alopurinol – Zyloric ®), o bien medicamentos que aumentan su eliminación por la orina (probenecid, sulfinpirazona…).
La gota
La gota es la enfermedad debida a la deposición de cristales de las sales de ácido úrico en y alrededor de las articulaciones (gota articular), en diversos órganos (gota visceral) y, finalmente, estos cristales también pueden formar cálculos en las vías urinarias (litiasis úrica).
La gota afecta al 1-2% de la población general en algún momento de la vida, en mayor medida a hombres que a mujeres (8:1) y principalmente en edades medias de la vida (después de los 30 años).
Factores de riesgo de la gota
Hiperuricemia crónica : es el factor de riesgo más importante en el padecimiento de gota. Ahora bien, no todos los pacientes con hiperuricemia padecerán gota, sólo la padecerá un pequeño porcentaje (uno de cada cinco). Incluso, en algunas ocasiones, existen episodios de gota con niveles de ácido úrico en sangre normal.
Edad : el riesgo de padecerla aumenta con la edad.
Determinados estilos de vida y dietas poco saludables (obesidad, alcoholismo…): es frecuente que las personas que padecen gota sean obesas y tengan, además, diabetes y/o hipertensión arterial. La gota es más común en sociedades opulentas, debido a una dieta rica en proteínas, grasas y alcohol.
Signos y síntomas de la gota
Gota articular :
En la crisis de gota aguda típica, que suele comenzar por la noche, el síntoma primordial es el dolor, que puede presentarse de forma aguda e intensa, junto con inflamación (enrojecimiento e hinchazón) de la articulación. Es una artritis por depósito de microcristales. Las articulaciones habitualmente afectadas son: la articulación metatarso-falángica del dedo gordo del pie (y en este caso recibe el nombre de podagra), las rodillas, los tobillos, hombros o el empeine de los pies, entre otras localizaciones.
En la gota crónica, después de una larga evolución de la enfermedad, se producen los denominados “tofos gotosos”, que son unos nódulos indoloros situados debajo de la piel, que se forman por depósito lento de ácido úrico en los mismos, por lo que van aumentando de tamaño progresivamente. Tienden a desaparecer poco a poco cuando la enfermedad está bien controlada.
Gota visceral:
Nefropatía aguda úrica: por obstrucción de los túbulos del riñón por culpa de los cristales de ácido úrico, provocando una intensa inflamación y, secundariamente, insuficiencia renal aguda.
Litiasis (piedras en el riñón):
La litiasis úrica consiste en la formación de cálculos de ácido úrico, que pueden obstruir las vías urinaria, provocando intenso dolor (cólico nefrítico). Sólo suponen el 5-10% del total de cálculos renales.
Diagnóstico y tratamiento
Se diagnostica por la clínica típica. En algunas ocasiones será necesario el análisis del líquido sinovial (líquido intraarticular), obtenido por punción de la articulación, para analizarlo y diferenciar la artritis gotosa de otros tipos de artritis, como puede ser la infecciosa, por ejemplo. En cuanto al tratamiento:
Fármacos antiinflamatorios no esteroideos (AINE): son los medicamentos más usados para el tratamiento de la crisis de gota aguda. También son analgésicos (calman el dolor).
Fármaco Colchicina : también usado frecuentemente en la crisis aguda, pero presenta efectos secundarios molestos como, por ejemplo, diarrea.
El mismo tratamiento anteriormente mencionado para la hiperuricemia (dieta, control de peso, abstinencia en el consumo de alcohol, alopurinol, diuréticos…).
Contenidos sobre enfermedades
Somos conscientes de que los conceptos médicos pueden resultar confusos si no te los explican con claridad. Para evitar esto, le hemos pedido a nuestros profesionales que preparen estas fichas en donde podrás acceder a información relevante sobre enfermedades que te ayudará a entender de una manera sencilla por qué se producen y por qué es necesario su tratamiento.
Ver todas las enfemedades 
Enfermedad
Hipoglucemia
¿Qué es la hipoglucemia?
La hipoglucemia es una bajada de la cantidad de azúcar en la sangre por debajo de 60 mg/ml. En los recién nacidos son más frecuentes en los niños pretérmino, llegando a ser hasta del 14% de los casos. En los niños a término suele darse como mucho en un 7%. Las hipoglucemias en los diabéticos son más frecuentes en pacientes con insulina o secretagogos que con otros tratamientos hipoglucemiantes. Es una situación urgente de revertir ya que es grave porque puede poner en peligro la vida del individuo.
Causas de la hipoglucemia
La causa principal de la hipoglucemia es la alteración hormonal a nivel de hipófisis y tiroides . También se puede producir en pacientes normales sin alteraciones hormonales por causa de falta de alimento, exceso de ejercicio , o descarga insulínica en el páncreas.
Síntomas de la hipoglucemia
Los síntomas son: malestar, cansancio, adormecimiento, temblor, sudoración profusa, palpitaciones, mareos, visión borrosa, dolor de cabeza, convulsiones y trastorno del comportamiento.
Tratamiento para la hipoglucemia
El tratamiento para la hipoglucemia es dar azúcar de forma rápida. Se puede dar un producto azucarado como pueden ser los zumos de frutas , o también se puede dar directamente un sobre de azúcar disuelto en un vaso de agua. En casos muy difíciles de revertir y en pacientes diabéticos, puede ser necesario darles Glucagón mediante inyección subcutánea.
Pruebas complementarias del tratamiento de la hipoglucemia
La prueba complementaria será la determinación de glucosa en sangre capilar, hasta normalización de la misma, cada media hora.
Factores desencadenantes de la hipoglucemia
Los factores desencadenantes de la hipoglucemia son la falta de aporte de hidratos de carbono en la dieta , o el exceso de insulina en la sangre.
Factores de riesgo de la hipoglucemia
Son factores de riesgo para sufrir hipoglucemia en los pacientes en tratamiento con insulina y con secretagogos como Repaglinida y Glibenclamida . Los largos periodos de ayuno sin ingesta de hidratos de carbono , el periodo neonatal en niños pretérmino que tienen más problemas en regular hormonalmente sus niveles de glucemia, y también en niños a término en especial si son hijos de madres diabéticas.
Complicaciones de la hipoglucemia
Daños neurológicos.
Convulsiones.
Pérdida de conocimiento.
Coma.
Prevención de la hipoglucemia
No realizar ejercicio en ayunas.
Ingesta adecuada de hidratos de carbono.
Control capilar de glucemia.
Especialidades a las que pertenece la hipoglucemia
En el caso de hipoglucemias neonatales se trata de control con pediatras neonatólogos, en el resto de casos, se controla por el endocrino.
Preguntas frecuentes:
¿Qué es la hipoglucemia en bebés?
La hipoglucemia en bebés es la bajada de azúcar que se puede producir en los recién nacidos, más frecuente en niños prematuros, en niños nacidos a término que presentan madres diabéticas en el embarazo, y en niños con retraso en el crecimiento intrauterino.
¿Qué puede ocasionar la hipoglucemia?
Las hipoglucemias se producen por el exceso de insulina o por la falta de hidratos de carbono. En personas con tratamiento con insulina o fármacos secretagogos (fármacos que producen la secreción de insulina), se pueden producir hipoglucemias. En los neonatos que no tienen aún una buena regulación hormonal también se produce por parte del organismo un exceso de insulina que es la que causa la hipoglucemia. Las personas que tienen largos periodos de ayuno pueden presentar una hipoglucemia por falta de ingesta.
¿Qué diferencia hay entre hiperglucemia e hipoglucemia?
Las hiperglucemias son valores por encima de lo normal de azúcar en sangre (son niveles normales entre 70 y 129 mg/dl). La hipoglucemia son valores por debajo de lo normal de azúcar en sangre . Para tener síntomas de hipoglucemia, la glucosa deberá de estar por debajo de 60 mg/dl.
¿Cuáles son los niveles normales de azúcar en sangre?
Los niveles normales de azúcar en sangre son diferentes antes y después de la ingesta, así, en ayunas se consideran normales niveles de entre 70 y 128 mg/ml, por encima de estas cifras se habla de hiperglucemia, cuando se ha consumido alimento se considera que a las dos horas de haberlo ingerido los niveles de azúcar deben estar por debajo de 140 mg/ml
¿Qué es la hipoglucemia reactiva?
La hipoglucemia reactiva o hipoglucemia postprandial es la que se produce unas cuatro horas después de comer y no necesita un tratamiento especial, salvo el regular la ingesta de alimentos. Suele ser suficiente con no comer alimentos azucarados con el estómago vacío y hacer cinco comidas al dia.

Enfermedad
Síncope Vasovagal
¿Qué es el síncope vasovagal?
El síncope vasovagal o lipotimia, es la pérdida de conocimiento que se produce por estímulo del nervio vagal , dando lugar a un enlentecimiento del ritmo cardíaco y una bajada de la tensión arterial . La presencia de síncope varía entre el 10% y 20% de la población, siendo más frecuente en pacientes ancianos y en mujeres . Ante un síncope siempre se debe acudir a ser valorado por un médico, ya que también puede tratarse de un síncope cardiogénico . Es una enfermedad leve.
Tipos de síncopes
Síncope vasovagal : se produce una bajada de la frecuencia cardíaca y de presión arterial por el estímulo vagal .
Síncope cardíaco : se produce por la estimulación de la carótida . Por presión en la misma se produce una disminución de la frecuencia cardíaca.
Síncope ortostático : se produce por la disminución de la presión arterial al ponerse de pie tras estar sentado o tumbado. Es muy frecuente en personas mayores que reciben medicación hipotensora .
Síncope cardíaco : se debe a problemas cardíacos . En general se dan bloqueo cardíaco y alteraciones en el ritmo, ya sean bradicardias y taquicardias. También puede producirse por alteraciones en la válvula aórtica o por hipertrofias ventriculares importantes.
Causas del síncope vasovagal
La causa del síncope vasovagal puede ser:
Por estrés laboral .
Estrés emocional .
Por una impresión desagradable , por ejemplo, el que se produce al ver sangre.
Por estar en un ambiente muy cálido .
Por estar mucho tiempo de pie. En estas circunstancias se produce una vasodilatación que da lugar al síncope.
El embarazo .
Dolores fuertes .
Síntomas del síncope vasovagal
El síntoma del síncope vasovagal es la pérdida de conciencia que se produce, pero previo a ello el paciente puede notar sensación de debilidad, sofocos, vértigo, visión borrosa, palidez, sudoración profusa y zumbido de oídos. Puede presentar también náuseas, vómitos y diarrea.
Tratamiento para el síncope vasovagal
El síncope vasovagal no tiene tratamiento , se deberá indicar al paciente que permanezca en posición tumbado con los pies elevados. Posteriormente se le sentará y solo cuando esté totalmente recuperado deberá proceder a ponerse en pie. Se deberá beber líquido abundante para evitar la deshidratación, que favorece el episodio.
Pruebas complementarias del tratamiento de síncope vasovagal
Las pruebas complementarias a realizar con un síncope vasovagal serán:
Analítica de sangre con iones para descartar deshidratación.
Electrocardiograma que nos permita conocer posibles alteraciones cardíacas.
En casos determinados puede ser necesaria una valoración por el neurólogo para descartar problemas neurológicos.
Las pruebas complementarias tienen como fin descartar otros orígenes del síncope vasovagal.
Factores desencadenantes del síncope vasovagal
Son factores desencadenantes del síncope vasovagal, el calor excesivo , permanecer mucho rato de pie , o bien situaciones de estrés emocional .
Factores de riesgo del síncope vasovagal
Son factores de riesgo vasovagal las situaciones de deshidratación , ya sea por episodios de diarrea o vómitos o por falta de ingesta, y en personas ancianas, los tratamientos diuréticos o hipotensores .
Complicaciones del síncope vasovagal
Golpes o contusiones .
Fracturas de brazos o piernas.
Heridas inciso-contusas , en especial en la cabeza.
Prevención del síncope vasovagal
Beber abundante líquido durante el día.
Evitar periodos de ayuno prolongado .
Sentarse ante el malestar previo que produce el síncope.
Elevar las piernas .
Dormir con la cabeza incorporada .
Realizar ejercicios de tensión en las piernas a la vez que se aumenta la presión abdominal.
Ponerse de puntillas de forma repetida cuando se permanece mucho tiempo de pie.
Especialidades a las que pertenece el síncope vasovagal
El síncope vasovagal será valorado por el médico de familia , que estudiará este, remitiendo a cardiología o neurología si sospecha de otra etiología no vasovagal.
Preguntas frecuentes
¿Qué hacer cuando te da un síncope vasovagal?
Cuando se produce un síncope vasovagal, se debe tumbar al paciente en un lugar plano y elevar las piernas, y cuando mejore y se haya recuperado del proceso, se le dejará sentado un rato para luego incorporarle despacio .
¿Están relacionadas las convulsiones con los síncopes?
No, las convulsiones son un síntoma de la epilepsia , una alteración neurológica compleja que necesitarán de terapia anticonvulsivante. El síncope es una pérdida de conocimiento breve que no precisa de tratamiento tras la recuperación del paciente.
¿Qué es el reflejo vagal?
El reflejo vagal es la activación que se produce del nervio vago , que produce un descenso de los latidos cardíacos y un descenso de la tensión arterial, la cual se produce por una activación de este nervio, y que es el origen del síncope vasovagal.
¿Qué es perder el conocimiento?
La pérdida de conocimiento es el desmayo o la lipotimia , que se da cuando una persona pierde la conexión con el mundo exterior, no habla ni oye, ni reacciona a lo que se le indica desde el exterior. No es capaz de responder, y cuando el paciente se despierta no recuerda lo que ha ocurrido durante este tiempo.
¿Cuál es la diferencia entre síncope y epilepsia?
La epilepsia es la descarga neuronal que da lugar a convulsiones, esto es, se producen movimientos de las extremidades y el cuerpo del paciente. En el síncope no hay movimientos anormales, por el contrario, el paciente se queda sin responder y se le ve pálido . En general las pérdidas de conocimiento son menos preocupantes si su origen es vasovagal, no obstante, se deben estudiar por si fueran de origen cardiogénico.

Enfermedad
ETS
¿Qué es una ETS?
Las ETS, enfermedades de transmisión sexual , son el conjunto de enfermedades que se contagian de una persona a otra mediante el contacto sexual. También se conocen como enfermedades venéreas , enfermedades sexuales o infecciones de transmisión sexual (ITS). Las enfermedades de transmisión sexual son causadas por el contagio de virus, bacterias y parásitos , pudiéndose contraer por cualquiera persona que realice prácticas sexuales sin protección, tanto hombres como mujeres. Pertenecen a la especialidad de enfermedades infecciosas y son consideradas enfermedades de tipo grave.
Tipos de ETS
Las ETS pueden estar causadas por virus, bacterias, parásitos u hongos, diferenciándose 20 tipos diferentes, de las cuales las más comunes son:
VIH : virus de la inmunodeficiencia humana, es una de las ETS más graves. Recibe el nombre de SIDA, síndrome de inmunodeficiencia adquirida, en su fase terminal.
Gonorrea : no siempre presenta síntomas, pero puede llegar a ser una enfermedad muy grave. Provoca la inflamación de las vías urinarias y de los genitales y aumenta en exceso el flujo genital.
Sífilis : producida por una bacteria y que provoca alteraciones cutáneas al producirse úlceras.
Herpes genital : se producen llagas y úlceras en la zona de los genitales, provocando irritación, ardor e inflamación de la zona. Se puede transmitir antes de presentar síntomas.
Causas de las ETS
Las principales causas de las ETS se deben a la presencia, en el organismo, de bacterias, virus, parásitos u hongos , infectado tras la práctica de relaciones sexuales.
Síntomas de una ETS
Según el tipo de ETS que presente el paciente así serán los síntomas. No obstante, algunos de los síntomas son comunes en distintas enfermedades:
Llagas o úlceras en la zona bucal o genital.
Dolor o ardor genital.
Anomalías en el flujo vaginal.
Sangrado vaginal fuera del ciclo menstrual.
Fiebre y malestar.
Erupciones cutáneas.
Tratamiento para las ETS
Las enfermedades de transmisión sexual suelen ser tratadas con antivirales y antibióticos. En los casos en los que la enfermedad está muy desarrollada y los pacientes presentan gravedad, además del tratamiento con medicamentos, se realizan terapias psicológicas para que el paciente lo afronte de la mejor manera posible.
Pruebas complementarias del tratamiento de ETS
Para determinar si un paciente sufre o no una ETS se realizan las siguientes pruebas:
Análisis sanguíneo : se extrae una muestra de sangre del paciente para analizarla y evaluar si existen parámetros indicadores de ETS.
Análisis de orina : al igual que en el análisis de sangre, se toma una muestra de orina para determinar si existen patógenos causantes de la enfermedad.
Muestras de la zona : en caso de que se manifiesten síntomas externos como úlceras, llagas, eczemas o flujo genital extraño, se tomará también una muestra para analizar.
Factores desencadenantes de una ETS
El factor desencadenante de una enfermedad de transmisión sexual (ETS) es la práctica de relaciones sexuales sin el uso de protección y sin haberse realizado ambas partes las pruebas específicas para cerciorarse de que no padecen ni son portadores de ninguna ETS.
Factores de riesgo de una ETS
El factor de riesgo a la hora de adquirir una ETS es principalmente la práctica de relaciones sexuales , sobre todo sin protección. Además, mantener relaciones sexuales con diferentes personas incrementa el riesgo de contraerlas, a la vez que mantener relaciones sexuales con aquellas personas que padecen o están infectadas de alguna ETS, y aún más si no se usa protección.
Complicaciones de las ETS
Infertilidad.
Virus del papiloma humano (VPH)
Anomalías cardiacas.
Cáncer rectal.
Riesgos durante el embarazado.
Prevención de las ETS
Usar protección sexual en tus relaciones.
Cumplir la cartilla de vacunación.
Realizarse análisis para detectar las infecciones.
Conocer si la persona con la que mantienes relaciones sexuales es portador o padece alguna ETS para tomar las precauciones necesarias.
Especialidades a las que pertenecen las ETS
La especialidad médica encargada de tratar las ETS es enfermedades infecciosas.
Preguntas frecuentes:
¿Qué es la tricomona vaginal?
La tricomona vaginal, también conocida como tricomoniasis, es un tipo de ETS producida por un protozoo, el Trichomonas vaginalis. Es una de las enfermedades de transmisión más comunes y a la vez de las más fáciles de curar. Los síntomas son variados y muchas veces ni siquiera se manifiestan. Generalmente estos síntomas son picor e inflamación de las zonas sexuales.
¿Qué es la clamidia?
Es un tipo de ETS causado por una bacteria llamada Chlamydia trachomatis . Afecta al cuello del útero, la garganta y el recto.
¿Qué causa la sífilis?
La sífilis es una enfermedad de transmisión sexual causada por la bacteria Treponema pallidum , que infecta al organismo a través de las membranas mucosas de los genitales.
¿Cuánto tarda en manifestarse una ETS?
El tiempo en el que se manifiesta una ETS varía según el tipo, pueden ir desde 7 hasta 28 días o incluso no presentar síntomas.
¿Cómo puedo saber si tengo una ETS?
En primer lugar debes observar si padeces síntomas anómalos y acudir al médico a realizarte las pruebas correspondientes al diagnóstico de ETS, las cuales suelen ser: análisis de sangre, análisis de orina, examen pélvico y extracción de una muestra de tejido del cuerpo.

Enfermedad
Esquistosomiasis
¿Qué es la esquistosomiasis?
La esquistosomiasis es una enfermedad parasitaria producida por un gusano conocido como Schistosoma , que se transmite por trabajar o bañarse en aguas infectadas . Está presente en 78 países y de estos, en 52 se considera enfermedad endémica. Hay unos 200 millones de personas infectadas en todo el mundo. Se da en zonas tropicales y subtropicales , y un 92% de las personas que se encuentran enfermas pertenecen a África. Los niños y las mujeres embarazadas son los más sensibles a la infección. Es una enfermedad con una alta tasa de morbilidad , aunque su mortalidad no es muy alta, si bien no es muy conocida, ya que hay mortalidad que se produce por causas relacionadas con la esquistosomiasis. Es una enfermedad considerada de tipo grave.
Tipos de esquistosomiasis
Los tipos de esquistosomiasis son:
Esquistosomiasis intestinal : Schistosoma japonicum , Mekongi e Intercalatum , son los tipos de esquistosomas que lo producen. Afecta al sistema digestivo, donde se queda el esquistosoma.
Esquistosomiasis urogenital : afecta a la vejiga, los uréteres, los riñones y el aparto genital, y es producido por el Schistosoma haematobium.
Causas de la esquistosomiasis
Las causa es el contacto con aguas dulces infectadas por los parásitos que van a penetrar a través de la piel.
Síntomas de la esquistosomiasis
Síntomas de la esquistosomiasis intestinal : diarrea, dolor abdominal, sangre en las heces, aumento del tamaño del hígado y ascitis (presencia de líquido en la cavidad abdominal), hipertensión portal y aumento de tamaño del bazo.
Síntomas de la esquistosomiasis urogenital : incluye presencia de sangre en la orina, suele producirse fibrosis de la vejiga y de los uréteres acompañada de daño renal, y puede llegar a producir un cáncer de vejiga. En las mujeres puede dar lugar a alteraciones genitales con sangrado vaginal, dolor durante las relaciones sexuales y nódulos vulvares. En los hombres puede dañar las vesículas seminales y la próstata, así como puede producir infertilidad.
Tratamiento para la esquistosomiasis
El tratamiento de la esquistosomiasis es con Praziquantel contra los Schistosomas haemoliticum, mansoni e intercalatum. Se dará un día de tratamiento a dosis de 20mg/kg de peso dos veces al día un solo dia. En los sitios con prevalencia de Schistosomas japonicum y mekongi se da tres veces al día en una dosis de 20 mg/kg de peso también un solo dia. En los viajeros se deberá hacer el tratamiento pasadas de 6 a 8 semanas de la exposición. Se deberá r eexaminar a los pacientes a los 6-8 meses para ver si quedan huevos del parásito y repetir el tratamiento si fuera necesario.
Pruebas complementarias del tratamiento de la esquistosomiasis
Las pruebas complementarias serán analíticas , con búsqueda de anticuerpos y búsqueda de huevos en las heces o en la orina. Cuando hay alta sospecha de esquistosomiasis y no se consiguen observar huevos, se puede necesitar una biopsia de la mucosa intestinal o mucosa vesical.
Factores desencadenantes de la esquistosomiasis
La exposición a los Schistosomas por contacto con aguas contaminadas.
Factores de riesgo de la esquistosomiasis
Exposición a agua dulce que puede tener los gusanos.
Complicaciones de la esquistosomiasis
Anemia.
Hepatomegalia: aumento patológico del tamaño del hígado.
Esplenomegalia: agrandamiento patológico del bazo o estructura esplénica más allá de sus dimensiones normales (11 cm).
Ascitis: acumulación de líquido seroso en la cavidad peritoneal.
Infertilidad.
Cáncer de vejiga.
Alteraciones renales.
Prevención de la esquistosomiasis
Hervir el agua del baño durante un minuto y dejar enfriar antes de bañarse.
Almacenar el agua de baño durante al menos dos días antes de usarla
Ante caídas accidentales a zonas que pueden estar infectadas, proceder a secarse de forma intensa con una toalla y frotar con alcohol de 70 grados.
Especialidades a las que pertenece la esquistosomiasis
La esquistosomiasis debe ser tratada por un médico de medicina interna especialista en enfermedades tropicales.
Preguntas frecuentes:
¿En qué países es más probable que contraiga la esquistosomiasis?
S. haematobium : ampliamente distribuido en todo el continente africano con focos menores en Medio Oriente, Turquía e India.
S. mansoni : ampliamente distribuido en África, con focos en Medio Oriente y la única especie presente en el hemisferio occidental en zonas de Sudamérica y algunas islas del Caribe
S. japonicum : Asia, sobre todo en China, Filipinas, Tailandia e Indonesia
S. mekongi : sudeste de Asia
S. intercalatum : África Central y Occidental
Voy a viajar a un país subdesarrollado, ¿hay alguna vacuna contra la esquistosomiasis?
No existe ninguna vacuna contra el esquistosoma. El paciente no debe bañarse en ríos o aguas dulces que puedan estar contaminadas. Otros consejos son calentar el agua del baño o hervirla si fuera necesario para después dejarla enfriar antes de bañarse, y secarse con una toalla enérgicamente si se tiene contacto con agua contaminada, así como frotar con alcohol de 70 grados. Con estos consejos se evita el paso se los esquistosomas a través de la piel.
¿Cómo se contagia la esquistosomiasis?
Al bañarse en zonas donde hay caracoles con cercarias , que salen al agua dulce, entran en la piel de la persona, donde se convierten en esquistosomas, que penetran en los vasos sanguíneos y, a través de ellos, llegan al hígado, donde se transforman en adultos.
Artículos por especialidad
CertificadosAlergologíaAnatomía PatológicaAnestesiología y ReanimaciónAngiología y Cirugía VascularAnálisis ClínicosAparato DigestivoCardiologíaChequeosCirugía General y del Aparato DigestivoCirugía General y del Aparato Digestivo PediátricaCirugía Oral y MaxilofacialCirugía Ortopédica y TraumatologíaCirugía Ortopédica y Traumatología PediátricaCirugía PediátricaCirugía Plástica y ReparadoraCirugía TorácicaClínica u HospitalDermatología Médico-Quirúrgica y VenereologíaEndocrinología y NutriciónEnfermeríaFisioterapiaGenética HumanaGinecología y ObstetriciaInmunologíaLogopedia y FoniatríaMedicina Estética y Unidad LaserMedicina Física y RehabilitaciónMedicina GeneralMedicina InternaMedicina NuclearMedicina del DeporteNefrologíaNeumologíaNeurocirugíaNeurofisiología ClínicaNeurologíaNutrición y DietéticaOdontología y EstomatologíaOftalmologíaOncología MédicaOncología RadioterápicaOsteopatíaOtorrinolaringologíaPediatríaPodologíaPoliclínicasPreparación al PartoPsicologíaPsiquiatríaRadiodiagnóstico-Diagnóstico Por ImagenReumatologíaTricologíaUnidad del DolorUrgencias HospitalariasUrología
Todas las especialidades  Savia
Savia