Radiodiagnóstico-Diagnóstico Por Imagen
La especialidadArtículos especializados
Enfermedades
Síntomas
Otros contenidos
Artículo especializado
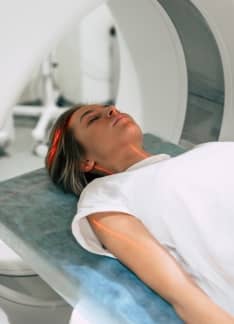
Diferencia entre TAC y Resonancia
En algunas ocasiones, para completar el estudio y llegar al diagnóstico de una patología es necesario realizar pruebas de imagen. Algunas de ellas son la tomografía axial computarizada (TAC) y la resonancia magnética .
¿Qué es el TAC?
La tomografía axial computarizada , TAC o escáner es una prueba diagnóstica por imagen en la que se utilizan rayos X sobre las áreas del cuerpo a estudiar. Posteriormente, toda la información obtenida es recogida por un ordenador que las ensambla para generar imágenes detalladas de diferentes planos o cortes de la zona de interés, permitiendo reconstrucciones anatómicas multiplanaes y tridimensionales.
Mediante las imágenes de un TAC se pueden analizar diferentes estructuras del organismo, aportando una gran resolución anatómica. Permite el estudio de diferentes partes del cuerpo y detectar enfermedades:
Cerebro: infecciones, tumores, accidentes cerebrovasculares y fracturas.
Aparato digestivo: tumores, infecciones y obstrucción intestinal.
Aparato urinario: litiasis, infecciones y tumores.
Aparato musculo esquelético: Tumores y fracturas.
Pulmones: neumonía, trombos, enfermedades pulmonares y tumores.
Hoy en día, esta técnica permite confirmar muchos de los diagnósticos que se llevan a cabo.
Debido a la utilización de rayos X, la radiación ionizante es el elemento que limita el uso del TAC. La dosis que utiliza es muy superior a la de una radiografía. La radiación se acumula y puede causar daño en los tejidos a largo plazo.
Preparación y explicación de la prueba
No es necesario ir en ayunas a no ser que se precise un estudio con contraste.
Se trata de una prueba no invasiva e indolora.
La máquina es circular como una rosquilla. El paciente debe tumbarse sobre la mesa del TAC. Debe estar tranquilo y quieto durante la prueba. Suele durar unos 20 minutos, dependiendo de la zona anatómica a estudiar.
A veces se necesita utilizar contraste intravenoso para visualizar mejor las imágenes o para un estudio concreto.
Es necesario informar cuando se está embarazada o dando lactancia, si tiene alergia al contraste o padece diabetes o asma.
¿Qué es la resonancia magnética?
La resonancia magnética es una técnica de diagnóstico basada en la imagen que utiliza un potente imán y ondas de radiofrecuencia muy altas para obtener imágenes de la zona anatómica a estudio. Estas imágenes oportunamente tratadas por un programa informático son analizadas por un médico radiólogo. De este modo, se obtiene información muy detallada y específica de la región corporal estudiada. El informe de la resonancia se entregará al médico solicitante que junto con el resto de información clínica hará un diagnóstico.
Se trata de una prueba no invasiva que no utiliza rayos X.
La resonancia nos informa sobre detalles de los órganos, vasos y tejidos músculo-esqueléticos, existiendo diferentes tipos en función de la zona que se quiere estudiar:
Resonancia magnética de huesos y articulaciones. Permite el estudio de la anatomía musculo esquelética y detectar infecciones, tumores, lesiones de ligamentos y músculos, fracturas óseas, etc.
Resonancia magnética de mama. Permite junto con la mamografía y ecografía mamaria estudiar tumores en las mamas.
Resonancia magnética del cerebro y medula espinal. Permite estudiar accidentes cerebrovasculares, tumores, esclerosis múltiple, hemorragias, lesiones en ojos, oído, etc.
Resonancia magnética de órganos internos. Permite el estudio de hígado, páncreas, bazo, riñones, ovarios, próstata, etc.
Resonancia magnética del corazón y sus vasos. Permite estudiar la estructura y función del corazón y así diagnosticar enfermedades del sistema cardiovascular.
Está indicada para estudio de diferentes enfermedades y en personas que no pueden realizarse TAC por ser alérgicas a los contrastes que utilizan.
Preparación y explicación de la prueba
Antes de la prueba hay que quitarse todos los objetos metálicos (joyas, relojes, dentadura, audífonos, etc.).
Es necesario avisar si es portador de marcapasos cardíaco, electrodos cardiacos o cerebrales, grapas usadas en las cirugías de los aneurismas, desfibrilador automático implantable, implantes cocleares y cualquier fragmento u objeto metálico introducido por accidente o cirugía en el organismo.
No es necesario acudir en ayunas, salvo que la prueba se realice con contraste.
Al comenzar la prueba el paciente se tumbará en una mesa que se moverá y le desplazará al interior de la máquina, que es como una especie de túnel. Se escucharán unos ruidos que darán fe del funcionamiento del aparato. La prueba suele durar entre 30 y 60 minutos.
En algunas ocasiones por problemas de claustrofobia, ansiedad o uso pediátrico es necesario realizar la prueba con sedación. También existen aparatos abiertos para personas con obesidad o para personas que por diferentes motivos no toleran la prueba cerrada.
Se debe informar al médico si se está embarazada o lactando, se padece insuficiencia renal grave, alergia al contraste o se ha sido trasplantado de hígado.
Principales diferencias entre TAC y RM
Una de las principales diferencias entre el TAC y la RM es que la segunda no utiliza rayos X y, por lo tanto, no presenta los efectos adversos de la radiación .
La duración de la exploración por TAC es menor que la que la resonancia.
El TAC no hace apenas ruido y es más abierto, por lo que no genera los problemas de claustrofobia y ansiedad de la resonancia, que es como un tubo alargado y más ruidoso.
Los equipos para realizar la resonancia son más caros que el TAC.
En el TAC no existen los problemas con los objetos metálicos como en la resonancia.
En definitiva, la resonancia magnética y el TAC son pruebas que facilitan el diagnóstico de diversas patologías, mediante distintas técnicas no invasivas. Cada una de estas pruebas tiene unas indicaciones específicas y debe ser el médico el que decida cuál es la más adecuada en función de la sospecha clínica y las características del paciente.
Artículo especializado
Gastrosquisis fetal: diagnóstico prenatal
¿Qué es la gastrosquisis?
La palabra gastrosquisis deriva del prefijo griego “gaster”: estómago y “schisis”: fisura. Actualmente, se define como una malformación congénita caracterizada por una herniación visceral a través de un defecto de la pared abdominal. La presencia de la fisura por lo general es pequeña (menos de 4 cm) y está localizada en la mayoría de los casos a la derecha del cordón umbilical.
Esta lesión da lugar a la herniación de las asas intestinales, el estómago, el hígado y en ocasiones la vejiga, que no se encuentran cubiertas por una membrana protectora. Las vísceras expuestas al líquido amniótico responden desarrollando un proceso inflamatorio de la capa seromuscular, la que además de serositis causa la destrucción de las células de Cajal; este daño seromuscular es el que da lugar a la hipomotilidad del intestino en el neonato.
Hay varias teorías que explican el origen de la gastrosquisis. La más aceptada considera como causa principal la involución precoz de los vasos que irrigan la pared abdominal que son la vena umbilical y la arteria onfalomesentérica derecha.
Los factores de riesgo más importantes asociados a esta patología incluyen:
El consumo de tabaco, alcohol y drogas como marihuana, cocaína, metanfetaminas.
Medicamentos como aspirina, efedrina e ibuprofeno.
Ser madre joven (menor de 20 años).
Primer parto.
Malnutrición y ausencia de fortificación con ácido fólico previo al inicio de la gestación.
Infecciones de transmisión sexual y del tracto urinario en el primer trimestre del embarazo.
La gastrosquisis presenta un porcentaje bajo de asociación con anomalías cromosómicas u otras malformaciones.
El pronóstico de la gastrosquisis está dado por las complicaciones intestinales asociadas, producidas por la inflamación ante la exposición a sustancias irritativas del líquido amniótico y la constricción, con la consiguiente isquemia a nivel del defecto de pared.
Se ha propuesto clasificar a la gastrosquisis en simple (sin lesiones intestinales) y gastrosquisis compleja (con anomalías intestinales asociadas como atresia, necrosis, vólvulo, perforación, etc.). El factor pronóstico más importante es la presencia de lesión en las asas intestinales, asociada a gran morbilidad debido a estancias hospitalarias prolongadas y complicaciones neonatales, aunque con un porcentaje elevado de supervivencia.
¿Cuándo y cómo se diagnóstica la gastrosquisis?
El diagnóstico prenatal de gastrosquisis se realiza cada vez más frecuentemente. Puede realizarse tan precozmente como a las 12 semanas de edad gestacional, ya que es en esta etapa cuando se produce el cierre definitivo parietal.
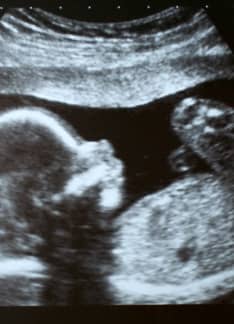
Sin embargo, lo más frecuente es que el diagnóstico prenatal se realice en el segundo trimestre de embarazo mediante ecografía morfológica .
La alfafetoproteína es la principal glicoproteína del suero fetal y está elevada en los pacientes con esta patología, por lo que puede servir para apoyar el diagnóstico, si bien no es específico de la gastrosquisis, ya que también se eleva en otras patologías.
La ecografía es el método de elección para la detección y la confirmación diagnóstica de la gastrosquisis en la etapa prenatal. El diagnóstico se realiza al detectar las asas intestinales flotando libremente en el líquido amniótico.
La mayor fortaleza del diagnóstico prenatal de gastrosquisis es la posibilidad de realizar consulta prenatal con cirujano, neonatólogo, ginecólogo y obstetra. El objetivo de la consulta prenatal será el de la evaluación conjunta por parte de un equipo interdisciplinario que estudiará el caso clínico. En base a ello brindarán asesoramiento y consejo a los padres, pudiendo además explicar las características de la patología, posible evolución y pronóstico.
El objetivo principal en el manejo perinatal de estos fetos es detectar aquellos casos con riesgo de presentar una gastrosquisis compleja, para esto se han descrito múltiples marcadores ecográficos para predecir la lesión intestinal, tales como dilatación de las asas extra o intra abdominales y la dilatación gástrica.
Savia pone a tu disposición los mejores especialistas en Ginecología y Obstetricia .
Tratamiento de la gastrosquisis
El tratamiento de la gastrosquisis es quirúrgico y consiste en devolver el intestino y los órganos herniados a la cavidad abdominal. Existen diferentes técnicas para lograr la reintroducción del contenido eviscerado al abdomen y el cierre parietal. En el mayor porcentaje de los casos es posible la realización de un cierre primario, borde a borde o utilizando el cordón umbilical para permitir el cierre con menor tensión parietal. En un porcentaje más bajo no es posible realizar un cierre primario, por lo que es necesario realizar un silo quirúrgico (bolsa de silicona que cubre el defecto y produce la reducción progresiva por gravedad de las vísceras) para protección del contenido eviscerado y una reintroducción progresiva del contenido abdominal. Posteriormente se realizará el cierre definitivo en una segunda intervención.
Actualmente el símil-EXlT ( Exit-Like procedure ), técnica de reducción de las vísceras intra abdominales, manteniendo el soporte placentario para evitar la deglución de aire por el recién nacido, se vislumbra como un procedimiento prometedor, encontrando mayor supervivencia, menor uso de ventilación y menor índice de infección.
En cualquier caso, se hace necesario un protocolo institucional que abarque el control prenatal, la planificación del parto, el soporte al recién nacido, el tipo y tiempo de cirugía, con seguimiento de las complicaciones postoperatorias, en aras de reducir la alta mortalidad postoperatoria.
¿Cómo prevenir la gastrosquisis?
Desde el punto de vista de la prevención, dado que se trata de una patología cuya incidencia está íntimamente relacionada con la edad de la madre, habría que hacer especial énfasis en la prevención de embarazos no deseados, especialmente cuando la madre es muy joven.
De igual modo, es muy importante en todas las mujeres embarazadas llevar a cabo las pertinentes pruebas durante el embarazo para la detección prematura y control de patologías en el feto y en la madre.

Artículo especializado
La radiografía lateral de cavum: ¿para qué sirve?
Las amígdalas faríngeas, tonsilas faríngeas, adenoideas o vegetaciones son un tejido linfoide que fabrica sustancias inmunitarias contra las infecciones. Se encuentra situado en la parte posterior de la nariz.
Nos defiende de los patógenos que entran en nuestro organismo por las fosas nasales y por la boca.
Los catarros y las infecciones respiratorias hacen que aumenten de tamaño, siendo más frecuente en edad escolar (3-6 años). En algunos casos, esa hipertrofia origina obstrucción del paso del aire por la cavidad nasal produciendo síntomas como ronquidos, moqueo persistente, pausas de respiración durante el sueño, falta de concentración e infección de oídos.
Cuando esto sucede es necesario consultar con el pediatra para su estudio.
¿Qué es una radiografía lateral de cavum?
Es una prueba de imagen con rayos X que permite estudiar diferentes zonas de la anatomía de la nariz y boca (adenoides y amígdalas palatinas) y así detectar si existen problemas de permeabilidad y funcionalidad en la vía aérea.
¿Cómo se realiza una radiografía lateral de cavum?
Es una prueba no invasiva y que no requiere ningún contraste.
Consiste en la realización de una radiografía con una proyección lateral del cráneo y cuello. Para ello el paciente se coloca con la boca cerrada para respirar por la nariz y con el cuello extendido. Como en cualquier radiografía, se deben retirar todos los objetos metálicos que puedan alterar la imagen y comprometer la eficacia diagnóstica.
El nivel de radiación que se aplica es muy bajo.
Las mujeres embarazadas deben advertir de su estado antes de que les realicen una radiografía simple de cabeza para valorar el riesgo para el feto.
¿Qué ocurre si tengo los adenoides inflamados?
En etapa escolar es frecuentes padecer infecciones respiratorias que hacen que el tejido linfoide de las adenoides crezca y se hipertrofie, ya que está trabajando para acabar con los patógenos y por eso crece.
Cuando este crecimiento produce obstrucción de la vía área pueden existir problemas de salud como rinorrea, otitis de repetición, apneas nocturnas, ronquidos, voz gangosa, irritabilidad y falta de concentración.
Diagnóstico de hipertrofia adenoidea
Tras una historia clínica detallada y ante la sospecha de una hipertrofia adenoidea es necesario realizar exploraciones complementarias. Las adenoides no se observan a simple vista, por lo que se puede utilizar:
Rinoscopia anterior. Consiste en introducir un pequeño tubo a través de la nariz y se observa el interior de las fosas nasales.
Se observa la cavidad oral y la garganta desde fuera, ayudado por luz y depresor lingual.
La nasofibroscopia, consiste en introducir una cámara muy fina a través de uno o ambos orificios nasales. Sirve para observar directamente el tejido adenoideo. Si no es posible esta prueba por falta de colaboración se puede solicitar radiografía lateral cavum .
Estudio del sueño o polisomnografía.
Extracción quirúrgica
La extracción quirúrgica de las adenoides hay que valorarla como tratamiento cuando existe hipertrofia adenoidea con otros síntomas:
Obstrucción nasal crónica.
Otitis media aguda recurrente.
Rinitis y sinusitis aguda recurrente o crónica.
Otitis media con supuración crónica.
Síndrome de apnea del sueño.
Las decisiones sobre el tratamiento quirúrgico deben individualizarse de acuerdo con los posibles beneficios y riesgos, el curso natural de la enfermedad y los valores y preferencias de la familia y el niño.
¿Para qué sirve una radiografía lateral de cavum?
La radiografía lateral de cavum era una prueba muy solicitada para descartar la hipertrofia adenoidea.
Actualmente y según una revisión reciente (Preevid 19) se concluye que “en niños con sospecha de hipertrofia adenoidea el examen endoscópico de la nasofaringe parece ser el método más preciso y el que mejor se correlaciona con la gravedad de la enfermedad en lo que respecta a la estimación del tamaño adenoideo”. “Respecto al papel de la radiografía lateral de “cavum” en niños con sospecha de hipertrofia adenoidea, se indica que no sería necesaria su realización y que para la confirmación diagnóstica lo mejor sería la visualización directa de las adenoides”. “No obstante consideran que se podría utilizar como estrategia diagnóstica en la evaluación de los niños con sospecha de hipertrofia adenoidea, fundamentalmente cuando no cooperan para la endoscopia o en los que no es posible su realización”.
Por lo que con los métodos diagnósticos actuales y según la últimas revisiones estaría indicada la radiografía lateral de cavum en sospecha de hipertrofia adenoidea en niños no colaboradores.
Preguntas frecuentes
¿Qué son las adenoides?
Las amígdalas faríngeas, tonsilas faríngeas, adenoideas o vegetaciones son un tejido linfoide que se encuentra en la nasofaringe.
Junto con las amígdalas palatinas y linguales forman el anillo linfático de Waldeyer. En su superficie se produce una gran cantidad de sustancias inmunitarias, constituyendo una importante barrera frente a las infecciones.
Aumentan muy rápidamente durante los primeros años y se atrofia en la adolescencia.
¿Qué es una adenoidectomía?
Es la extirpación o extracción quirúrgica de las glándulas adenoides.
Esta cirugía se realiza bajo anestesia general y de forma ambulatoria, por lo que la gran mayoría de los pacientes pueden volver a su domicilio en unas horas.
Artículo especializado
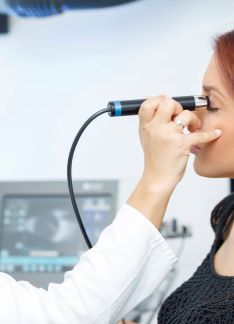
Ecografía ocular: ¿qué detecta?
La ecografía ocular o ecografía oftalmológica es una exploración inocua, rápida, indolora y segura.
Permite obtener datos y mediciones de la estructura del globo ocular y es de gran utilidad para el seguimiento y diagnóstico de patología oculares.
La ecografía ocular es un método diagnóstico que utiliza ultrasonidos para producir imágenes de las estructuras internas del ojo de forma segura y evitando el riesgo de otras pruebas basadas en la radiación.
¿Qué es una ecografía ocular?
La ecografía ocular u oftalmológica es una técnica de diagnóstico por imagen que utiliza ultrasonidos que se emiten a través del globo ocular y se transforman en imagen en una pantalla. De esta forma, podemos estudiar la anatomía del ojo y detectar anomalías de forma no invasiva.
La ecografía ocular es una técnica cómoda, rápida, indolora y segura para el paciente que nos da información en tiempo real.
Tipos de ecografías oculares
La ecografía ocular permite realizar 3 tipos de evaluaciones distintas en función del tipo de lesión a examinar:
La ecografía B, B-Scan o ecografía bidimensional es la más común y permite la obtención de imágenes y vídeos del interior del ojo y de la órbita. Nos da información sobre la localización, forma, crecimiento y consistencia de las lesiones en el interior de ojo.
La ecografía A, A-Scan o ecografía unidimensional estudia la estructura, consistencia y medidas exactas de una lesión. Se utiliza para conocer el valor dióptrico de la lente intraocular en la cirugía de catarata y en la órbita estudia el espesor de los músculos oculares y el nervio óptico.
La ultrabiomicroscopía, biomicroscopía ultrasónica o UBM utiliza ultrasonidos de alta frecuencia. Es un método diagnóstico para el estudio de estructuras de la parte anterior del ojo, incluyendo iris, el ángulo iridocorneal, el cristalino y la córnea.
¿Cómo es el procedimiento de una ecografía ocular?
El procedimiento para realizar una ecografía ocular es muy sencillo y no requiere preparación previa.
El paciente se coloca generalmente en sedestación y con los párpados cerrados. Se aplica gel en la sonda del ecógrafo y se apoya suavemente sobre los párpados. Se pide al paciente que mueva los ojos en diferentes posiciones para hacer un estudio completo de la estructura ocular.
En la UBM la prueba se realiza con los ojos abiertos. Se administran gotas de anestésico para evitar las molestias de un separador que se coloca entre los párpados para mantenerlos abiertos.
¿Es peligroso realizarse una ecografía ocular?
La exploración es indolora para el paciente y absolutamente inocua.
¿Requiere de alguna preparación previa?
La ecografía oftalmológica no requiere ningún tipo de preparación previa.
Se recomienda no aplicar maquillaje en la zona cercana a los ojos.
La prueba dura aproximadamente 10 minutos.
¿Qué lesiones se pueden diagnosticar con una ecografía oftálmica?
Lesiones de la cámara anterior del ojo.
Lesiones del iris.
Valoración de los músculos oculomotores que permiten el movimiento a los globos oculares.
Alteraciones en la morfología y tamaño del globo ocular (cuerpos extraños, roturas).
Traumatismos oculares.
Lesiones del cristalino como cataratas, luxación o subluxación del cristalino y ausencia de cristalino.
Patologías del vítreo (hemorragias, desprendimiento, infección).
Desprendimiento de retina.
Diámetro del nervio óptico.
Tumores intraoculares.
Artículo especializado
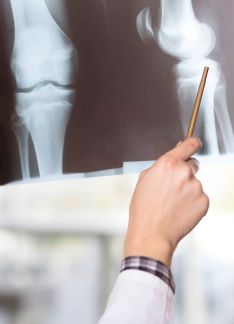
Radiografía de rodilla: ¿por qué se hace?
La rodilla es una articulación bisagra con gran movilidad, que contiene estructuras óseas, musculares, tendinosas y ligamentosas.
El dolor y los traumatismos en rodilla suelen ser frecuentes a cualquier edad, por lo que es habitual que el médico solicite una radiografía rodilla para estudiar posibles lesiones.
Suele ser la primera prueba solicitada para estudiar la rodilla tras una exploración física detallada.
¿Qué es una radiografía de rodilla?
Una radiografía de rodilla es una prueba radiológica de diagnóstico por imagen no invasiva, indolora, que no requiere anestesia ni el uso de contrastes.
Se trata de una de las formas más prácticas y rápidas para que los especialistas evalúen el estado de las estructuras internas de la rodilla a través de imágenes, especialmente los huesos y la articulación.
Esta prueba la pueden solicitarla médicos de familia, internistas, traumatólogos, reumatólogos, rehabilitadores u otros especialistas.
¿Cómo se hace una radiografía de rodilla?
Para poder obtener las imágenes por medio de una radiografía, un técnico en radiología situará la rodilla a evaluar en la máquina de rayos X. Esta trabaja con haces de rayos X a dosis controladas que son absorbidos en diferente grado en función de la densidad de las estructuras sobre las que son aplicados. De este modo, se obtienen unas imágenes en blanco y negro en las que los huesos, más densos, son blancos, y el resto de tejidos aparecen en una escala de grises. Este contraste permite la valoración de la morfología normal y el diagnóstico de las patologías.
No requiere de preparación previa.
El examen radiológico se lleva a cabo en la sala de radiología del hospital o en el consultorio del médico. Antes de hacer el estudio se deben retirar la ropa y los objetos metálicos de la zona a explorar que pueden impedir la correcta realización del estudio.
El examen radiológico de rutina de la rodilla consiste en proyección anteroposterior (rodilla completamente extendida) y lateral (rodilla flexionada 30 grados y tendido sobre la rodilla afectada).
Cuándo pedir una radiografía de rodilla
La radiografía será solicitada por un facultativo para estudio complementario de:
Dolor de rodilla.
Inflamación articular.
Limitación de movilidad.
Inestabilidad de la articulación.
Estudio antes y después de cirugía de rodilla.
Sospecha de infección ósea.
Seguimiento de fracturas.
De este modo, la radiografía de rodilla permite detectar fracturas, defectos osteocondrales, lesiones óseas, derrames articulares, estrechamiento del espacio articular y alteraciones en la alineación de los huesos.
¿Qué diagnostica una radiografía de rodilla?
La radiografía de rodilla puede ser útil en diferentes situaciones. Las más comunes son:
Enfermedad articular degenerativa (artrosis, artritis).
Derrame articular.
Alteraciones de la mineralización ósea.
Problemas crónicos en la articulación.
Riesgos y limitaciones de una radiografía de rodilla
El nivel de radiación de una radiografía simple de extremidades, gracias a los avances de la tecnología, es muy bajo y no entraña de manera aislada ningún riesgo para la salud del paciente. Las mujeres embarazadas deben advertir su estado al médico por el riesgo para el feto.
En cualquier caso, el médico valorará los riesgos de radiaciones innecesarias. Dependiendo de las circunstancias específicas del paciente, se pueden indicar otras pruebas diagnósticas que pueden ofrecer resultados similares, como la resonancia magnética o la ecografía, técnicas no invasivas, indoloras y que no utilizan radiación ionizante.
Por otro lado, la limitación fundamental de la radiología convencional es que las imágenes obtenidas solo muestran dos dimensiones, por lo que en ocasiones es difícil delimitar bien algunos aspectos anatómicos. En algunos a casos es necesario completar el estudio con ecografía o resonancia magnética.
Artículo especializado
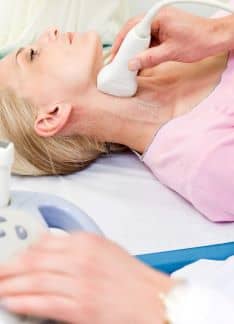
¿Qué es un Ecosonograma o ecografía Doppler?
Un ecosonograma o ecografía es una prueba de diagnóstico médico por imagen que utiliza ondas sonoras. Por lo tanto, se trata de una técnica sin riesgo que no requiere ninguna preparación. De este modo, se utiliza de forma habitual para el control del embarazo, en las revisiones de ginecología, para analizar el corazón, los vasos sanguíneos y diferentes órganos. También se utiliza para la evaluación de lesiones músculo-articulares y deportivas.
La ecografía se basa en la emisión de ultrasonidos −ondas sonoras de alta frecuencia− que se difunden por los órganos blandos que contienen agua.
El transductor o emisor de ultrasonidos se coloca sobre la piel, próximo al órgano o estructura que se quiere estudiar. Las ondas atraviesan los órganos y acaban rebotando a diferentes frecuencias según la densidad de los tejidos. El mismo transductor recoge las ondas que le vienen devueltas y envía la información a un ordenador que las transforma en imágenes en la pantalla del ecógrafo.
¿Qué tipos de ecografías hay?
Las diferentes ecografías que se pueden llevar a cabo dependen de la zona anatómica a explorar. De este modo, se pueden diferenciar, entre otros, los siguientes tipos de ecografías:
Ecografía abdominal . Es útil para evaluar los órganos situados dentro del abdomen, como el hígado, las vías biliares, riñones, vejiga y otras estructuras.
Ecografía ginecológica . Es útil para valorar el útero y los ovarios. Se puede realizar de forma abdominal o transvaginal.
Ecografía de próstata . Es útil para detectar anomalías prostáticas.
Ecografía de tiroides .
Ecografías del embarazo . Se utilizan para valorar la evolución del feto y del embarazo.
Ecocardiograma . Es útil para valorar el corazón y su funcionamiento tanto en reposo como tras un esfuerzo.
Ecografía venosa y arterial . Para evaluar la presencia de trombos y varices en las venas o trastornos en las arterias.
Ecografía articular . Es útil para valorar lesiones en ligamentos, tendones y articulaciones.
Ecografía para diferentes intervenciones . En multitud de casos la ecografía sirve de guía para llevar a cabo diferentes procedimientos terapéuticos con seguridad, como biopsias, tratamientos tumorales, exploraciones, etc.
En Savia ponemos a tu disposición ecografías desde 17 € .
¿Qué es la Ecografía Doppler?
Dentro de las ecografías, la ecografía Doppler es un tipo especial de estudio ultrasónico que utiliza el efecto descrito por el físico Christian Doppler que relaciona la longitud de onda con la velocidad de los cuerpos. De este modo, cuando el órgano que se estudia está en movimiento como el corazón o la sangre, emite una frecuencia distinta si el movimiento va en el sentido del transductor o en sentido contrario. El aparato ecográfico interpreta los datos y ofrece imágenes de los órganos en colores dentro de la gama del rojo y el azul.
Para llevar a cabo la prueba se coloca el transductor en la zona que se desea explorar y mediante el eco-Doppler se obtienen imágenes de estructura, velocidad del flujo e indirectamente, el volumen circulante en arterias y venas.
¿Cuándo está indicada una ecografía Doppler?
Se trata de la prueba principal para el diagnóstico de enfermedades relacionadas con la circulación de la sangre y los problemas cardíacos. De este modo, la ecografía Doppler es muy útil en la detección de trastornos circulatorios en el abdomen, las extremidades, el cerebro y en órganos como el hígado y los riñones.
De manera específica, la ecografía Doppler puede resultar una técnica diagnóstica útil en las siguientes situaciones:
Problemas circulatorios en órganos y tejidos.
Control de la evolución de las lesiones que pueden aparecer en las arterias carótidas.
Accidente cerebrovascular o ictus.
Problemas de coágulos y trombos en las venas de las extremidades.
Aneurismas y varices.
Seguimiento del embarazo, especialmente la fase final. Es útil para detectar patologías cardiacas del bebé, entre otros problemas.
Tipos de Doppler
Dentro de las técnicas de ecografía Doppler se puede distinguir el Doppler en imagen que distingue en función de las direcciones de flujo y movimiento. Por otro lado, el Doppler espectral muestra la medición de flujo sanguíneo, por ejemplo de una arteria, en forma de gráfico.
Riesgos y contraindicaciones de una ecografía Doppler
Las ecografías son pruebas que no suponen ningún riesgo para el paciente y no presentan contraindicaciones.
La ecografía Doppler tampoco requiere de ninguna preparación especial, es una técnica indolora y no invasiva que no requiere de sedación y se realiza de forma ambulatoria.
¿Cuánto vale una ecografía Doppler?
Se puede realizar una ecografía desde 17 €. En el caso de una ecografía Doppler, incluyendo una consulta de cardiología, el precio puede rondar los 70 €.
En Savia contamos con los mejores centros y especialistas en ecografía Doppler .
Bibliografía
Sociedad Española de Ecografía. Casos clínicos. Consultado: 07/12/2021 .
Sociedad Española de Ultrasonidos. Guías técnicas SEUS. Consultado: 07/12/2021 .
Loncaric F et al. La integración de la inteligencia artificial en el abordaje clínico del paciente: enfoque en la imagen cardiaca. Rev Esp Cardiol 2020; 74(1): 72-80. DOI: 10.1016/j.recesp.2020.07.012 .
Perez L et al. Documento de consenso de SEMI, semFYC, SEN y SEC sobre ecocardioscopia en España. Rev Esp Cardiol 2018; 71(11): 935-940. DOI: 10.1016/j.recesp.2018.05.027 .

Artículo especializado
Resonancia magnética con contraste
Las técnicas de diagnóstico por imagen han mejorado significativamente con el avance tecnológico y se constituyen como una herramienta insustituible en la práctica clínica. La resonancia magnética se ha convertido en las últimas décadas en un procedimiento esencial, debido a la excepcional diferenciación que permite de los tejidos blandos y la ausencia de radiación ionizante, que sí presentan otras técnicas.
Junto con una amplia variedad de mecanismos para diferenciar los tejidos endógenos, existe la posibilidad de utilizar agentes de contraste que determinan una mayor sensibilidad para poder identificar numerosas lesiones y patologías.
Qué es la resonancia magnética con contraste
La resonancia magnética es un tipo de prueba diagnóstica por imagen que permite analizar estructuras óseas y blandas, vísceras, vasos sanguíneos y las estructuras del sistema nervioso central.
Este procedimiento utiliza ondas de radio enfocadas en la zona del cuerpo que se quiere estudiar y que está sometida, a su vez, a un campo magnético. Éste determina que los núcleos de hidrógeno (protones) presentes en las estructuras del cuerpo absorban cierta cantidad de energía electromagnética. En estas condiciones, las ondas de radio son devueltas por los protones de una forma característica y son captadas por diferentes sensores. Finalmente, toda la información es procesada en un ordenador que la muestra en forma de imágenes precisas.
Su principal característica es que permite la obtención de imágenes de gran calidad y detalle, lo cual es muy útil para que el médico detecte modificaciones en las estructuras y tejidos y pueda establecer un diagnóstico, especialmente relacionadas con las partes blandas no óseas.
Además, esta exploración permite realizar el seguimiento evolutivo de lesiones sometidas a tratamiento y es muy eficaz como herramienta preoperatoria para observar la región anatómica que se debe intervenir.
La realización de una resonancia magnética nuclear puede estar indicada cuando otras pruebas diagnósticas más sencillas, como una radiografía o una ecografía, no permiten hacer un diagnóstico certero. La resonancia es especialmente útil para estudiar:
Tumores y quistes.
Tejidos con hemorragias.
Roturas de tejidos blandos.
Lesiones cardíacas e infartos.
Aneurismas y arterias.
Lesiones intracraneales.
Lesiones de la columna.
Glándulas y órganos (páncreas, tiroides, hígado, riñones, etc.).
Estructuras blandas de articulaciones y músculos.
Qué es el contraste
Los agentes de contraste para la resonancia magnética son una clase de productos farmacéuticos que mejoran la diferenciación por imagen entre el tejido normal y el dañado y permiten valorar el estado funcional de los órganos y el flujo sanguíneo. Estas sustancias tienen la capacidad de acumularse en determinados tejidos, modificando temporalmente sus propiedades electromagnéticas y, por tanto, destacándolos en las imágenes obtenidas en la resonancia magnética.
Para qué sirve el contraste
Junto con la amplia variedad de mecanismos de diferenciación tisular que permiten los aparatos de resonancia magnética, la aplicación de sustancias de contraste puede ser útil para diferenciar o destacar lesiones en diferentes tejidos, como tumores y anomalías vasculares y cardíacas, entre otros.
Generalmente, el contraste se administra por vía intravenosa por medio de una sonda. También se puede inyectar directamente en una articulación.
Otras vías de administración para otros tipos de contraste usados en técnicas de diagnóstico por imagen como los rayos X o el TAC incluyen la vía oral para visualizar el tracto digestivo alto o la vía rectal para evaluar el recto y el colon.
Qué sustancias se incluyen en el contraste
Las sustancias más utilizadas como contraste en la resonancia magnética son moléculas que contienen ciertos metales, como los quelatos de gadolinio o los óxidos de hierro.
De este modo, se pueden diferenciar dos tipos de contrastes:
Contrastes positivos . Principalmente moléculas que contienen gadolinio, un metal que acentúa la señal electromagnética emitida desde las células.
Contrastes negativos . Principalmente compuesto de hierro. Debilitan las señales electromagnéticas de ciertos tejidos, resaltando las estructuras adyacentes.
Por otro lado, existen algunos efectos secundarios que pueden aparecer tras la utilización de un contraste de gadolinio. Éstos son leves e incluyen cefalea, dolor en la zona de inyección, náuseas, vómitos o erupción cutánea. En cuanto a una posible reacción alérgica, si bien es poco común (la existencia de reacciones alérgicas graves en el caso del gadolinio resulta excepcional, situándose entre un 0,001 y un 0,1%), es importante tenerlas en cuenta. También es importante tener en cuenta los posibles efectos a la hora de administrar un contraste de gadolinio en mujeres embarazadas y en los pacientes con insuficiencia renal.
Si necesitas una resonancia magnética en Savia ponemos a tu alcance a los mejores especialistas muy cerca de ti.
Bibliografía
Yan GP, Robinson L, Hogg P. Magnetic resonance imaging contrast agents: Overview and perspectives. Radiography 2007; 13(1): e5-e19. Doi: 10.1016/j.radi.2006.07.005 .
Anderson CE et al. Dual Contrast – Magnetic Resonance Fingerprinting (DC-MRF): A Platform for Simultaneous Quantification of Multiple MRI Contrast Agents. Sci Rep 2017; 7: 8431. Doi: 10.1038/s41598-017-08762-9 .
Li H, Meade TJ. Molecular Magnetic Resonance Imaging with Gd(III)-Based Contrast Agents: Challenges and Key Advances. J Am Chem Soc 2019; 141(43): 17.025-17.041. Doi: 10.1021/jacs.9b09149 .
Ministerio de Sanidad. Unidad asistencial de diagnóstico y tratamiento por la imagen. Estándares y recomendaciones de calidad. 2013. Consultado: 19/11/2021 .
Sociedad Española de Imagen Cardíaca. ¿Cuáles son las precauciones que se deben considerar cuando se usa gadolinio? Consultado: 19/11/2021 .

Artículo especializado
Información Ecografía Testicular
Actualizado el 17/12/2021
La ecografía testicular es la primera prueba diagnóstica utilizada en pacientes que presentan dolor o inflamación en los testículos y a nivel escrotal. También cuando se aprecia la presencia de una masa palpable o se ha producido un trauma.
Como todas las ecografías, se trata de una prueba no invasiva y que no emite radiación ionizante.
¿Qué es la ecografía testicular?
La ecografía testicular es una prueba diagnóstica por imagen que permite visualizar los tejidos y estructuras de los testículos y las zonas adyacentes. Con frecuencia se complementa mediante la ecografía Doppler, que permite ver el flujo sanguíneo y la irrigación de las estructuras estudiadas.
Además de los testículos, el resto de estructuras próximas que permite explorar la ecografía incluyen:
El epidídimo.
Las vesículas seminales.
Las venas y vasos linfáticos de los testículos.
El escroto.
¿Cómo se realiza?
La ecografía permite la obtención de imágenes en tiempo real. El ecógrafo funciona por medio de un transductor que emite ultrasonidos cuyo reflejo es recogido por el mismo transductor. El tratamiento de las ondas reflejadas por un ordenador determina la obtención de imágenes de las distintas estructuras testiculares. No se trata de radiaciones ionizantes y las imágenes se obtienen en tiempo real, lo que permite ver el movimiento de los órganos o el flujo sanguíneo.
En el inicio de la prueba se coloca un gel sobre el escroto para facilitar el movimiento del transductor y la emisión y captación de ultrasonidos.
¿En qué casos puede ser útil la ecografía testicular?
La ecografía testicular es muy útil para valorar diversas situaciones, tanto en adultos como en niños:
Masas testiculares. La ecografía testicular es una prueba esencial tras la aparición de una masa palpable. La mayoría de estas suelen ser benignas, frente a las malignas, caracterizadas por aparecer de forma intratesticular. La ecografía permite poder diferenciar si se trata de una masa sólida que pudiera constituir un posible tumor o de una masa líquida, como en el caso de un quiste.
En este sentido, el cáncer de testículo es el tumor más frecuente en hombres entre los 15 y los 35 años. Más allá de ese pico de incidencia, solo supone el 1% de los tumores en varones. En 2019 en España se diagnosticaron aproximadamente 1.300 casos.
Epididimitis . La ecografía testicular es también útil para valorar patologías en las estructuras adyacentes al testículo, como el epidídimo (colector del esperma que producen los testículos) y las vesículas seminales. El dolor testicular puede ser indicativo de una epididimitis. La ecografía testicular permitirá apreciar la inflamación de esta estructura. Por otro lado, si aparece sangre en el esperma puede ser debido a un quiste en las vesículas seminales, una lesión que también se apreciará en la ecografía testicular.
Hidrocele . Consiste en la acumulación de líquido entre las capas que rodean al testículo. Esta situación puede causar un aumento del tamaño escrotal que cursa con dolor. En la ecografía se podrá apreciar el líquido acumulado.
Varicocele . Es una dilatación o variz de las venas que irrigan los testículos. Causan molestia escrotal y pueden comprometer la fertilidad. En la ecografía se podrán apreciar las dilataciones tortuosas de los plexos venosos.
Torsión testicular . La torsión testicular supone una urgencia quirúrgica. Está relacionada con una acción en el desarrollo fetal y se manifiesta en la adolescencia con un fuerte dolor que puede llevar a la necrosis y pérdida del testículo. La ecografía testicular permite valorar la inflamación del testículo, la torsión y, mediante el Doppler, la irrigación sanguínea. En casos de traumatismos graves, la ecografía permite valorar si hay afectación del tejido testicular y si existen hematomas dentro o fuera de la gónada.
Testículo no descendido. En niños, la ecografía testicular suele ser útil para valorar la ausencia de testículos en el saco escrotal. Esto puede ser debido a que no se ha producido el descenso del testículo. La ecografía permite localizar los testículos que, mediante cirugía, se harán descender al saco escrotal. Dado que los testículos no descendidos tienen una mayor incidencia de cáncer, la intervención para su descenso se debe hacer cuanto antes. El testículo no descendido aparece en el 3% de los nacidos a término.
Riesgos de la ecografía testicular
Se trata de una prueba no invasiva que no utiliza radiación ionizante por lo que no presenta riesgos para el paciente.
Las escasas molestias que se pueden notar vienen dadas por el frío del gel utilizado para facilitar el desarrollo de la prueba y la presión sobre las estructuras estudiadas. En general, es una prueba que dura media hora como máximo.
Hazte una ecografía testicular sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí .
Preguntas frecuentes
¿Qué es una ecografía testicular?
Una ecografía testicular es una prueba diagnóstica por imagen basada en la utilización de ultrasonidos para visualizar las diferentes estructuras de la zona escrotal.
¿Qué se ve en una ecografía testicular?
La ecografía testicular muestra las estructuras escrotales y permite identificar anormalidades en los testículos y los tejidos adyacentes.
¿Cuánto tiempo dura una ecografía testicular?
El tiempo aproximado de la exploración es de 30 minutos. Tras ella, el radiólogo realiza un informe sobre los hallazgos de la prueba.
¿Qué es una ecografía Doppler testicular?
La ecografía Doppler testicular permite la visualización de los elementos en movimiento, por lo que sirve para evaluar el flujo sanguíneo en los vasos que irrigan la zona escrotal.
¿Cuánto cuesta una ecografía testicular?
Una ecografía testicular puede costar a partir de 20 €.
Bibliografía
Sociedad Española de Ultrasonidos. Información al paciente. Ecografía testicular. Consultado: 10/12/2021 .
Rodríguez JF. Sociedad Española de Oncología Médica. Cáncer de testículo. 29/01/2020. Consultado: 10/12/2021 .
Rodríguez R et al. Ecografía testicular. Arch Esp Urol 2006; 59(4): 441-454 .
Rebik K, Wagner JM, Middleton W. Scrotal Ultrasound. Radiol Clin North Am. 2019; 57(3): 635-648. Doi: 10.1016/j.rcl.2019.01.007.
Artículo especializado
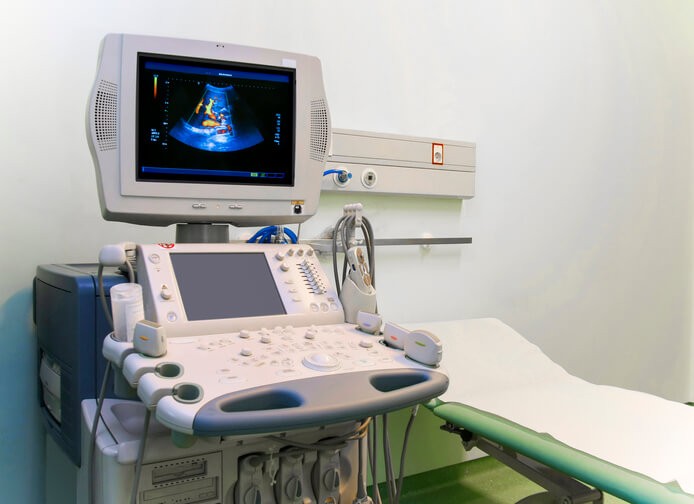
Ecografía Doppler
La ecografía es una prueba médica diagnóstica de imagen, absolutamente inocua , que no requiere de ninguna preparación y que se puede realizar sin causar ninguna molestia ni producir ningún efecto sobre los tejidos que estudia. Por este motivo la usamos con tanta asiduidad para control del embarazo y en ginecología, tanto sobre el abdomen como por vía vaginal, pues al estar el feto sumergido en la bolsa de aguas podemos obtener imágenes muy detalladas de su anatomía. Te explicamos en qué consiste la ecografía y, en particular, la Doppler.
Hazte una ecografía doppler sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
¿En qué consiste?
La ecografía se basa en la emisión de ultrasonidos , que son unas ondas sonoras de alta frecuencia (no las podemos oír, pero se transmiten como el sonido), que se difunden por los órganos blandos. No se transmiten por el aire ni por los órganos que no contienen agua, como los huesos.
Existe un transductor , que es el emisor del ultrasonido, que se coloca sobre la piel próxima al órgano a estudiar, a la que se ha aplicado previamente un gel acuoso que permitirá que se transmita por ella la onda, pues como hemos comentado no habría una buena difusión de esa energía sobre la piel seca. La onda atraviesa los tejidos del territorio que abarca y se va encontrando con diferentes órganos de distinta consistencia, que la harán rebotar en una frecuencia u otra según su densidad. El mismo transductor recoge las ondas que le vienen devueltas y envía la información a un ordenador que en función de las densidades que ha encontrado y a qué profundidad hará la composición de una imagen que veremos en la pantalla del ecógrafo.
En el embarazo…
Como hemos comentado, por el aire los ultrasonidos no se transmiten, y este es el motivo por el que para realizar una ecografía ginecológica en una paciente a la que no se puede explorar por vía vaginal , o para realizar una ecografía prostática a un paciente varón, pedimos que beban mucho líquido y aguanten las ganas de orinar para que la vejiga de la orina llena nos haga de pantalla que transmita los ultrasonidos a los órganos que hay detrás de ella. De lo contrario, los intestinos y el aire que hay en su interior se interpondrían entre el transductor y el órgano a explorar (útero y ovarios o próstata) impidiendo su visualización.
Particularidades de la Doppler
La ecografía Doppler es un tipo especial de estudio ultrasónico . Utiliza el efecto descrito por un físico llamado Doppler por el cual cuando el órgano que estamos estudiando está en movimiento , como el corazón o la sangre que circula por las distintas venas y arterias, emite una frecuencia distinta si el movimiento va en sentido del transductor o en sentido contrario, y nos puede dar información de la velocidad a la que se mueve. El ordenador del ecógrafo interpreta estos datos y nos ofrece una imagen del órgano en movimiento en colores de la gama de los rojos (desde el rojo intenso-anaranjado-casi amarillo) y de los azules (desde el azul más intenso al más claro casi verde). Por consenso son rojos los vasos en que la dirección del flujo sanguíneo es hacia el transductor y azules los que se alejan de él, y tanto más claros cuanto mayor es la velocidad a la que se mueven.
Hazte una ecografía doppler sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí
Sus aplicaciones en obstetricia
Este efecto es el que permite a un cardiólogo o un cirujano vascular estudiar las válvulas cardiacas, unas varices o si una arteria tiene reducido su calibre por arteriosclerosis . En el campo de la obstetricia este tipo de imágenes nos son de gran utilidad durante el estudio anatómico del feto para identificar las grandes arterias y venas de su anatomía y el corazón y poder valorar su normalidad o anormalidad.
Al mismo tiempo, podemos medir en un punto concreto de la circulación la velocidad por la que pasa la sangre en esa localización, lo cual tiene distintas e interesantes aplicaciones en la práctica médica, tanto en el protocolo general de control de todos los embarazos, como exploraciones específicas que se realizan en casos concretos con sospecha de patología.
En cuanto a ecografías Doppler que se realizan a todas las gestantes en el contexto de control de un embarazo normal:
Medir el flujo sanguíneo de las arterias que nutren el útero (las arterias uterinas) y detectar en qué casos hay un aumento de la resistencia al paso de la sangre por esos vasos, lo cual nos permite detectar pacientes en riesgo de desarrollar un problema de hipertensión durante el embarazo o de que se presente un retraso de crecimiento fetal y poderlas supervisar más estrechamente.
Valorar en ecografías obstétricas tempranas ciertos marcadores que nos pueden hacer sospechar patologías como el síndrome de Down: medición del Ductus venoso y la regurgitación tricuspídea pueden hacer sospechar de este síndrome.
En casos concretos de sospecha de patología podemos aplicar la ecografia Doppler para valorar casos de:
Anemia fetal: en caso de anemia la sangre es más fluida y, por tanto, va a mayor velocidad. Así, estudiando ecográficamente la velocidad de la sangre en un vaso podemos saber si un feto está anémico.
Retraso de crecimiento : los fetos que ecográficamente diagnosticamos como más pequeños de lo esperado pueden ser de constitución más pequeña o bien que les falte alimento u oxígeno. En este segundo caso la naturaleza prioriza el riego sanguíneo al cerebro a costa de otros órganos no tan prioritarios. Al estudiar con ecografía Doppler el latido de las arterias cerebrales y las del cordón umbilical podemos distinguir entre los fetos que se están “adaptando a unas condiciones hostiles” (por tanto, los que “sufren”) de los que no (es decir, son simplemente pequeños).
Así pues, la ecografía, y la ecografía Doppler son estudios que nos permiten obtener información de gran utilidad de una forma inocua y cómoda.
Hazte una ecografía doppler sin esperas. En Savia contamos con los mejores centros y especialistas. Cómprala ahora aquí

Artículo especializado
Ecografía 5D
¿Qué embarazada no está ansiosa por ver la cara de su bebé? ¿Qué futuro papá o mamá no imagina y fantasea sobre cómo será? Para dar respuesta a esta demanda se ha acelerado el desarrollo de tecnología con ultrasonidos que nos permite ver imágenes sorprendentes del feto dentro del vientre materno.
Un poco de historia…
La historia de la ecografía tiene poco más de 100 años. Se inició en el contexto de la ingeniería y la tecnología militar y no fue hasta mediados del siglo XX cuando se aplicó en medicina. Encontró en el campo de la obstetricia uno de las especialidades en la que más se ha utilizado su tecnología, por su inocuidad a la hora de explorar a las gestantes y por el gran nivel de información que nos ofrece al estar el feto sumergido en agua, que es el medio óptimo por el que se transmiten los ultrasonidos .
La tecnología 2D
La tecnología en la que se basa el diagnóstico actualmente es la “2D” , imágenes en blanco y negro que nos ofrecen cortes de los tejidos. Es como exploramos habitualmente los fetos para rastrear su anatomía y descartar malformaciones. Los aparatos actuales ofrecen imágenes cada vez más nítidas y precisas. Para ello se usan ultrasonidos, ondas de alta frecuencia que se aplican mediante un transductor sobre la piel de la paciente lo más cerca posible del órgano a explorar. Para favorecer su difusión se aplica sobre la piel un gel acuoso y estas ondas, al llegar a los distintos tejidos, rebotan en una frecuencia u otra según su densidad y profundidad, y el rebote es recogido por el mismo transductor (emisor-receptor). Un software interpreta los datos recogidos y los plasma en una imagen en la pantalla del ecógrafo en diferentes tonalidades de gris.
La tecnología 3D y 4D
Hace poco más de una década se desarrolló la tecnología 3D , con la que un “barrido” en dos dimensiones sobre un tejido a explorar, procesado por un ordenador, componía una imagen fija con aspecto de tres dimensiones. Con el tiempo se sofisticó y se podían ver estas imágenes 3D en movimiento en tiempo real. Aplicado a la obstetricia nos permite ver al feto moviéndose, gesticulando, bostezando, parpadeando… A esta nueva tecnología se la llamó 4D.
Hasta llegar a la tecnología 5D
Recientemente se ha mejorado el software que permite la composición y el tratamiento de la imagen, cambiando el tono sepia de las 3 y 4D por un tono rosado con más tonos de sombra y textura, como si se tratara de una imagen real del feto iluminado, dándole el nombre de 5D . En realidad, no hay mucha diferencia entre la 4 y 5D pues es la misma tecnología mejorada, lo ofrece resultados mucho más vistosos en cuanto a realismo .
No tiene finalidad diagnóstica
Tal y como está planteado en el mercado actualmente la ecografía 4-5D es más bien una exploración “festiva” cuya pretensión es obtener bonitas imágenes del feto en movimiento, de sus rasgos y evolución y no una prueba médica con finalidad diagnóstica. Existen infinidad de centros que realizan este tipo de ecografías:
Algunos en el contexto de un centro médico en el que además se puede hacer el control gestacional y las ecografías con finalidad diagnóstica.
En otro tipo de centros el único propósito es disfrutar de la imagen del feto. Para ello, disponen de aparatos de alta tecnología y personal altamente cualificado para hacer este tipo de ecografías, que no son fáciles de hacer.
PARA QUE QUEDEN BIEN…
Este tipo de ecografía es una exploración que depende mucho de la “colaboración” fetal. Se requiere de una buena posición del feto para obtener buenas imágenes, líquido abundante, cuanto más delgada esté la gestante mejor, si la placenta no obstaculiza la visión también mejor… No siempre se consigue un buen resultado a pesar de la cualificación del técnico o médico y de su mejor intención. En esto la tecnología 5D también ha supuesto un avance pues solventa mejor el problema de las interferencias de órganos o tejidos que se interponen en la imagen.
¿Qué nos llevamos a casa?
Actualmente se pueden contratar exploraciones a precios razonables que además de los 20-30 minutos de exploración en directo nos darán las imágenes registradas en soportes digitales como CD/DVD o lápices de almacenamiento, fotos, incluso proyecciones sobre el vientre materno a la vez que se realiza la ecografía. Se comercializan bonos de dos, tres o más ecografías para poder disfrutar de esas imágenes en distintas etapas del embarazo y así observar la impactante evolución del feto… Infinitas posibilidades para lo que es un negocio con un nicho de mercado interesado.
Más allá de la parte lúdica: una tecnología para el futuro
A parte de esta vertiente más lúdica y conocida de las ecografías 4-5D también hay que saber que existe una indicación médica muy importante de esta tecnología que está en sus inicios pero que tiene un gran futuro, pues nos permite visualizar mejor las posibles alteraciones anatómicas del “exterior” del feto (labio leporino, malformaciones genitales, hernias, malformaciones de las extremidades). Y la adquisición de volúmenes de imágenes que una vez terminada la exploración, cuando la paciente ya está en su casa, permite al médico examinarla desde ángulos distintos a los que la miró en directo y tomar diferentes medidas. Esto es una concepción diferente de lo que se conocía hasta ahora de una ecografía, que era una prueba que se interpretaba a medida que se realizaba.
Pruebas inocuas
Tanto la ecografía clásica como la 4-5D son absolutamente inocuas tanto para la madre como para el feto, indoloras y que se pueden realizar con la asiduidad que las condiciones requieran o permitan. No hace falta preparación alguna, en etapas precoces de embarazo se pueden realizar por vía vaginal y, si no, por el abdomen. En este caso se requerirá que la vejiga urinaria esté llena para que el líquido que contiene permita el paso de los ultrasonidos al útero que está detrás.
¿Cuándo es mejor realizarla?
De escoger una única fecha para realizar una ecografía 5D lo ideal es que sea entre la semana 26-30 , aunque se puede realizar en cualquier momento del embarazo. Se recomienda no ponerse cremas hidratantes o antiestrías el día de la exploración porque determinados componentes pueden interferir con la transmisión de los ultrasonidos y restar nitidez. Si el feto está colocado en una posición que dificulta la visión puede que el técnico/médico te estimule suavemente el abdomen para favorecer que el feto cambie de posición, igual que si está dormido, para conseguir imágenes en actividad que son más sorprendentes. Si no lo conseguimos, a veces se aconseja comer algo dulce , que también tiene la capacidad de activar al feto o volver en otro momento si realmente no se han conseguido imágenes de calidad por la posición fetal.
De todas maneras, no te sientas decepcionada, lo importante es que el resto de pruebas salgan bien y pronto tendrás a tu bebé en tus brazos y ¡podrás verlo tanto como quieras!
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Artículo especializado
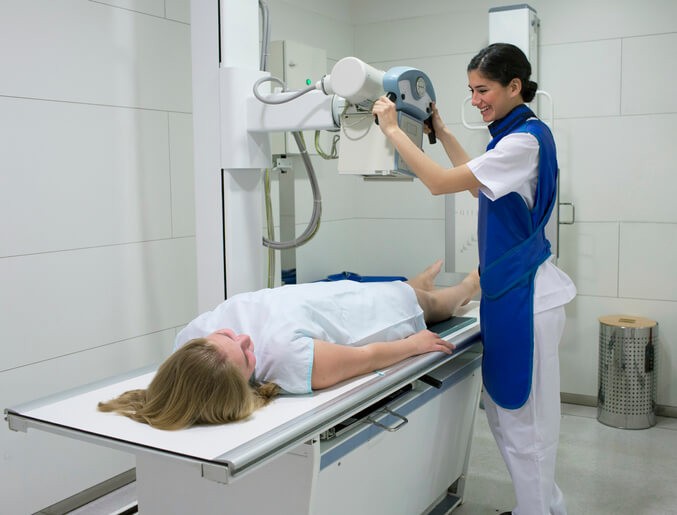
Radiografía y Radiación
Los rayos X constituyen una técnica médica basada en el uso de un tipo de energía (radiación ionizante) que penetra en el organismo y que permite crear imágenes de los órganos. Las radiaciones ionizantes también son la base de otras exploraciones radiológicas como la tomografía axial computarizada (TAC) o la tomografía por emisión de positrones (PET).
La dosis de radiación recibida en el organismo se mide en unas unidades llamadas millisievert (mSv). Se denomina “dosis efectiva” y es la que reciben los tejidos durante un procedimiento radiológico (radiografía, TAC o PET).
Sobre la radiación
Habitualmente estamos expuestos a una radiación natural de fondo, es decir, en el medioambiente hay diversas fuentes naturales de radiactividad . Es útil conocerla pues sirve de comparativo frente a la radiación recibida por exámenes radiológicos.
Los efectos de la radiación dependen de diversos factores como el sexo, la edad (son más sensibles los niños), los órganos que la reciben (por ejemplo, la glándula tiroides es más sensible) y el tipo de técnica utilizada. Así, la dosis efectiva recibida será variable y es la que se utiliza para medir los riesgos potenciales de la radiación sobre la salud. En países como Estados Unidos la radiación de fondo de promedio se ha calculado en 3mSv por habitante durante un año.
¿Riesgos?
El principal riesgo del uso de las radiaciones ionizantes es el aumento de cáncer. Los datos objetivos indican que las dosis que se reciben en las pruebas diagnósticas son muy bajas puesto que la dosis recibida es muy pequeña. Si se compara con la radiación de fondo, es decir, la exposición diaria a otras fuentes, la exposición sería la siguiente:
Radiografía simple (la más frecuente): radiación de 0.1msV
La mamografía: radiación de 0.4 mSv
Otras exploraciones como el TAC y el PET exponen a cifras más altas: de 2 a 10mSv y 25 mSv respectivamente.
La Organización Mundial de la Salud (OMS), a modo orientativo, ha establecido el límite recomendable de un máximo de 10 radiografías/año. Los expertos en radiación han estimado que la probabilidad de presentar cáncer por haber sido sometido a estudios radiológicos es extremadamente baja, frente a otros factores de riesgo conocidos (como el tabaco).
Por otro lado, es difícil calcular el riesgo aislado de un individuo que ha recibido dosis de radiación por exploraciones médicas, dado que los estudios científicos realizados se han hecho sobre grupos de población sometidos a una radiación muy alta (por ejemplo, tras un desastre en una central nuclear) motivo por el cual no son extrapolables. Además, cualquier persona está expuesta a otras fuentes (“radiación de fondo”) que interfieren en el cálculo del riesgo.
Bajo control
El desarrollo de la tecnología y de otras técnicas de imagen también ha permitido disminuir el tiempo de exposición a las técnicas radiológicas, utilizar la menor dosis posible y en muchos casos limitar su indicación, que puede ser sustituida por otros medios diagnósticos como la ecografía o la resonancia magnética.
Además, la radiografía se realiza en instalaciones sometidas a control riguroso (tanto para seguridad de los aparatos como del paciente y del personal sanitario habitual).
Contraindicaciones
Existen contraindicaciones claras para la radiografía como es el embarazo . Aunque el riesgo se considera bajo para el feto se deben evitar, y optar por otras técnicas como la ecografía. En mujeres en edad fértil, para minimizar el riesgo por si hubiera embarazo, se aconseja realizar estas exploraciones justo después de la menstruación.
A modo de conclusión, está comprobado que las grandes dosis de radiación pueden provocar claramente mutaciones celulares que generen un cáncer y que además pueden dañar directamente los tejidos (quemadura). Sin embargo, las radiografías y otras técnicas similares como el PET o el TAC utilizadas de forma justificada y puntualmente no tienen por qué tener ninguna repercusión sobre la salud del paciente.
Artículo especializado
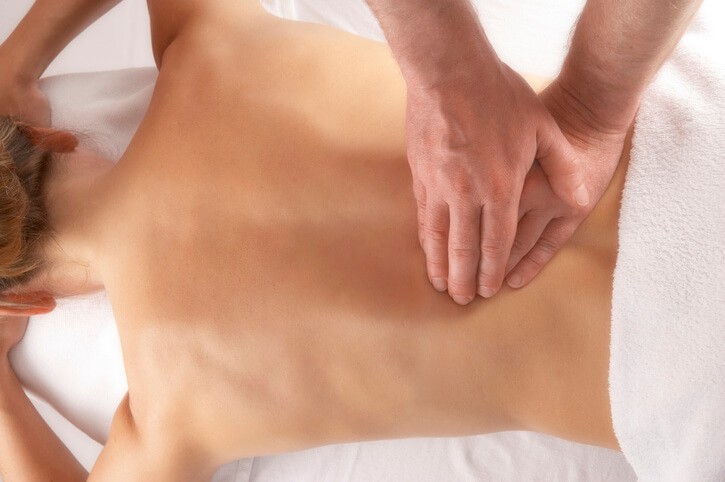
Despeja Tus Dudas sobre la Hernia Discal
Es la mayor causa de incapacidad en personas menores de 45 años , ¿lo sabías? ¿Y qué tiene que ver una hernia discal con una ciática? ¿Qué diferencia hay entre protusión y hernia discal? ¿Se ve una hernia discal en una radiografía? Son muchas las preguntas para formular ante esta patología tan frecuente.
¿Qué es una hernia discal?
Es una enfermedad que afecta al disco intervertebral , que es una estructura cartilaginosa que se encuentra entre las vértebras confiriéndoles capacidad de amortiguación. Este disco consta de dos partes claramente diferenciadas: anillo fibroso o halo periférico y núcleo pulposo o zona central de consistencia gelatinosa, cuyo contenido es un 88% de agua. Cuando el núcleo pulposo del disco intervertebral se desplaza hacia el exterior empuja al anillo fibroso e incluso puede llegar a romperlo. Es entonces cuando el núcleo pulposo ocupa un espacio anatómico que no le corresponde y compromete las estructuras de dicha área. Cuando el desplazamiento es en dirección lateral (derecha o izquierda) producirá una ocupación del canal medular que se traduce en una compresión y/o desplazamiento de la raíz nerviosa que discurre por allí, originando síntomas neurológicos (hormigueos, pérdida de fuerza o sensibilidad).
¿Cuál es exactamente la diferencia entre protusión y hernia discal?
La diferencia radica en la cantidad de disco desplazado . Si es menor del 50% del disco se llama protusión discal, mientras que si es mayor hablaremos de hernia discal. Es importante aclarar que el tamaño de la hernia no tiene correlación con los síntomas. Tiene más trascendencia la ubicación anatómica que el tamaño de la hernia.
Las ubicaciones más frecuentes de las hernias discales son: región lumbar (entre los espacios L4-L5 y L5-S1, que suponen el 95% de los casos) y región cervical (entre los espacios C5-C6 y C6-C7).
¿Qué síntomas puede dar una hernia?
En función de la ubicación la hernia producirá dolor en la región lumbar (lumbalgia) o cervical (cervicalgia). Se acompañará por un cortejo de síntomas asociados según la estructura anatómica que se vea comprometida por el disco herniado.
Podremos encontrar una alteración de la fuerza de la extremidad, una alteración de la sensibilidad, una afectación motora (disminución de la movilidad), una radiculagia (braquialgia o ciatalgia) e incluso mal control de los esfínteres.
¿Todas las lumbalgias tienen una hernia discal de base? En absoluto. A pesar de que la lumbalgia mecánica es uno de los principales motivos de consulta en urgencias de traumatología sospecharemos una implicación discal sólo ante determinados síntomas como pueden ser la sensación de hormigueo o la dificultad para el movimiento de la pierna. En caso de detectar estos síntomas investigaremos la raíz nerviosa afectada. Al realizar la exploración es muy probable que detectemos una disminución de los reflejos en la zona afectada.
¿Qué exploración y pruebas diagnósticas realizaremos?
Ante un dolor cervical o lumbar debemos realizar un buen interrogatorio y una exploración física exhaustiva (donde podremos valorar posibles deformidades, asimetría de extremidades y alteraciones neurológicas). Se deben explorar la fuerza, los reflejos y la sensibilidad de las raíces nerviosas locales.
En el caso concreto de una lumbociatalgia o ciática, aproximadamente el 90% de los casos será debido a una hernia discal que comprime una raíz nerviosa (casi siempre L5 o S1). El síntoma guía es un dolor irradiado hacia la extremidad inferior que puede llegar hasta el pie.
La primera prueba diagnóstica a realizar sería una radiografía de columna, aunque no nos permitirá la visualización del disco intervertebral por ser radiotransparente. Posteriormente se solicitarán otras pruebas de imagen para completar el estudio (resonancia magnética o tomografía computarizada). La resonancia magnética nuclear es el método de elección para evaluar la morfología del disco intervertebral. Las pruebas de imagen deben pedirse de forma inmediata ante la sospecha de patología vertebral grave. Uno de los objetivos de las pruebas de imagen es identificar a los pacientes candidatos a tratamiento quirúrgico.
Debemos mencionar la electromiografía por ser la siguiente prueba diagnóstica a realizar cuando detectamos una hernia discal que compromete una raíz nerviosa. Es una prueba que nos permite estudiar alteraciones en la conducción nerviosa. Valora el sistema nervioso periférico (nervio y músculo).
¿Cuál sería el tratamiento de elección?
Existen numerosas opciones terapéuticas disponibles. Sin embargo, ningún tratamiento ha demostrado ser más beneficioso que otros.
El tratamiento médico puede consistir en analgésicos, miorrelajantes, corticoides, antinflamatorios …, en función de los síntomas predominantes.
Otros tratamientos coadyuvantes pueden ser contemplados, como la fisioterapia y la rehabilitación. En fase de mantenimiento la práctica de natación sería de gran utilidad para tonificar la musculatura paravertebral.
En dolores rebeldes al tratamiento convencional o con mala respuesta al mismo puede indicarse el tratamiento en la Clínica del Dolor (supervisado por anestesistas que suelen infiltrar el foco del dolor con agujas dirigidas por escopia).
El tratamiento quirúrgico se reserva para aquellos casos en los que los tratamientos anteriores no han sido efectivos. Esta patología puede ser intervenida por el traumatólogo o por el neurocirujano. El tratamiento quirúrgico estrella es la discectomía (resección del disco herniado mediante laminectomía o hemilaminectomía). Otras opciones quirúrgicas serían la discólisis (desecación del disco con ozono), la artroplastia (fijación de dos o más vértebras consecutivas para descomprimir el disco intervertebral afecto), etc.
Como ves existen múltiples abordajes terapéuticos. La tendencia es conservadora. Se descarta la opción quirúrgica en aquellos pacientes con buena respuesta al tratamiento médico. Sin embargo, se contempla la opción quirúrgica en aquellos pacientes con afectación neurológica importante y dolor invalidante. Entre ambos extremos encontramos la mayoría de los casos.

Artículo especializado
Etapas del Cáncer de Vejiga
Existe cura para el cáncer de vejiga, y es que hasta el 80% de pacientes diagnosticados de este tipo de tumores sobrevivirán más allá de cinco años tras su diagnóstico. Este porcentaje es incluso superior en España respecto a otros países desarrollados, ya que la supervivencia media a cinco años en la Unión Europea se sitúa en torno al 69%.
Más frecuente en hombres
El cáncer de vejiga es el quinto cáncer más frecuencia en nuestro país , con más de 21.000 nuevos casos anuales. Pese a esta prevalencia, es el octavo tipo de cáncer por mortalidad, siendo el responsable de unas 4.300 muertes al año. Su frecuencia es muy superior en el sexo masculino , con más de 17.000 casos anualmente respecto a los 3.600 nuevos casos que se diagnostican en el sexo femenino. Por edades suele afectar a personas entre los 65 y 75 años, con el pico de incidencia alrededor de los 70 años.
¿Qué es?
El cáncer es una enfermedad producida por una mutación genética que provoca una reproducción incontrolada de las células de un tejido. Dicha reproducción incontrolada provoca un crecimiento del tumor que va invadiendo los tejidos de su alrededor y que en ocasiones puede infiltrarse en un vaso sanguíneo y migrar e implantarse en otros órganos ocasionando las metástasis.
El cáncer de vejiga es un tipo de cáncer que se origina frecuentemente en la capa mucosa de la vejiga (la capa interna que está en contacto con la orina), formando así el llamado carcinoma urotelial. En este tipo de tumores, podemos diferenciar dos subtipos:
Cáncer urotelial de bajo grado : rara vez invade tejidos en profundidad u ocasiona metástasis a distancia, pero sin embargo tiene tendencia de reaparecer tras su extirpación
Cáncer urotelial de alto grado : más agresivo. Va invadiendo los tejidos que lo rodean, en profundidad en la vejiga, y en ocasiones puede extenderse a otros órganos provocando metástasis.
¿Qué factores de riesgo existen?
El principal factor de riesgo evitable para el cáncer de vejiga es el tabaquismo . Se estima que los fumadores tienen el triple de riesgo de desarrollar un cáncer vesical respecto a los no fumadores. Esto puede ser producido porque muchos de los tóxicos del tabaco se eliminan por la orina.
Además del tabaquismo, los antecedentes familiares de cáncer de vejiga representan otro factor de riesgo importante para la aparición de un cáncer vesical.
Existen otros factores de riesgo, pero con una importancia menor como son las exposiciones a sustancias químicas como colorantes, derivados del petróleo o arsénico, entre otros.
¿Cómo se presenta?
El síntoma más frecuente en el cáncer vesical es la hematuria (la presencia de sangre en la orina). Sin embargo, ésta puede ser provocada por múltiples enfermedades como por ejemplo la presencia de piedras en los conductos urinarios (cólicos nefríticos), infecciones (cistitis) o enfermedades renales.
Al contrario que en la mayoría de enfermedades que pueden producir sangrado por la orina, el ocasionado por un cáncer de vejiga suele ser asintomático, es decir, el paciente únicamente verá sangre en la orina, pero no presentará molestias importantes, dolor ni otra sintomatología.
Además de la hematuria, los tumores vesicales pueden presentarse como polaquiuria (aumento de la frecuencia de micciones), disuria (molestias al orinar), nicturia (aumento de las micciones durante la noche) o tenesmo urinario (sensación continua de ganas de orinar).
¿Cómo se diagnostica?
La primera prueba diagnóstica que habrá que hacer es un análisis de orina y un análisis sanguíneo . Con ellos descartaremos otras causas de hematuria. Además, en algunos casos permite visualizar células tumorales que se expulsan con la orina, lo que nos permitiría asegurar que existe un cáncer en las vías urinarias, aunque no nos daría la localización exacta (podría tratarse de un tumor vesical pero también de un tumor en algún otro punto de las vías urinarias como los uréteres o la uretra).
La ecografía es una técnica útil en algunos casos ya que permite visualizar el tumor dándonos información de su tamaño y posible afectación de otros órganos.
La urografía endovenosa es una prueba radiológica que permite visualizar las vías urinarias y descartar la existencia de otras tumoraciones a lo largo de las mismas.
Pero ante todas, la prueba más útil en el diagnóstico del cáncer vesical es la cistoscopia. Es una técnica que consiste en introducir un tubo muy fino con una cámara en su punta, a través de la uretra para así poder visualizar el interior de la vejiga. Permite así ver directamente el tumor, su extensión y coger muestras (biopsias) para analizarlo. Además, como veremos más adelante, en muchas ocasiones permite también extirpar el tumor y tratar así la enfermedad.
Una vez diagnosticado ya el cáncer vesical, se suele hacer un estudio para descartar extensión del tumor a distancia a través de una TAC abdominal , una radiografía o TAC de tórax y en algunos casos una gammagrafía ósea para descartar metástasis en los huesos.
¿Cómo se trata?
La elección del tratamiento dependerá del tipo de tumor y del grado de afectación, tanto en profundidad de la vejiga como por la existencia o no de metástasis a distancia. Los tratamientos disponibles son la cirugía, la radioterapia y la quimioterapia.
En aquellos casos de tumores superficiales (tumores de bajo grado o tumores de alto grado, pero en fases muy precoces) el tratamiento básico será la cirugía. En muchas ocasiones se puede realizar la llamada RTU (resección transuretral), es decir, a través de una cistoscopia se extirpa la zona de tumor pudiendo curar por completo la enfermedad sin tener que hacer incisiones. En otros casos, por el contrario, será necesaria una cirugía mayor que implique una extirpación total o parcial de la vejiga de la orina.
La quimioterapia es otro de los tratamientos habituales en el cáncer vesical. Ésta puede administrarse de forma intravesical (se introduce por la uretra hasta el interior de la vejiga) o intravenosa.
La quimioterapia intravesical se suele utilizar tras una RTU en tumores superficiales y disminuye el riesgo de recidiva (reaparición) de la enfermedad. La quimioterapia intravenosa se emplea frecuentemente en caso de que existan metástasis o haya riesgo de que éstas aparezcan.
¿Y después del tratamiento?
Como ya hemos dicho, el cáncer vesical es un cáncer frecuente , pero en muchas ocasiones curable . Sin embargo, existe un riesgo elevado de recidivas, ya sea por reaparición del mismo tumor como por la aparición de otros tumores a nivel vesical. Se estima que el riesgo de recidiva en este tipo de tumores está entre un 40 y un 70%, aunque hay estudios que elevan ese porcentaje hasta el 90%. Por este motivo, es de especial importancia realizar un buen seguimiento tras haber superado un cáncer vesical, en muchas ocasiones incluso realizando cistoscopias seriadas para descartar la aparición de nuevas tumoraciones.
Artículo especializado
Pronóstico, Analítica y Test para Detectar el Cáncer de Pancreas
Infrecuente pero muy agresivo, el cáncer de páncreas es, además, difícil de diagnosticar en etapas tempranas porque, cuando da síntomas, en general ya suele estar en un estado avanzado, y muchas veces los síntomas son tan inespecíficos que se tarda en acudir al médico. Modificar los factores de riesgo que pueden propiciarlo está en nuestras manos, así que ¿por qué no hacerlo?
Cómo se produce
El cáncer de páncreas se origina cuando las células del páncreas comienzan a proliferar sin control y van acumulando cambios en la replicación del ADN que las hace invasivas y agresivas.
El páncreas tiene dos tipos de células, las exocrinas, que son las que producen una serie de enzimas que ayudan en la digestión de los alimentos, y las endocrinas , que producen diferentes hormonas, como la insulina o el glucagón. La mayoría de los tumores del páncreas se localizan en las células exocrinas , causando un adenocarcinoma de páncreas, mientras que los tumores endocrinos del páncreas son menos comunes.
Incidencia del tumor
No es un tumor muy frecuente : representa apenas el 2% del total de todos los cánceres). Cada año se diagnostican en el mundo unos 233.000 nuevos casos en todo el mundo. En España se detectan unos 4.000 casos anuales. Es un tumor un tanto más frecuente en los hombres que en las mujeres . La mayoría de los tumores de páncreas se diagnostican en personas entre los 65 y los 75 años.
Factores de riesgo
Este cáncer se ha relacionado con diversos factores de riesgo :
Hábito tabáquico.
Dietas ricas en grasas y en proteínas.
Pancreatitis crónica.
Cirrosis hepática.
Diabetes.
Colecistectomía.
Exposición a ciertos productos químicos (tintorería, industria metalúrgica).
Predisposición genética.
UN CÁNCER MUY AGRESIVO
El cáncer de páncreas es muy agresivo y se extiende a los tejidos que lo rodean con suma facilidad . Un 70% se diseminan a través de los vasos linfáticos y más del 50% lo hacen también por la sangre, de manera que las metástasis son habituales, sobre todo en el hígado, el peritoneo (la membrana que reviste por dentro la cavidad abdominal y sus órganos) o los pulmones.
Los estudios indican que un elevado número de cánceres de páncreas presentan alteraciones en unos genes concretos , el gen ras y el gen p53, ya sea en uno de ellos o muchas veces en ambos.
Síntomas
Por desgracia, la mayoría de estos tumores se detectan en un estado avanzado . El dolor de abdomen es el síntoma más habitual de este tipo de tumores. Suele tratarse de un dolor sordo y constante que se ubica en la zona superior e izquierda del abdomen y que se extiende hacia la espalda. Con frecuencia los pacientes lo describen como si les apretase un cinturón . Suele ser más frecuente durante la noche, no deja dormir. Se suele agravar al comer y al tumbarse, mientras que los pacientes explican un ligero alivio al inclinarse hacia adelante.
La pérdida de peso debida a un déficit de absorción de nutrientes suele ser el síntoma más precoz . Suele acompañarse de falta de apetito, cansancio importante y diarreas, al no poder digerir bien los alimentos por la alteración en la producción de las hormonas digestivas que produce el páncreas.
Otros síntomas habituales de los pacientes con cáncer de páncreas pueden ser:
Ictericia (coloración amarillenta de la piel por acumulación de bilirrubina).
Náuseas y vómitos .
Intolerancia a la glucosa o diabetes .
Pancreatitis aguda .
Es difícil diagnosticar el cáncer de páncreas en sus etapas tempranas porque, cuando da síntomas, en general, ya suele estar en un estado avanzado, y muchas veces los síntomas son tan inespecíficos que se tarda en acudir al médico. Hoy en día no existen pruebas de detección precoz ni se realiza ningún tipo de cribaje para el cáncer de páncreas.
Cómo se diagnostica
No existen marcadores específicos para el cáncer de páncreas que se puedan detectar en una analítica. Existen unos marcadores tumorales, el CEA y el CA 19.9 , que pueden estar elevados en los pacientes con cáncer de páncreas, pero son muy poco específicos. Es decir, pueden estar elevados como no estarlo y estos marcadores pueden aparecer elevados también por otros motivos que no sean el cáncer de páncreas, de manera que no son una herramienta útil para el diagnóstico de este tumor . Estos marcadores tumorales, como todos, son útiles, si están elevados, para valorar la respuesta a los tratamientos de quimioterapia, pero no para el diagnóstico de la enfermedad.
En aquellos pacientes con un elevado riesgo de padecer un cáncer de páncreas por una predisposición genética y familiar se pueden hacer estudios genéticos para valorar si existen alteraciones en ciertos genes que aumenten el riesgo de sufrir esta enfermedad . Ahora bien, que estos genes estén alterados no implica necesariamente que se vaya a padecer la enfermedad, sino que existe un riesgo mayor que el de otras personas.
Las principales herramientas para el diagnóstico del cáncer de páncreas siguen siendo los síntomas del paciente y las diferentes pruebas de imagen, como la ecografía, la ecoendoscopia, el escáner, la resonancia magnética nuclear o la tomografía por emisión de positrones (PET) . En una analítica de sangre se puede apreciar la elevación de ciertas enzimas hepáticas, como la lipasa y la amilasa, así como alteraciones de los niveles de glucosa o bilirrubina en determinados casos. Una vez se tiene el diagnóstico de sospecha se confirmará con la toma de una muestra de tejido del tumor mediante una PAAF o punción aspiración con aguja fina .
Tratamiento
El tratamiento del cáncer de páncreas dependerá del estadio. Por desgracia tan solo un 10%-20% de los cánceres de páncreas pueden ser tratados mediante cirugía cuando se diagnostican . En el resto de los casos las opciones quirúrgicas son paliativas. La quimioterapia y la radioterapia pueden ayudar a aumentar la supervivencia.
Con todo, el adenocarcinoma de páncreas es uno de los tumores que presentan un peor pronóstico. Se estima que solamente un 5% de las personas que padecen este tipo de tumor sobreviven más allá de 5 años desde el momento del diagnóstico. La mayoría de las muertes se producen a lo largo del primer año desde que se detecta la enfermedad.
LO QUE PODEMOS HACER…
Lo que está en nuestras manos para prevenir este tipo de cáncer, infrecuente pero muy agresivo, es modificar los factores de riesgo que pueden propiciarlo :
Abandonar el consumo de tabaco.
Mantener una dieta sana y equilibrada.
Limitar el consumo de alcohol.
Realizar una actividad física moderada.
Evitar la exposición laboral a ciertos productos químicos.

Artículo especializado
Las Consecuencias que Conlleva tener Cáncer de Ovario
En la sociedad actual, donde existe un auténtico “bombardeo” de información, es posible que hayamos recibido mensajes contradictorios acerca del padecimiento del cáncer de ovario, que pueden desembocar en confusión , alarma o preocupación innecesaria . Por eso, vamos a aclarar conceptos y tratar desde dentro un tema tan sensible para la mujer como es el cáncer de ovario.
Qué consecuencias puede tener
El diagnóstico de cáncer de ovario conlleva una cirugía , y un tratamiento médico que durante algunos meses generará un cambio significativo en la paciente y su entorno más cercano. La extirpación quirúrgica de ambos ovarios, de las trompas de Falopio y del útero conlleva la pérdida de la fertilidad, por lo que las mujeres que quieran tener hijos deberán someterse a una intervención de preservación de la fertilidad previa al tratamiento del cáncer. En el caso de que sea necesario extirpar los ganglios linfáticos situados en la pelvis podría dañarse el sistema linfático, provocándose una linfedema, un trastorno en el que el líquido linfático se acumula en las piernas y provoa su hinchazón.
Cómo se produce
El cáncer de ovario es un tumor, generalmente maligno, que se asienta en los tejidos que conforman este órgano incluido en el aparato reproductor femenino. El ovario es la glándula sexual femenina que produce óvulos y hormonas sexuales (estrógenos, progesterona…). Están situados a ambos lados del útero y serían el equivalente a los testículos masculinos.
El cáncer de ovario es más frecuente en los países industrializados de Europa Occidental, Israel, Canadá y EEUU , y representa entre el 4 y el 5% de los tumores femeninos. Es más común en las edades medias de la vida; la mayoría se diagnostican entre los 45 y los 75 años.
Factores de riesgo
De un modo general, en el medio que nos rodea, existen más de 100 agentes de los cuales se dispone de evidencia científica contrastada para poder asegurar que provocan cáncer a los humanos. En otros casos, no es tan fácil establecer esa relación.
En el caso concreto del cáncer de ovario no se conocen en profundidad los factores de riesgo que pueden inducir a la aparición de la enfermedad. Sin embargo, se han observado algunas circunstancias que pueden influir en su aparición, como son las siguientes:
Edad : como en la mayoría de los tumores, según avanza la edad también lo hace el riesgo de que la mujer sufra cáncer de ovario. No es frecuente antes de los 40 años.
Herencia genética : se calcula que sólo entre el 5% y el 10% de los tumores son hereditarios, es decir, son consecuencia de alteraciones genéticas heredadas de los progenitores. En estos casos, si la madre de una mujer y/o una hermana han presentado cáncer de ovario, de mama o de útero, ésta tiene un mayor riesgo de desarrollar la enfermedad que en la población general.
En las familias con predisposición hereditaria a padecer ciertos tipos de tumores se observan varios individuos integrantes de la familia afectados por el mismo tipo de cáncer (o de diferentes pero relacionados), así como diversas generaciones afectadas (abuela, madre, hija). Generalmente, los tumores hereditarios se diagnostican a una edad más joven de la habitual. El riesgo de padecer cáncer de ovario se correlaciona directamente con anomalías en los genes BRCA1 y BRCA2 (cuando estos genes funcionan adecuadamente, en realidad nos protegen de la aparición de tumores, pero cuando están alterados, aumentan el riesgo de desarrollar cáncer antes de cumplir los 70 años).
No haber tenido hijos : en diversos estudios se ha observado que las mujeres que han tenido varios hijos (multíparas) tienen menos riesgo de desarrollar cáncer de ovario que las que no han tenido hijos (nulíparas).
Anticonceptivos hormonales (ACH) : los anticonceptivos hormonales son fármacos que incluyen hormonas propias del ciclo menstrual femenino (estrógenos y progestágenos), que se utilizan como método de anticoncepción principalmente o, para otras finalidades como la regulación de los síntomas de la endometriosis, por ejemplo.
Vienen en múltiples formatos o presentaciones (comprimidos, anillos vaginales, parches, inyectables…) y se puede elegir el que se adapta mejor a nuestro estilo de vida y necesidades. Se ha constatado que los ACH tienen un efecto protector frente al padecimiento de cáncer de ovario y de endometrio uterino, pero, como contrapartida, son preparaciones que aumentan el riesgo de padecer cáncer de mama, de cérvix uterino y también de hígado.
Terapia hormonal sustitutiva (THS) : es un tratamiento con hormonas que se puede recomendar durante la menopausia para aliviar sus síntomas molestos (p.ej. sofocos, sequedad vaginal, etc.) Probablemente, si estás en la etapa menopáusica y has padecido estos síntomas que alteran tanto la calidad de vida, te habrás planteado si eres una candidata óptima para recibir este tipo de tratamientos. Plantéaselo a tu ginecólogo para poner sobre la mesa los beneficios y riesgos que conllevan, ya que este tipo de tratamientos aumentan el riesgo de padecimiento de cáncer de ovario, de mama y de endometrio, así como también de enfermedades cardiovasculares . Por ello, se intenta limitar al mínimo su uso o, en caso de utilizarse, tomarse a las mínimas dosis útiles y durante el mínimo tiempo posible, debido a que el riesgo disminuye progresivamente una vez se abandona el tratamiento.
Otros factores de riesgo serían: seguir dieta rica en grasas, el sobrepeso, el consumo de tóxicos como el tabaco, alcohol, y /o la exposición a radiaciones ionizantes (Rx, TC, radioterapia…), entre otros.
QUÉ PROTEGE
Los embarazos, la terapia anticonceptiva y dar lactancia materna protegen del cáncer de ovario, y en menor medida también son protectores el ejercicio moderado y seguir una dieta pobre en grasas animales y rica en frutas y vegetales.
Síntomas
Por lo general, el cáncer de ovario produce pocos síntomas, o directamente ninguno , hasta etapas de desarrollo avanzadas. El primer síntoma puede ser un ligero malestar en la parte inferior del abdomen, o hinchazón de este, pero la hemorragia uterina no es frecuente.
Diagnóstico
Debido a la escasez de síntomas anteriormente mencionada, la mayoría de los casos plantean un diagnóstico difícil y se detectan cuando la enfermedad ya está avanzada .
Desgraciadamente, además de ello, no existe actualmente ningún método eficaz que facilite el diagnóstico precoz del cáncer de ovario (no existen pruebas que cumplan los requisitos necesarios en la población general).
Tratamiento y pronóstico
El tratamiento incluye la intervención quirúrgica . En función de los hallazgos de la cirugía, será necesario complementar el tratamiento con quimioterapia .
Es importante tener en cuenta que el diagnóstico precoz permite reducir el impacto sobre la salud y la calidad de vida de la paciente, así como mejorarse el pronóstico de supervivencia .

Artículo especializado
Pruebas para Detectar el Cáncer Colorrectal
Es así, no existe una forma eficaz de prevenir la aparició n de un cáncer colorrectal, el tumor maligno más frecuente en nuestro país (con más de 40.000 nuevos casos cada año). Por suerte, contamos con pruebas de detección precoz y otras que nos pueden ayudar al diagnóstico y posterior tratamiento. Además, evitando algunos factores de riesgo podemos reducir la probabilidad de que aparezca. Por tanto, si hay algo en nuestra mano para evitarlo… ¡a qué esperamos!
Cómo se produce
El cáncer colorrectal es el tumor que afecta al colon (conocido como intestino grueso) o al recto (tramo final del intestino de unos 15 cm de longitud que desemboca en el ano). Se produce cuando algunas células del intestino sufren una mutación genética que provoca que se reproduzcan sin control, generando entonces una tumoración que crece continuamente afectando a los tejidos de alrededor. Esas células, frecuentemente obtienen la capacidad de entrar en el torrente sanguíneo , trasladarse a otros órganos del cuerpo, implantarse en esos órganos y seguir creciendo sin control, originando así las metástasis.
Causas
No existe una causa conocida que explique la aparición un cáncer colorrectal, pero sí hay varios factores que pueden favorecer su aparición:
Edad: suele presentarse en pacientes de más de 50 años. La edad media de aparición se sitúa en torno a los 65-70 años .
Sexo: existe una mayor predisposición en el sexo masculino (se diagnostican más de 24.000 casos nuevos anualmente en hombres frente a los 16.000 en mujeres).
Antecedentes familiares: tan solo un 5% de los cánceres de colon detectados se consideran genéticamente hereditarios (traspasados de padres a hijos a través de alguna mutación genética). Sin embargo, las personas con antecedentes familiares de cáncer de colon tienen aproximadamente el doble de probabilidad de presentar esta enfermedad a lo largo de su vida si los comparamos con personas sin antecedentes familiares de cáncer colorrectal.
Antecedentes personales de otros cánceres : las personas que han sufrido un cáncer colorrectal tienen un riesgo superior al de otras personas de presentar otro cáncer. También existe un riesgo superior en las mujeres que han presentado un cáncer de ovario o de útero.
Enfermedades intestinales: algunos tipos de enfermedades que afectan al intestino pueden aumentar el riesgo de padecer cáncer colorrectal , como por ejemplo la Enfermedad Inflamatoria Intestinal, la Poliposis Adenomatosa Familiar o el Síndrome de Gardner, entre otras.
Pólipos en el colon : los pólipos en el intestino grueso tienen riesgo de acabar degenerando en cáncer colorrectal a lo largo de los años. Por ese motivo, cuando se detectan a través de alguna prueba complementaria se recomienda su extirpación.
Obesidad : se considera que aproximadamente un 17% de los casos de cáncer colorrectal son atribuibles a la obesidad. Esto no quiere decir que la obesidad ocasione en sí misma el cáncer, pero facilita su aparición y dificulta su control, por lo que, erradicando la obesidad podríamos evitar el 17% de casos de cáncer colorrectal, además de prevenir muchas otras enfermedades.
Nutrición : el consumo de carnes rojas y carnes procesadas se relaciona claramente con el riesgo de cáncer colorrectal. Esto no quiere decir que no haya que consumir este tipo de carnes, pero sí que debe evitarse su abuso y consumirlas dentro de una dieta equilibrada.
Tabaquismo : aunque no es uno de los tumores que más claramente se relacionan con el tabaquismo, el cáncer colorrectal es más frecuente en personas fumadoras que en las no fumadoras.
Raza: las personas de raza negra tienen una probabilidad de desarrollar un cáncer colorrectal superior al de otras razas.
Síntomas
Gran parte de los casos de cáncer colorrectal no presentan síntomas hasta fases avanzadas , pero en muchos otros casos aparecen un conjunto de síntomas que, correctamente interpretados, pueden ayudarnos a diagnosticar precozmente la enfermedad. Los más frecuentes son:
Alteraciones del ritmo gastrointestinal : alternar deposiciones sólidas con deposiciones líquidas de manera repetida.
Sangrado con las deposiciones .
Tenesmo : sensación de vaciado incompleto tras la deposición.
Pérdida de peso sin causa aparente .
Anemia ferropénica (por déficit de hierro) sin otra causa que lo justifique
Existen otras manifestaciones pero que pueden ser muy inespecíficas y se presentan en muchas otras enfermedades intestinales, como por ejemplo molestias abdominales, distensión abdominal, cansancio y fatiga.
Detección precoz
Dado que el cáncer colorrectal suele aparecer en personas de más de 50 años , en muchas localidades de nuestro país se han empezado a realizar pruebas de screening (detección precoz) basadas principalmente en la detección de sangre oculta en heces . Estas pruebas consisten en la recogida de tres muestras de heces en las que se analiza si existen restos de sangre. En caso de que la prueba sea positiva , se debe continuar un estudio para comprobar el origen de la sangre, ya que problemas como hemorroides o fisuras anales pueden ser los causantes.
¿SABÍAS QUE…
La detección de marcadores tumorales (CEA) en el análisis sanguíneo no debería utilizarse como método de detección precoz de cáncer colorrectal, puesto que, por un lado, el 40% de los cánceres colorrectales no elevan los marcadores tumorales y, además, existen muchos casos de falsos positivos (pacientes que tienen marcadores elevados y sin embargo no presentan cáncer de colon).
Diagnóstico
El diagnóstico definitivo del cáncer colorrectal se realiza mediante la realización de una colonoscopia (tubo flexible con una cámara que se introduce por el ano y nos permite ver el interior del intestino). Con ella podemos visualizar el tumor y recoger muestras (biopsias) que nos darán el diagnostico específico de qué tipo de tumor se trata.
Hay otras pruebas diagnósticas que nos pueden ayudar en el diagnóstico o en el seguimiento del cáncer colorrectal, como la TAC abdominal , el enema de bario , el estudio de marcadores tumorales , entre otros, pero ninguno de ellos sustituye la colonoscopia para el diagnóstico definitivo.
SOBRE LA COLONOSCOPIA…
Es importante destacar que la colonoscopia es una prueba invasiva , no exenta de riesgos, incluso a veces potencialmente graves. En muchas ocasiones nos encontramos pacientes que, sin tener ningún factor de riesgo o ninguna sintomatología, quieren que se les realice una colonoscopia para descartar la existencia de un cáncer colorrectal. En esas ocasiones, se debe explicar correctamente los riesgos que conlleva la realización de dicha prueba y evaluar si compensa asumir esos riesgos frente a la posibilidad de detectar un tumor de colon en una persona asintomática y sin factores de riesgo.
Tratamiento
El tratamiento del cáncer colorrectal dependerá de múltiples factores, entre los que destacan la localización del tumor y su grado de diseminación (tanto local, en la zona del intestino en la que se ha originado, como a distancia, si ha hecho metástasis).
En la mayor parte de los casos, el tratamiento es quirúrgico acompañado de quimioterapia antes y/o después de la operación. En los casos de cáncer de recto (parte final del intestino antes de desembocar en el ano) se puede añadir también tratamiento con radioterapia.
Prevención
No existe una forma eficaz de prevenir la aparición de un cáncer colorrectal, aunque evitando los factores de riesgo ya explicados, podemos disminuir la probabilidad de que aparezca .
Pronóstico
La supervivencia global del cáncer colorrectal a los cinco años se estima en torno a un 63%, es decir, que el 63% de los pacientes diagnosticados vivirán más de cinco años. El pronóstico dependerá mucho de lo evolucionada que esté la enfermedad en el momento de su detección . Así, en los casos en los que el diagnóstico se realiza muy tempranamente (estado A de la enfermedad), la supervivencia puede aumentar hasta el 90%.

Artículo especializado
Pruebas durante el Embarazo
El embarazo, y dar a luz un bebé sano, es un proceso fisiológico casi mágico. Son infinitas las posibilidades de que algo falle, pero, por suerte, la mayoría llegan a término perfectamente. La naturaleza normalmente ayuda, pero hay algunos casos en que aparecen complicaciones y para ello hay una batería de pruebas que se realizan a lo largo del embarazo que nos permiten asegurarnos del bienestar tanto de la madre como del bebé.
Pruebas de primer trimestre
Ecografía de diagnóstico : se suele realizar una ecografía al inicio del embarazo, entre la sexta y octava semana para confirmar el embarazo y que está correctamente situado. Se confirma si es único o múltiple y se comprueba que corresponde a las semanas respecto a la última regla.
Ecografía de la semana 12: en esta fecha el feto es suficientemente grande como para mostrarnos ya parte de su anatomía y poder descartar malformaciones graves ya visibles ahora. También es el momento óptimo para valorar factores de riesgo de síndrome de Down: el más importante es la translucencia nucal. Se trata de una banda líquida por debajo de la piel de la nuca del feto que se ha relacionado directamente con el síndrome de Down (a mayor grosor de esta banda, más riesgo). Esta estructura anatómica desaparecerá a lo largo del embarazo, y es concretamente alrededor de la semana 12 cuando es más precisa. Otros marcadores indirectos de este síndrome y que son visibles en esta cita son la presencia de hueso nasal, el latido del Ductus venoso y la regurgitación tricuspídea.
Analítica general: pretendemos valorar el estado general de la gestante, si requiere algún suplemento vitamínico, su inmunidad respecto ciertas enfermedades infecciosas, como las hepatitis, el VIH…
Analíticas de diagnóstico prenatal:
Triple screening: es un análisis de sangre en la semana 12 que calculará el riesgo de que el feto sea síndrome de Down en función de tres datos: edad materna, grosor de la translucencia nucal y valor de unas hormonas segregadas durante el embarazo. El resultado se expresa en forma de fracción: una probabilidad entre 100.000 es, por ejemplo, un riesgo mucho menor que 1/100. Si el riesgo es alto o no nos tranquiliza se puede hacer otro tipo de pruebas.
Otra analítica en sangre que tiene como finalidad diagnosticar los síndromes de Down es el Test Prenatal no Invasivo. Este test aísla en sangre materna fragmentos de ADN del feto o fetos y puede resolver con un valor predictivo positivo próximo al 100%. Se puede realizar a partir de la semana 10.
Amniocentesis o la biopsia corial , la amniocentesis es una punción sobre la bolsa amniótica para extraer una pequeña cantidad de líquido amniótico en el que flotan células del feto. Se realiza alrededor de la semana 15. La biopsia corial consiste en obtener mediante punción de la placenta células de la placenta, se puede hacer a partir de la semana 12. Tanto las células fetales como las placentarias nos permitirán su estudio y en este caso, con toda seguridad, saber si tiene un síndrome cromosómico o enfermedad genética.
Pruebas de segundo trimestre
Ecografía de la semana 20: a estas alturas de embarazo ya podemos realizar un rastreo completo de toda la anatomía fetal y descartar malformaciones y valorar el crecimiento fetal.
Análisis de sangre para valorar el estado de la gestante, si el embarazo está causando un poco de anemia, estado inmunitario respecto determinadas infecciones y Test de O’Sullivan, para medir niveles de glucosa en sangre después de haber tomado una sobrecarga oral de azúcar, con objeto de diagnosticar diabetes del embarazo. Se suele realizar entre la semana 25-27, aunque en determinadas gestantes se puede repetir en el primer y tercer trimestre.
Pruebas de tercer trimestre
Ecografía de tercer trimestre , generalmente sobre la semana 32, para ver cómo van evolucionando los órganos fetales, repasar la anatomía y valorar el crecimiento fetal y hacer un pronóstico de su peso
Analítica de tercer trimestre , sobre la semana 34-36, para seguir evaluando el estado de la gestante y tener unas pruebas de coagulación recientes en el momento del parto que no contraindiquen la anestesia peridural o aumenten el riesgo de sangrado durante el parto.
Cultivo vaginal y rectal, para detectar un porcentaje importante de gestantes que, de forma asintomática, son portadoras de un microorganismo en su vagina o recto, que forma parte de su flora, que se llama estreptococo Agalactiae o del grupo B. Para la gestante no es problema, pero el recién nacido se puede infectar con él el día del parto y causarle problemas. Al identificar a las gestantes positivas se les administrará una dosis de antibiótico para que el bebé no se lo encuentre cuando salga.
Monitorización de la frecuencia cardiaca fetal o Test no estresante : consiste en registrar durante 20-30 minutos la frecuencia cardiaca del feto y la presencia/ausencia de contracciones mediante unos transductores que se fijan al abdomen de la madre mediante unas cintas elásticas (popularmente se les llama “correas”). Los fetos sanos tienen un patrón característico de FC, que va variando entre 120 y 160 latidos por minuto y que hacen periódicamente aceleraciones puntuales. Este patrón es el que queremos observar durante esta prueba para distinguirlos de un feto que pueda estar sufriendo a causa de falta de oxígeno. Se suelen realizar semanalmente las últimas semanas de embarazo.
Pruebas durante todo el embarazo
Durante todo el embarazo, con una periodicidad más o menos mensual, se realizan visitas en la que supervisamos la evolución del embarazo, incremento de peso, tensión arterial, crecimiento fetal, movimientos fetales…
Con estas pruebas que se realizan comúnmente a todas las embarazadas somos capaces de diagnosticar la mayoría de patologías del embarazo y el feto. En casos concretos, con sospechas concretas, pueden ser necesarias otro tipo de pruebas.
Haz nuestro test de embarazo y averigua todo lo que debe saber una embarazada. Descubre todos los consejos y cuidados de las mujeres embarazadas.
Artículo especializado
Tipos, Diagnóstico y Preparación de la Resonancia Magnética Nuclear
Para obtener imágenes de las estructuras internas del cuerpo humano se utiliza la resonancia magnética nuclear (RMN). Este procedimiento diagnóstico médico utiliza ondas de radio que pasan a través de la zona del cuerpo que se quiere estudiar y que está sometida al efecto de un campo magnético durante la exploración. Permite obtener imágenes de gran calidad y detalle , lo cual ayuda al médico a detectar las variaciones en la forma, consistencia y tamaño de los órganos, y ello puede facilitar mucho el diagnóstico.
Hazte una resonancia magnética sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí
¿En qué consiste?
La RMN emplea un campo magnético potente, ondas de radiofrecuencia y un programa informático que permite transformar las señales captadas en una serie de imágenes muy detalladas de los órganos, tejidos blandos, huesos, y prácticamente el resto de las estructuras internas del cuerpo. La RMN, a diferencia del TAC, no utiliza radiaciones ionizantes, es decir, rayos X. Las ondas de radiofrecuencia realinean los átomos hidrógeno del cuerpo, sin causar ningún cambio químico en los tejidos. A medida que los átomos de hidrógeno regresan a su posición habitual, emiten diferentes cantidades de energía que varía en función del tipo de tejido del cuerpo del que provienen. Dicha energía se capta y crea, mediante un programa informático, una imagen de los tejidos explorados.
¿Cómo se realiza?
La realización de una resonancia magnética nuclear puede estar indicada cuando otras pruebas diagnósticas más sencillas, como una radiografía o una ecografía, no han permitido hacer un diagnóstico de certeza . La RMN es muy útil para estudiar:
Masas tumorales y quistes.
Hemorragias.
Roturas de tejidos blandos.
Infartos.
Aneurismas.
Lesiones intracraneales o cardíacas.
Grandes vasos arteriales.
Columna vertebral.
Glándulas (páncreas, tiroides, suprarrenales).
Órganos abdominales (hígado, vías biliares, bazo, riñones).
Estructuras blandas de las articulaciones y de los músculos (tendones, ligamentos).
Para llevar a cabo una resonancia magnética nuclear, el paciente debe de quitarse las joyas y objetos metálicos o que tengan bandas magnéticas como las tarjetas de crédito o los teléfonos. La realización de la prueba supone someter al paciente a un campo magnético, por lo tanto, cualquier objeto metálico puede provocar alteraciones en la captación de las imágenes.
El paciente deberá permanecer durante todo el tiempo relajado y sin moverse . La realización de la resonancia magnética conlleva más tiempo que la de un TAC. La exploración supone entre tres cuartos de hora y algo más de una hora, en función de la estructura anatómica estudiada. En ocasiones puede que sea preciso sedar al paciente para mejorar la relajación. Durante la prueba se oyen ruidos fuertes, como golpes y sonidos metálicos. Al paciente se le facilitan unas protecciones auditivas para amortiguar el sonido de la exploración.
Hazte una resonancia magnética sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí
¿Y si sufro claustrofobia o me angustia estar encerrado?
Es importante que si se sufre claustrofobia se informe previamente al equipo médico, dado que el paciente debe estar inmóvil durante un largo tiempo dentro de la máquina de la resonancia, que es una estructura cerrada. Hoy en día, sin embargo, existen aparatos de resonancia abiertos que hacen que la realización de la prueba sea menos agobiante. De todos modos, el paciente siempre tiene a mano un pulsador que puede apretar para detener la prueba temporalmente si es preciso.
¿CUÁNDO SE INYECTA CONTRASTE?
En ocasiones, es necesario inyectar contraste para mejorar las imágenes . El material de contraste más comúnmente utilizado para un examen de RMN contiene un metal llamado gadolinio, que se puede usar en pacientes con alergias al contraste yodado. Es mucho menos común que un paciente tenga una alergia al material de contraste a base de gadolinio usado para la resonancia magnética que al contraste yodado empelado en el TAC. No obstante, incluso si el paciente tuviese alergia al contraste con gadolinio, se podría utilizar dicho contraste tras la administración de una medicación adecuada.
En el caso de la mujer…
Las mujeres deben informar siempre de la posibilidad de estar embarazadas . La resonancia magnética se ha empleado desde los años 80 sin que haya habido ningún informe sobre un efecto nocivo en las mujeres embarazadas o en sus bebés. Sin embargo, debido a que el feto estará en un fuerte campo magnético, las mujeres embarazadas no deben hacerse este examen durante los primeros tres a cuatro meses de embarazo, a menos que se asuma que el potencial beneficio de llevar a cabo la resonancia magnética supera con creces los posibles riesgos. El uso del contraste con gadolinio, sin embargo, está contraindicado en las mujeres embarazadas, a menos que sea absolutamente necesario para el tratamiento médico.
¿Es un procedimiento seguro?
En la mayoría de los casos el examen de RMN es seguro para los pacientes que tienen implantes de metal, a excepción de algunos tipos. No se puede realizar una resonancia magnética si se es portador de:
Implante coclear (del oído).
Algunos tipos de clips que se utilizan para los aneurismas cerebrales.
Algunos tipos de bobinas colocadas dentro de los vasos sanguíneos.
Casi todos los desfibriladores y marcapasos cardíacos.
Algunos implantes pueden interferir con el examen o suponer un riesgo potencial al ser sometido al potente imán de la resonancia. Algunos aparatos implantados requieren de un período corto de tiempo después de su colocación (unas seis semanas) antes de poder realizar una resonancia magnética de manera segura. Algunos de estos implantes son:
Válvulas cardíacas artificiales.
Vías de acceso implantables para administrar medicamentos (port-a-cath).
Extremidades artificiales o prótesis metálicas para las articulaciones.
Estimuladores nerviosos implantables.
Broches metálicos, tornillos, placas, stents o grapas quirúrgicas.
La resonancia magnética es, pues, una prueba segura y que permite obtener mucha información. Sin embargo, como siempre, debe ser el médico quien decida si es la prueba más adecuada para el problema que se quiere estudiar. Asimismo, la RMN no es una prueba que se haga nunca de urgencias, salvo en el caso de que se crea que existe una compresión aguda de la médula espinal.
Hazte una resonancia magnética sin esperas. En Savia contamos con los mejores centros y especialistas. Cómpralo ahora aquí

Artículo especializado
Descubre las Causas del Cáncer de Piel
Como cualquier órgano del cuerpo, la piel puede desarrollar tumores malignos o cánceres. Al estar en contacto con el exterior, y muy especialmente con la luz solar, que puede provocar alteraciones en las células, los cánceres de piel son muy frecuentes . Por fortuna, al ser visibles a simple vista, pueden curarse con un diagnóstico precoz y una actuación terapéutica correcta.
¿Qué tipos de cáncer de piel hay?
Existen centenares de tipos de cánceres de la piel, pero los más frecuentes son tres: el carcinoma basocelular, el carcinoma escamoso (también llamados “cáncer de piel no melanoma”) y el melanoma. De ellos, el más grave puede ser el melanoma , por su capacidad de extenderse e invadir otros órganos y provocar la muerte.
¿Cómo se produce el cáncer de piel?
En cualquiera de los tres tipos de cáncer mencionados, la luz solar parece ser el factor más claramente implicado , especialmente el haber padecido muchas quemaduras solares en la infancia o el permanecer muchas horas al sol sin protección adecuada. No es el único factor, ya que vemos melanomas y carcinomas en zonas donde no toca el sol, como las axilas o las plantas de los pies. El tabaco, otras radiaciones o factores genéticos parecen jugar un papel, aunque menos importante que el sol.
Síntomas del cáncer de piel
El carcinoma basocelular suele manifestarse como un granito brillante de crecimiento muy lento o una herida que no cura y crece.
El carcinoma escamoso puede tener un aspecto algo similar, aunque forma más costra, y el crecimiento es más rápido.
El melanoma es muy diferente, ya que se manifiesta como una peca especialmente irregular, asimétrica o de diferentes colores (sobre todo si hay un color muy negro), que puede aparecer sobre una peca presente anteriormente y que ha cambiado, o sobre cualquier otra zona de la piel sin pecas.
Diagnóstico del cáncer de piel
Es importantísimo acudir al dermatólogo a revisarse periódicamente la piel, especialmente si se han padecido muchas quemaduras solares, si hay historia de cáncer de piel en la familia, y si se es una persona de piel y ojos claros.
Los dermatólogos estamos muy bien entrenados para reconocer posibles cánceres de piel, y utilizamos unos dispositivos para la exploración llamados dermatoscopios , que son como pequeños microscopios portátiles que permiten ver el interior de la piel. En caso de necesitar extirpar alguna lesión por sospechosa de cáncer debe hacerse con biopsia para saber el tipo del tumor y para asegurar que está completamente extirpado.
Tratamiento del cáncer de piel
El tratamiento pasa por extirpar el tumor con unos márgenes suficientes para asegurar que no volverá a crecer, e intentando obtener unos resultados estéticos aceptables, ya que una gran mayoría de los cánceres “no melanoma” aparecen en la cara.
En casos de carcinomas basocelulares de tipo infiltrante, existe una técnica denominada cirugía micrográfica de Mohs que asegura la curación en prácticamente el 100 % de los casos. En casos no operables es posible utilizar radioterapia. También existe una quimioterapia llamada vismodegib para los carcinomas basocelulares múltiples, gigantes o no operables.
En el caso del melanoma , los márgenes de extirpación dependerán del grosor del tumor en el momento de extirparlo. Además, en función de la fase de crecimiento en que se encuentra, puede ser necesario buscar afectación de los ganglios (ganglio “centinela”). Asimismo, el dermatólogo u oncólogo buscará extensión de la enfermedad por otros órganos del cuerpo mediante radiografías, TACs, o PETs (diferentes pruebas radiológicas). Para el melanoma con metástasis el pronóstico es malo. Existen diferentes tipos de quimioterapia aprobados.
Medidas preventivas del cáncer de piel
Las medidas preventivas del cáncer de piel se basan en una correcta protección solar y en la detección precoz mediante autoexploración o visita al dermatólogo . En personas con elevado riesgo de melanoma por una historia familiar, por haber padecido muchas quemaduras solares o presentar muchas pecas, se realiza un mapeado de todo el cuerpo con una técnica de microscopía de epiluminiscencia, con el fin de detectar cambios en las pecas o pecas nuevas que pueden ser melanomas incipientes. Un melanoma detectado y extirpado a tiempo puede estar completamente curado.
Artículo especializado
Qué Debes Saber Sobre el TAC
Poco suele interesar saber qué es o cómo funciona hasta que no nos han de realizar uno. Pues bien, si es tu caso, te diremos que mediante las imágenes de un TAC se pueden analizar diferentes estructuras del organismo , lo que permite el diagnóstico de fracturas óseas, hemorragias internas, tumores o infecciones en órganos internos. Sin esta tecnología no podríamos realizar muchos de los diagnósticos de certeza que hoy en día realizamos. Asimismo, permite estudiar la forma de las vértebras de la columna, los discos intervertebrales y la médula espinal.
¿Qué es?
Una tomografía axial computarizada, llamada habitualmente TAC o escáner, es una prueba diagnóstica que emplea la tecnología de los rayos X asociada a un sistema informático que se encarga de procesar las imágenes generadas y que permite, de ese modo, obtener una serie de imágenes que son secciones, es decir, imágenes radiológicas a diferentes planos de profundidad, de las estructuras que se están estudiando. Asimismo, si es preciso, la tecnología informática permite recrear una imagen tridimensional conformada a partir de estas secciones. De hecho, la palabra tomografía deriva del griego y significa literalmente “imágenes de cortes”.
En algunos casos, al realizar la prueba, se puede utilizar un contraste yodado . Se trata de un líquido que se introduce por la vena y que se aprecia en las imágenes, lo cual permite estudiar mejor ciertas estructuras, como los vasos sanguíneos o las cavidades cerebrales con líquido cefalorraquídeo.
¿Qué permite explorar?
El TAC permite explorar diferentes estructuras del organismo :
Cerebro y cráneo.
Senos paranasales.
Dental.
Columna cervical, dorsal y lumbar.
Tórax (mediastino, pulmones, corazón).
Abdominal (hígado, vías biliares, bazo, páncreas, grandes vasos).
Urológico (riñones, uréteres, vejiga, próstata).
Ginecológico (útero, ovarios).
El TAC es una prueba de imagen que no es dolorosa, que dura menos de un minuto y que proporciona imágenes de gran calidad y precisión . En caso de que se tenga que poner contraste puede durar un poco más, dado que se tiene que coger una vía venosa para poder poner el contraste. Si se tiene que utilizar contraste se debe acudir a la prueba en ayunas. En otras ocasiones, para estudiar estructuras digestivas, sobre todo, puede que se tenga que tomar un contraste vía oral o mediante un enema anal. En caso de utilizar contraste la prueba la exploración puede durar un poco más. Siempre debe de informarse al equipo médico de los antecedentes de alergia a contrastes radiológicos.
¿Cómo se realiza?
La exploración se lleva a cabo con el paciente estirado sobre una camilla que se desplaza mecánicamente guiada por el técnico radiólogo. De esta manera se hace avanzar el cuerpo del paciente a través del tomógrafo, que tiene la forma de un aro que rodea al paciente. A medida que se avanza se van realizando las radiografías seriadas que luego el ordenador recompondrá. La persona a la que se le realiza el TAC tiene que estar relajada e inmóvil. En todo momento el paciente es supervisado por los técnicos de radiología, que se comunican con el paciente por un sistema de megafonía, indicando cuándo tiene que aguantar la respiración mientras se realiza la captación de las imágenes.
El TAC, al igual que las radiografías, supone una exposición a rayos X , pero mayor, dado que a efectos prácticos es como realizar muchas radiografías. La unidad de medición de la radiación es el milisievert (mSv). Los diferentes tejidos del cuerpo son más o menos sensibles a estas radiaciones. Mientras que una radiografía de tórax o de abdomen supone una exposición de unos 0,1 y 7 mSv, un TAC conlleva una radiación superior, de 7 y 10 mSV respectivamente. La radiación se acumula y puede causar daño en los tejidos a largo plazo, de manera que es muy importante que el TAC se realice cuando sea realmente preciso y no como una prueba rutinaria.
¿Es seguro?
Se tiene que tomar especial precaución con las mujeres embarazadas . Si el TAC es craneal o torácico no existe ningún problema. Si la exploración supone irradiar la cavidad abdominal o la pelvis y, por lo tanto, el feto, se debe valorar la posibilidad de realizar otro tipo de exploración, como una resonancia magnética o una ecografía.
Asimismo, debido a que los niños son más sensibles a la radiación , se les debe someter a un TAC solamente si dicha prueba fuese esencial para poder llegar a un diagnóstico de certeza. No se les debe realizar estudios por TAC de manera seriada a menos que sea estrictamente necesario para el seguimiento de una enfermedad en concreto.
El TAC es, por lo tanto, una prueba esencialmente sencilla, segura y rápida que nos permite obtener mucha información y facilita el diagnóstico. De todos modos, no siempre es la mejor opción como prueba de imagen, así que tendrá que ser el médico quien determine la pertinencia o no de la realización de una exploración que no está exenta de riesgos, tanto por la radicación como por el contraste.
Contenidos sobre enfermedades
Somos conscientes de que los conceptos médicos pueden resultar confusos si no te los explican con claridad. Para evitar esto, le hemos pedido a nuestros profesionales que preparen estas fichas en donde podrás acceder a información relevante sobre enfermedades que te ayudará a entender de una manera sencilla por qué se producen y por qué es necesario su tratamiento.
Ver todas las enfemedades Artículos por especialidad
CertificadosAlergologíaAnatomía PatológicaAnestesiología y ReanimaciónAngiología y Cirugía VascularAnálisis ClínicosAparato DigestivoCardiologíaChequeosCirugía General y del Aparato DigestivoCirugía General y del Aparato Digestivo PediátricaCirugía Oral y MaxilofacialCirugía Ortopédica y TraumatologíaCirugía Ortopédica y Traumatología PediátricaCirugía PediátricaCirugía Plástica y ReparadoraCirugía TorácicaClínica u HospitalDermatología Médico-Quirúrgica y VenereologíaEndocrinología y NutriciónEnfermeríaFisioterapiaGenética HumanaGinecología y ObstetriciaInmunologíaLogopedia y FoniatríaMedicina Estética y Unidad LaserMedicina Física y RehabilitaciónMedicina GeneralMedicina InternaMedicina NuclearMedicina del DeporteNefrologíaNeumologíaNeurocirugíaNeurofisiología ClínicaNeurologíaNutrición y DietéticaOdontología y EstomatologíaOftalmologíaOncología MédicaOncología RadioterápicaOsteopatíaOtorrinolaringologíaPediatríaPodologíaPoliclínicasPreparación al PartoPsicologíaPsiquiatríaRadiodiagnóstico-Diagnóstico Por ImagenReumatologíaTricologíaUnidad del DolorUrgencias HospitalariasUrología
Todas las especialidades  Savia
Savia
